
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
| 加入稀盐酸的次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 烧杯及反应后混合物的总质量/g | 121.4 | 144.8 | 168.6 | 193.6 |
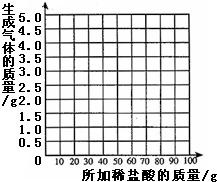
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:阅读理解
 29、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多种顽固污渍”.
29、夏天到了,衣服上常会留下难以清洗的汗渍、果汁渍等.现在市场上出售一种“污渍爆炸盐”,宣称“含天然活性氧,能在瞬间去除洗衣粉难以除去的多种顽固污渍”.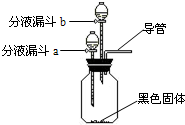
| 序号 | 主要操作步骤 | 主要实验现象 | 操作目的 |
| ① | 在集气瓶中加入少量MnO2(黑色固体);在分液漏斗a中加入新配制的“污渍爆炸盐”的饱和水溶液;在分液漏斗b中加入 稀盐酸 . |
||
| ② | 打开分液漏斗a的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | |
| 然后 用带火星的木条接近导管口 . |
带火星的木条复燃 . |
验证生成气体的成分. | |
| 第②步操作得到的结论: “污渍爆炸盐”溶于水生成过氧化氢 . | |||
| ③ | 待②步反应停止后,打开分液漏斗b的活塞,放出适量溶液后,关闭活塞. | 生成大量无色气体. | |
| 将生成的气体通入 澄清石灰水 . |
澄清石灰水变浑浊 . |
验证生成气体的成分. | |
| 第③步操作得到的结论: “污渍爆炸盐”溶于水生成碳酸钠(或碳酸盐) . | |||
查看答案和解析>>
科目: 来源: 题型:
| 金 属 | 钛 | 铝 | 铜 |
| 与盐酸反应 | 放出气体缓慢 | 放出气泡快 | 无现象 |
查看答案和解析>>
科目: 来源: 题型:
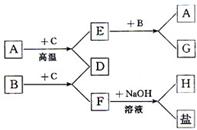 26、图是表示A~H八种物质的关系,其中H为红褐色沉淀物.
26、图是表示A~H八种物质的关系,其中H为红褐色沉淀物.查看答案和解析>>
科目: 来源: 题型:
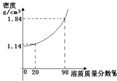 25、右图为硫酸溶液溶质质量分数与密度关系图.
25、右图为硫酸溶液溶质质量分数与密度关系图.查看答案和解析>>
科目: 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com