
科目: 来源: 题型:
| |
的实际质量分数,小明用pH测定仪组成实验装置。实验时先在烧杯中加入20g 40%的氢氧
化钠溶液,再逐滴加入该盐酸,测定仪打印出加入盐酸的质量与烧杯中溶液的pH的关系图
⑴ 请以此次测定的结果,列式计算该盐酸的实际质量分数(5分)?
⑵ 请分析你的计算结果与标签标示的质量分数不一致的可能原因 (1分)___________________________________________________________

查看答案和解析>>
科目: 来源: 题型:
儿童缺锌会引起食欲不振、发育不良。右
图为某种补锌口服液说明书的一部分,请回答:
(1)该口服液中的含锌,其中锌指 (填:“元素或金属或原子);葡萄糖酸锌分子中的碳、氢元素的质量比为 。
(2)每支口服液中含葡萄糖酸锌的质量为 ____ g(1g=1000mg)。
(3)若儿童1kg体重每日需要0.5mg锌,每天从食物中只能摄入所需锌的一半;体重为20kg的儿童每天还须服该口服液 ______ 支,才能满足身体的需要
______ 支,才能满足身体的需要
 |
查看答案和解析>>
科目: 来源: 题型:
小亮在做“盐酸中和氢氧化钠溶液”的实验时,滴加盐酸前忘了加酸碱指示剂,导致无法判断该中和反应进行的程度。于是他对所得溶液的酸碱性进行探究。
【探究目的】 探究所得溶液的酸碱性
【提出猜想】 所得溶液可能呈碱性,也可能呈酸性,还可能呈 ___________性。
【实验验证】
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入无色 | 无色酚酞试液变 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈中性或 |
【分析与思考】
⑴ 若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小亮提出了以下方案:
方案一:取样,加入碳酸钙,若观察到固体消耗并有气泡,则所取溶液呈酸性,有关化学方程式_______ _________________________;若无明显现象,则呈中性。
_________________________;若无明显现象,则呈中性。
 方案二:取样,加入金属锌,若有气泡产生,则所取溶液呈__________;若无明显现象,则呈中性。
方案二:取样,加入金属锌,若有气泡产生,则所取溶液呈__________;若无明显现象,则呈中性。
⑵ 若溶液呈碱性,则溶液中使其呈碱性的离子是 (填写微粒符号),为避免碱性溶液污染环境,小亮对所得溶液进行了如下处理:向溶液中逐滴加入稀盐酸溶液,直到 为止。
查看答案和解析>>
科目: 来源: 题型:
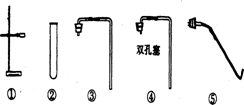 实验室有如下图所示的仪器:
实验室有如下图所示的仪器:
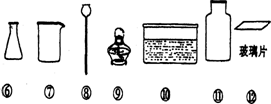
(1)写出下列仪器的名称:
① ;⑧.
(2)实验室用碳酸钙与稀盐酸反应制取并收集CO2气体,若已选用了⑷,⑹,⑾,⑿,还应选用的一种仪器是(填编号): _____。干燥二氧化碳气体可用下图中的甲装置,甲装置中应放_____________干燥剂(填“浓硫酸、氧化钙或氢氧化钠”);若用乙装置测量 二氧化碳气体的体积,图中植物油作用为__________________________________
二氧化碳气体的体积,图中植物油作用为__________________________________
(3) 实验室用高锰酸钾制取氧气的发生装置,除需①②⑤外,还需(填编号):__________,写出用高锰酸钾制取氧气的化学方程式 ,若用下图甲装置并用排水法收集氧气,应先在瓶中装满水,氧气应从 端(填“左”或“右”)导入。

查看答案和解析>>
科目: 来源: 题型:
A为碳酸钠,C为相对分子质量为100白色不溶物,请填空:
(1)B常做食品干燥剂,理由(写化学方程式)_____________________________________
(2)D中一定含有的溶质是________________ ,检验D中是否含有A,可选用的试剂为______ (填下列序号)
a、酚酞溶液 b 、稀盐酸 c 、 澄清石灰水 d、pH试纸

(3)写出A、B和水三种物质的总反应的化学方程式___________________________________________________
(已知 Na2CO3+Ca(OH)2=CaCO3↓+2NaOH)
查看答案和解析>>
科目: 来源: 题型:
某实验室的废水中含有大量AgNO3、Zn(NO3)2和Fe(NO3)2,课外小组同学欲从该废液中回收银,并得到副产品硫酸亚铁晶体。实验方案如下:
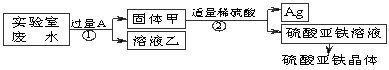 |
(1) 固体甲中含有的物质是(填化学式) ;溶液乙中有颜色的离子符号为 。
(2)写出步骤①的化学方程式: ,反应②的基本类型是_________________________
( 3)检验步骤①向废水中加入A是否过量的物理方法是 。
3)检验步骤①向废水中加入A是否过量的物理方法是 。
(4)加入过量A 的目的是___________________________ __
__
查看答案和解析>>
科目: 来源: 题型:
 某兴趣小组用右图所示装置做酸碱中和反应实验,试回答:
某兴趣小组用右图所示装置做酸碱中和反应实验,试回答:
(1)用胶头滴管吸取盐酸逐滴加入烧杯中,当溶液刚好由 色变成______色时,停止加入盐酸.
(2)实验(1)中,某同学不小心又多加了几滴盐酸,这时溶液的pH _____7(填“>”“<”或“=”),烧杯中溶液的溶质为________________(写化学式)
(3)中和反应在实际中具有广泛的应用,请举出一个实例:
(4)固体氢氧化钠必须密封保存,是因为它在空气中不仅易吸水 而潮解,而且还能跟 发生反应,该反应的化学方程式为 ________________________________ _______
查看答案和解析>>
科目: 来源: 题型:
A、B、C三种固体物质的溶解度曲线如右图所示。
(1)t1℃时,A、B、C的溶解度大小关系是(用“>”、“<”或“=”表示) _____________ ,它们的等质量的饱和溶液中含水的质量最小的是____________
(2)t2℃时,将A、B、C各25 g分别放入100g水中,能形成饱和溶液的物质是 ,而没有形成饱和溶液的,可将溶液温度降到t1℃时,又能恰好形成饱和溶液的是 ;
 (3)t1℃时,将20gA物质充分溶解在50g水中所得溶液的溶质质量为______克
(3)t1℃时,将20gA物质充分溶解在50g水中所得溶液的溶质质量为______克
(4)当温度由t1℃升高至t2℃时(不考虑水分蒸发),乙烧杯中固体质量增加,则乙烧杯溶液中的溶质是 (填A或B或C)
(5)若A溶液中含有少量C,提纯A晶体的结晶方法为____________________

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com