
科目: 来源: 题型:
下列说法正确的是( )
A.常温常压下,只有一种元素的单质呈液态
B.周期表中所有元素都是从自然界中发现的
C.过渡元素不全是金属元素
D.常温常压下,气态单质的分子都是由非金属元素的原子形成的
查看答案和解析>>
科目: 来源: 题型:
铝在人体中积累可使人慢慢中毒,1989年世界卫生组织正式将铝确定为食品污染源之一并加以控制。铝在下列场合使用必须加以控制的是( )
①制铝锭 ②制易拉罐 ③制电线电缆 ④制牙膏皮 ⑤用明矾净水 ⑥制炊具 ⑦用明矾和小苏打作食品膨化剂 ⑧用氢氧化铝〔Al(OH)3〕制成药片治胃病 ⑨制防锈油漆?
A.①②④⑤⑥⑦⑧ B.②⑤⑥⑦⑨
C.②④⑤⑥⑦⑧ D.③④⑤⑥⑦⑧
查看答案和解析>>
科目: 来源: 题型:
在某温度时,一定量的元素A的氢化物AH3在一定体积密闭容器中可完全分解成两种气态单质,此时压强增加了75%。则A单质的一个分子中有_______个A原子,AH3分解反应的化学方程式为__________________________________________。
查看答案和解析>>
科目: 来源: 题型:
N2O5—是一种新型硝化剂,其性质和制备受到人们的关注.
(1)N2O5与苯发生硝化反应生成的硝基苯的结构简式是 。
(2)2N2O5(g)→4NO2(g)+O2(g);ΔH>0
①反应达平衡后,若再通入一定量氮气,则N2O5的转化率将 (填“增大”、“减小”、“不变”)。
②下表为反应在T1温度下的部分实验数据:
| t/s | 0 | 500 | 1000 |
| e(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为 。
③在T3温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2 T1。
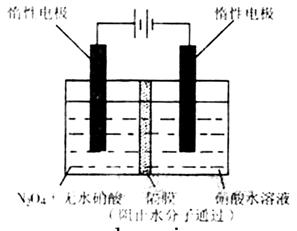
(3)如图所示装置可用于制备N2O5,则N2O5在电解池的 区生成,其电极反应式为 。
查看答案和解析>>
科目: 来源: 题型:
今有A、B、C、D、E五种短周期元素,它们的核电荷按 C、A、D、E的顺序增大。C、D都能分别与A按原子个数比1:1或2:1形成化合物。CB可与EA2反应生成C2A与气态物质EB4。
⑴写出五种元素名称A B ,C ,D , E 。
⑵画出E的原子结构简图 ,写出电子式D2A2 , EB4 。
⑶比较EA2与EB4的熔点高低 < 。
⑷写出D单质与CuSO4溶液反应的离子方程 。
查看答案和解析>>
科目: 来源: 题型:
钛(Ti)因为具有神奇的性能越来越引起人们的关注,常温下钛不和非金属、强酸反应,红热时,却可与常见的非金属单质反应,钛是航空、军事、电力等方面的必需原料。地壳中含钛铁矿石之一是金红石(TiO2),目前大规模生产钛的方法是:
第一步:金红石、炭粉混合,在高温条件下,通入Cl2制得TiCl4和一种可燃气体,该反应的化学方程式为__________________________________________________________,该反应的还原剂是__________。
第二步:在氩气的气氛中,用过量的镁在加热条件下与TiCl4反应制得金属钛。
(1)写出此反应的化学方程式____________________________________________________。
(2)简述从上述所得产物中获得金属钛的步骤。
__________________________________________________________________
查看答案和解析>>
科目: 来源: 题型:
我国在春秋战国时期,就懂得将白铁淬火得到如锋利宝剑一类的铸钢,白铁淬火的主要作用是( )
A.除硫、磷杂质 B.适当降低含碳量
C.掺进合金元素 D.改善表面结构
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com