
科目: 来源:2011-2012年辽宁省高一上学期10月考化学试卷 题型:计算题
取1.43g Na2CO3·10H2O溶于水配成100ml溶液,求:
(1)Na2CO3物质的量浓度
(2)Na+ 物质的量浓度
(3)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.004mol/L,求加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略不计)
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
下列说法中不正确的是( )
①将BaSO4放入水中不能导电,所以BaSO4是非电解质
②氨溶于水得到的溶液氨水能导电,所以氨水是电解质 ③固态共价化合物不导电,熔融态的共价化合物可以导电 ④固态的离子化合物不导电,熔融态的离子化合物也不导电
⑤强电解质溶液的导电能力一定比弱电解质溶液的导电能力强
A.①④ B.①④⑤
C.①②③④ D.①②③④⑤
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
下列叙述中一定能判断某化学平衡发生移动的是( )
A.混合物中各组分的浓度改变 B.正、逆反应速率改变
C.混合物中各组分的含量改变 D.混合体系的压强发生改变
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
下列说法正确的是( )
A.pH<7的溶液一定是酸性溶液
B.改变外界条件使溶液中c(H+)增大,则其pH增大
C.室温下,每1×107个水分子中只有一个水分子发生电离
D.常温时,pH=5的溶液和pH=3的溶液相比,前者c(OH-)是后者的100倍
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
下列事实,不能用勒夏特列原理解释的是
A.氯水中有下列平衡:Cl2+H2O HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅
HCl + HClO,当加入AgNO3溶液后,溶液颜色变浅
B.对2HI(g)  H2(g)+I2(g),平衡体系增大压强可使颜色变深
H2(g)+I2(g),平衡体系增大压强可使颜色变深
C.反应CO+NO2  CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
CO2+NO(正反应为放热反应),升高温度可使平衡向逆反应方向移动
D.合成NH3反应,为提高NH3的产率,理论上应采取低温度的措施(N2+3H2 2NH3;DH<0)
2NH3;DH<0)
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
下列说法正确的是( )
A.ΔH<0、ΔS>0的反应在温度低时不能自发进行
B.NH4HCO3(s)=NH3(g)+H2O(g)+CO2(g) ΔH=+185.57 kJ/mol能自发进行,原因是体系有自发地向混乱度增加的方向转变的倾向
C.因为焓变和熵变都与反应的自发性有关,因此焓变或熵变均可以单独作为反应自发性的判据
D.在其他外界条件不变的情况下,使用催化剂,可以改变化学反应进行的方向
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
下列各组变化中,ΔH或Q前者小于后者的一组是
①CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1; CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH2
②在稀溶液中:含0.5 mol H2SO4硫酸与含1 mol NaOH的溶液混合:H+(aq)+OH-(aq)=H2OΔH1
NaOH(aq)+CH3COOH(aq) =CH3COONa(aq)+H2O(l) ΔH2
③t ℃时,在一定条件下,将1 mol SO2和1 mol O2分别置于恒容和恒压的两个密闭容器中,达到平衡状态时放出的热量分别为Q1、Q2
④CaCO3 (s)=CaO(s)+CO2(g) ΔH1 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH2
A.①②③ B.②③ C.①② D.①③④
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
下列实验事实不能证明醋酸是弱酸的是( )
A.常温下,含有石蕊的醋酸溶液加热颜色变深
B.常温下,测得0.1 mol/L醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1 000倍,测得pH<4
D.常温下,将物质的量浓度相同的醋酸溶液与氢氧化钠溶液等体积混合后恰好中和
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
等物质的量的X(g)与Y(g)在密闭容器中进行可逆反应:X(g)+Y(g)= 2Z(g)+W(s)ΔH<0,下列叙述正确的是( )
A.达到平衡后,降低温度,正向反应速率减小的倍数大于逆向反应速率减小的倍数
B.达到平衡后,升高温度或增大压强都有利于该反应平衡向逆反应方向移动
C.达到平衡时,反应速率v正(X)=2v逆(Z)
D.平衡常数K值越大,X的转化率越大
查看答案和解析>>
科目: 来源:2011-2012年黑龙江双鸭山一中高二上学期期中考试化学试卷 题型:选择题
已知下列反应的反应热为:
(1)CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) △H1=-870.3KJ/mol
(2)C(s)+O2(g)=CO2(g)
△H2=-393.5KJ/mol (3) H2(g)+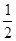 O2(g)=H2O(l) △H3=-285.8KJ/mol
O2(g)=H2O(l) △H3=-285.8KJ/mol
试计算下列反应的焓变:2C(s)+2H2(g)+O2(g)=CH3COOH(l) △H ( )
A.-488.3 KJ/mol B. +488.3KJ/mol C. -245.7KJ/mol D. +245.7KJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com