
科目: 来源: 题型:
已知亚硝酸铵很不稳定,在溶液中加热能分解生成氮气和水。有人设计下图所示装置(A中盛有饱和NaNO2、NH4Cl的混合溶液)来进行有关实验。

实验步骤如下:
①检查装置的气密性;
②用酒精灯加热NH4Cl和NaNO2的饱和溶液,待有气体生成,停止加热,但仍有大量气体产生;
③再用酒精灯加热铁铈合金至一定温度;
④从胶头滴管中不断滴入一定浓度的盐酸,不久发现石蕊试液变蓝。
请回答下列问题:
(1)本实验的主要目的是__________________。
(2)先加热NH4Cl和NaNO2饱和溶液的目的是_______________________,停止加热后,仍有大量气体生成的原因是___________________________。
(3)B中应装_______________________,其作用是_____________________________。
(4)C中铁铈合金的作用是_________________,要先加热至一定温度的原因是_____________。
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
科目: 来源: 题型:
有关物质间的转化如下图所示,其中:A的浓溶液与单质B在加热时能发生反应(Ⅰ),A的稀溶液与足量的B发生反应(Ⅱ)。据此回答: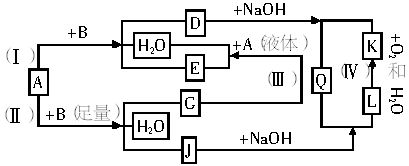
(1)反应(Ⅳ)产生的现象为__________________。
(2)写出反应(Ⅱ)的离子方程式:_____________。
(3)根据图示信息判断,A的浓溶液和单质B加热时能否产生G,说明理由:__________________。
查看答案和解析>>
科目: 来源: 题型:
蛇纹石矿可以看作由MgO、Fe2O3、Al2O3、SiO2组成的。由蛇纹石制取碱式碳酸镁的实验步骤如下:
(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是________。
(2)进行Ⅰ操作时,控制溶液的pH=7~8(有关氢氧化物沉淀的pH见下表),Ca(OH)2不能过量,若Ca(OH)2过量可能会导致____________溶解,___________沉淀。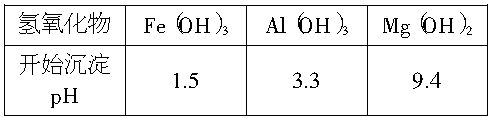
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入_________ (填物质的化学式),然后_____________________ (依次填写实验操作名称)。
(4)物质循环使用能节约资源。上述实验中,可以循环使用的物质是____________ (填写物质的化学式)。
(5)为确定产品aMgCO3?bMg(OH)2?cH2O中a、b、c的值,请完成下列实验步骤(可用试剂:浓硫酸、碱石灰):
①样品称量;②高温分解;③_______;④________;⑤MgO称量。
(6)18.2g产品完全分解后产生6.6gCO2和8.0g MgO,由此可知,产品的化学式中a=______、b=_______、c=______。
查看答案和解析>>
科目: 来源: 题型:
某化学研究小组通过查阅资料得知,实验室可通过多种途径得到氮气,常用的三种方法是:
①将氨气通过灼热的氧化铜粉末,得到纯净的氮气和铜;
②将空气通过灼热的铜,得到较纯净的氮气和氧化铜粉末;
③将亚硝酸钠(NaNO2)和氯化铵的混合溶液加热,逸出氮气。
进行上述实验时可从下列实验仪器(铁架台、铁夹、铁圈、石棉网、酒精灯等未列出)中选择: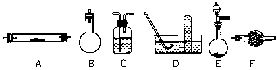
请回答下列问题:
(1)写出方法③中发生反应的化学方程式:_________________________。
(2)若按方法②制氮气,应先向_______(填编号)装置中加入_______(填物质的化学式),将空气送入反应器,反应中可观察到的主要现象为_________________________________。
(3)制取氮气的三种方法中,方法①和方法②越来越受人们的关注,经常被联合使用。这两种方法与方法③相比,其优越性在于①____________________;②_______________________________。(至少写两点
查看答案和解析>>
科目: 来源: 题型:
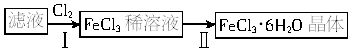 某校化学小组的同学利用所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3?6H2O晶体。(图中夹持及尾气处理装置均略去)
某校化学小组的同学利用所列装置进行“铁与水反应”的实验,并利用产物进一步制取FeCl3?6H2O晶体。(图中夹持及尾气处理装置均略去)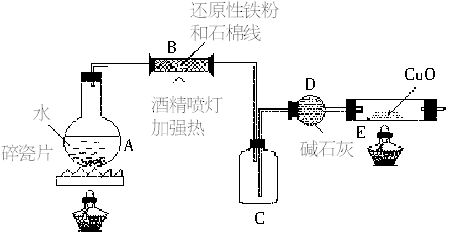
查看答案和解析>>
科目: 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com