
科目: 来源: 题型:选择题
| A. | 氯化钠:食盐;天然气:沼气、坑气 | |
| B. | 氢氧化钠:火碱、烧碱、苛性钠 | |
| C. | 氢氧化钙:熟石灰、碱石灰 | |
| D. | 碳酸钠:纯碱、苏打;碳酸氢钠:小苏打 |
查看答案和解析>>
科目: 来源: 题型:解答题
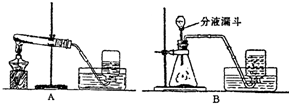
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氧化汞加热→ 汞+氧气 | B. | 乙炔+氧气点燃→ 二氧化碳+水 | ||
| C. | 铜+氧气加热→ 氧化铜 | D. | 氧化铜+氢气 加热→ 铜+水 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |

查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
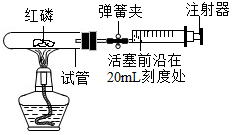 为测定空气中氧气的含量,小华同学打算设计如下方案:选用大试管作反应容器,将过量的红磷放入试管,用橡皮塞塞紧试管口,通过导管与润滑性很好的针筒注射器组成如下图的实验装置.
为测定空气中氧气的含量,小华同学打算设计如下方案:选用大试管作反应容器,将过量的红磷放入试管,用橡皮塞塞紧试管口,通过导管与润滑性很好的针筒注射器组成如下图的实验装置.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com