
科目: 来源: 题型:
【题目】“宏观现象—微观结构—符号表征”是学习化学的思维方法。下图表示在催化剂作用下,将汽车尾气中的一氧化碳、二氧化氮转化为无害气体的反应原理。
![]()
(1)用化学符号表示5个二氧化氮分子______。
(2)上图所示反应物和生成物中属于单质的是_______(填化学式)。
(3)上图所示的化学反应方程式为________。
查看答案和解析>>
科目: 来源: 题型:
【题目】(1)用化学用语填空:
①碳元素______;②3个钾原子______;③4个氮分子_______; ④钠离子_____;
⑤氢气_______; ⑥标出氧化钙中钙元素的化合价________.
(2)化学符号中数字的意义。
①3Cu2+中表示离子个数的数字是_______;②SO2中的“2”表示________________.
(3)“水循环”和“碳循环”是自然界中存在的两大重要循环。
①从微观的角度看:水分子是由_________构成。
②从宏观的角度看:二氧化碳是由_________组成。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学反应的微观示意图如下,根据该图得出的结论,正确的是
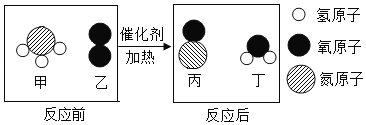
A. 四种物质中只有丙属于氧化物
B. 该反应为化合反应
C. 该化学反应前后原子种类、个数不变
D. 若有17 g 物质甲参加反应,生成物丁的质量为18 g
查看答案和解析>>
科目: 来源: 题型:
【题目】铁、铜的氧化物能与氢气、一氧化碳和氨气(NH3)等具有还原性的气体反应生成金属单质,某研究性学习小组设计实验进行系列探究。
(-)探究氨气(NH3)与氧化铜的反应
资料一1
①实验室常用浓氨水和生石灰混合的方法制取氨气:CaO+NH3·H2O=Ca(OH)2+NH3↑。
②碱石灰和浓硫酸是常用的干燥剂,浓硫酸能与氨气反应
③Cu20是一种红色固体,能与稀硫酸反应:Cu2O+H2SO4=Cu+CuSO4+H2O。
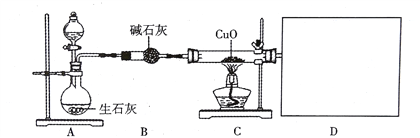
(1)小组同学按图设计组装好仪器,装入药品前应进行的实验操作是_______
(2)A中锥形瓶内发生的反应为___________反应(填“放热”或“吸热”)。
(3)C中玻璃管内氨气与氧化铜在加热条件下完全反应生成铜、水和一种气体单质X,反应的化学方程式为___,反应过程中氨气也可能将氧化铜还原为Cu2O。反应一段时间后,C中固体全部变为红色,取反应后固体少许于试管中,加入足量的稀硫酸,观察到溶液呈_____说明红色固体中含有Cu2O,该红色固体的成分是_____(写出所有可能)。
(4)气体X的密度和空气接近,难溶于水,上图D处欲用下图装置①②③收集较纯净的气体X
并测其体积,装置的连接顺序是_________.

(二)探究一氧化碳与铁的氧化物反应
【资料二】
①Fe2O3·xH2O在温度为110℃时分解为Fe2O3和H2O,FeCO3在282℃时分解为FeO和CO2。
②温度高于500℃时铁的氧化物才能被CO还原。
③用CO还原Fe2O3炼铁的过程大致分为三个阶段
阶段1:3Fe2O3+CO![]() 2Fe3O4+CO2
2Fe3O4+CO2
阶段2:Fe3O4+CO![]() 3Fe++CO2
3Fe++CO2
阶段3:FeO+CO![]() Fe+CO2
Fe+CO2
(5)已知铁锈的成分为Fe2O3·xH2O和FeCO3由此可知:铁生锈过程中,空气中的氧气、水和____都参与了反应.
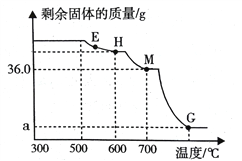
(6)小组同学将铁锈在300℃热分解的产物继续分阶段升温,通人CO还原铁的氧化物。剩余固体质量随温度变化的曲线如下图所示。E点固体的成分是_____.计算图中G点对应的a的值,写出计算过程_____。
(7)金属矿物资源储量有限且不可再生,为防止铁制品生锈,可以采取____________的措施。
查看答案和解析>>
科目: 来源: 题型:
【题目】V2O3广泛应用于治金、化工等行业,实验室制取V2O3的流程如下:
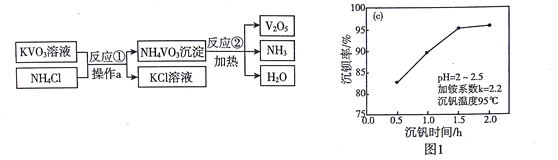
(1)KVO3中钒元素的化合价是_________
(2)操作a的名称是____________。图1表示反应①的沉钒率随时间变化的情况,为使生成沉淀的效率较高,反应①适合的时间是__________小时。
(3)反应②的化学方程式为____________,该反应的基本类型是________
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列实验装置图,回答有关问题。
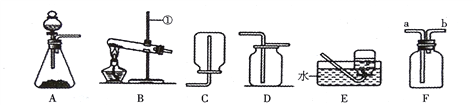
(1)图中标有①的仪器名称是_______________。
(2)实验室用氯酸钾和二氧化锰制取氧气,反应的化学方程式为____,应选择的发生装置是_____,应选择的收集装置是_____。将点燃的硫粉伸入盛满氧气的集气瓶中观察到火焰的颜色为_____。
(3)实验室制取二氧化碳,应选择的发生装置是________,反应的化学方程式为___________若用F装置收集二氧化碳,检验二氧化碳收集满的方法是______________。
(4)某实验小组的同学设计以下装置,准确称量1.0g铜锌合金,加入足量的盐酸,充分反应后通过测定生成氢气的体积,计算铜锌合金中锌的质量分数。
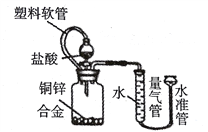
①实验前将块状合金加工成碎屑,目的是_________,装置中塑料软管的作用是______
②实验时反应的化学方程式为__________
③实验测得氢气的体积是0.224L,在该实验条件下氢气的密度为0.089g·L-1,该铜锌合金中锌的质量分数是____
查看答案和解析>>
科目: 来源: 题型:
【题目】向K2CO3溶液中滴入Ba(OH)2溶液至恰好完全反应。
(1)可以观察到的实验现象是_______________________。
(2)下图表示该反应前后溶液中存在的主要离子,写出下列图形代表的离子。(填离子符号)![]() ___________;
___________;![]() ____________。
____________。
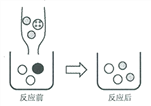
(3)下列物质能与K2CO3溶液反应产生类似上述实验现象的是__________。
A.Ca(OH)2 B.HCl C.BaCl2 D.(NH4)2SO4
查看答案和解析>>
科目: 来源: 题型:
【题目】为测定某硫酸溶液的溶质质量分数,某同学取10g样品,逐滴加入溶质质量分数为5%的NaOH溶液,边加边搅拌,溶液pH的变化如图所示.请回答下列问题:
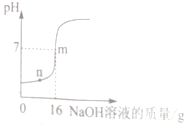
﹙1﹚n点所对应的溶液中所含阴离子符号;
﹙2﹚图中m点所消耗氢氧化钠溶液中溶质的质量;
﹙3﹚计算该硫酸的溶质质量分数(请写出计算过程)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com