
科目: 来源: 题型:
【题目】全世界每年因生锈而损失的钢铁约占世界钢铁年产量的1/4.某同学想探究铁生锈的条件,他将干净的铁钉分别同时放入A、B、C三支试管中进行探究。
(设计实验)请你帮助该同学完成下列实验设计的内容:
编号 | 操作方法 | 实验目的 |
A | 在干燥的试管中放入铁钉,并放入少量氯 化钙做干燥剂 | 探究铁在_____铁的生锈情况 |
B | 放入铁钉,注入蒸馏水浸没铁钉,并用植 物油液封 | 探究铁在_____铁的生锈情况 |
C | _____ | 探究铁在有氧气和水同时存在时的生锈情况 |
(实验结论)一周后,编号为_____的试管中的铁钉最易生锈。
(扩展延伸)苹果切开不久,果肉上就会产生一层咖啡色的物质,也好象是生了“锈”一样。
(1)切开的苹果“生锈”与什么因素有关?
猜想①:可能与空气没有关系,只是果肉内的物质自身相互反应而“生锈”。
猜想②:可能是果肉中的物质与空气中的氧气作用而“生锈”。
猜想③:可能是果肉中的物质与空气中的氮气作用而“生锈”。
猜想④:可能是果肉中的物质与空气中的二氧化碳作用而“生锈”。
(2)查阅资料:已知苹果“生锈”是果肉里的物质(酚和酶)与空气中的一种物质发生反应,生成咖啡色的物质。且不切开的苹果没有此现象,所以苹果“生锈”与猜想①无关。
(3)在②﹣④猜想中,你认为猜想_____最不合理,理由是_____。
(实践应用)(1)用相同材料制作,经过相同防锈处理的铁栏杆,安装在沿海比安装在内陆更易生锈,其主要原因是_____。
(2)有时候铁制品腐蚀不一定是因为锈蚀而引起的,如用铁桶盛装农药波尔多液(含硫酸铜溶液)就很容易被腐蚀,写出该反应的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】近年各大体坛赛事报道频繁出现一个名词“嗅盐”。某校兴趣小组在老师的指导下,对“嗅盐”展开了系列探究:
(查阅资料)①嗅盐,是一种由碳酸铵和香料配制而成的药品,给人闻后有刺激作用;
②嗅闻原理是碳酸铵晶体产生的氨气对人体有刺激作用,过量嗅闻不利健康;
③碳酸铵[(NH4)2CO3]晶体受热易分解,产生 NH3、H2O、CO2。
(定性初探)验证“嗅盐”的化学性质
(1)甲同学进行了NH4+的验证实验:取适量嗅盐于试管中,加入氢氧化钠溶液共热,在试管口放一张_____,观察到了预期的实验现象。请写出氢氧化钠溶液与碳酸铵反应的化学方程式_____。
(2)乙同学进行了 CO32﹣的验证实验:取适量嗅盐于试管中,再加入稀硫酸,并将生成的气体通入_____,预期的实验现象是_____,实验后观察到了预期的现象。
(定量再探)测定“嗅盐”中碳酸铵(NH4)2CO3的质量分数
方案Ⅰ:取样品 6.0 克,用图 1 装置进行实验,测量C装置在反应前后增加的质量即为产生NH4+的质量:
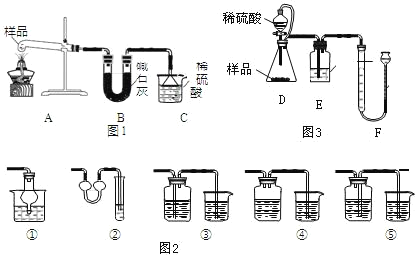
(3)装置B的作用_____,装置C中普通漏斗的作用是_____,图2装置中不能与其起到相似作用的是_____。
(4)小组同学经讨论后,均认为用该套装置测量会导致碳酸铵的质量分数偏小,原因是_____。
方案Ⅱ:取样品6.0克,用图3装置进行实验,利用F装置测量反应生成气体的体积。
(5)请写出装置D中发生反应的化学方程式_____,装置 D 中橡胶管除平衡压强,便于液体顺利滴下外,还有_____的作用。
(6)该方案实验结束后,会有气体残留,不能完全进入量气管中,_____(填“需要”或“不需要”)通入N2将其 中残留的气体排入量气管中,阐述你的理由_____。
(7)实验测得量气管中产生气体的体积为 558mL,该方案所测嗅盐中碳酸铵的质量分数为_____。(已知实验条件下,CO2的密度约为 1.97g/L)。(请写出过程,计算结果精确到 1%)
(8)若其他操作均正确,下列因素会导致所测嗅盐中碳酸铵的质量分数偏大的是_____ (填字母)
a反应前量气管液面在 0 刻度处以下
b实验结束后,调节两端液面相平读数
c反应结束后未等装置冷却到室温,就开始读数
d反应前正确读取量气管中液体体积,反应后仰视读数
查看答案和解析>>
科目: 来源: 题型:
【题目】工业上以半水煤气(主要成分是 N2、H2、CO、CO2和H2O)、食盐等为原料制取纯 碱的流程如图 1:
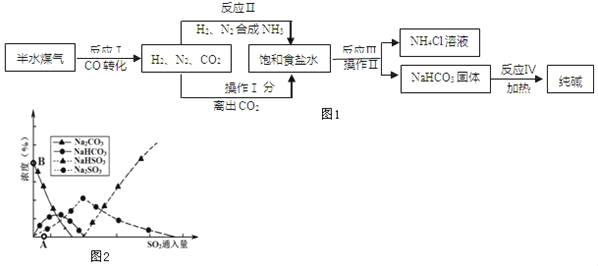
(1)反应Ⅰ是在使用铜催化剂和加热条件下,半水煤气主要成分间发生反应,实现了 CO 转化,化学方程式是_____。
(2)将反应Ⅱ生成的 NH3和操作Ⅰ分离出的CO2通入饱和食盐水中即可得 NaHCO3固体,下列两种操作,你觉得更为合理的是_____。
a先通 NH3再通入CO2 b先通 CO2再通入 NH3
(3)操作Ⅱ的名称是_____,实验室进行该项操作时,需要用到的玻璃仪器有:普通漏斗、烧杯和_____,该仪器在此操作中的作用是_____。
(4)反应Ⅲ的成功实现说明该实验条件下,NaHCO3的溶解度_____(填“>”“<”或“=”)NH4Cl 的溶解度。
(5)纯碱用途广泛。工业上可用废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2,制备无水Na2SO3,达到减少污染、节约资源的目的。反应过 程中溶液组成变化如图 2 所示。
①吸收初期(图2中A点以前)反应的化学方程式为_____。
②不断通入 SO2,最终产物是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】食盐是人类生存的必需品,获取食盐的途径有多种。
(1)开采岩盐。地下盐层含氯化钠、硫酸钠等物质,构成硫酸钠的阴离子是_____ (填符号)。 除去氯化钠溶液中的硫酸钠应选用的试剂是_____(填化学式)溶液。
(2)熬制井盐。用井中产生的天然气作为燃料熬制井盐。CH4燃烧的化学方程式是_____。
(3)海水晒盐。某地海水中主要物质的含量见表。 该海水中氯化钠的质量分数为_____,配制某氯化钠溶液需 85mL 水,应选用量筒的规格为_____mL。
物质 | 每 100g 海水所含质量(g) |
水 | 96.5 |
氯化钠 | 2.7 |
硫酸钠 | 0.2 |
…… | …… |
(4)松花蛋的制作过程也需用氯化钠,还有生石灰、纯碱等,制作料泥时将上述原料加入水中,混合均匀即可。
从物质分类的角度看,该料泥是_____物,料泥中的“纯碱”是_____(填物质的名称) 的俗称;原料中可以做干燥剂的物质是_____(填化学式),它与水发生反应的化学方程式为_____,该反应过程_____热量(填“放出”或“吸收”)。
查看答案和解析>>
科目: 来源: 题型:
【题目】向一定量的硝酸铜、硝酸银的混合溶液中加入5.6g铁粉,充分反应后过滤、洗涤、干燥,称得固体14g。向固体中加入稀盐酸,无气泡产生。则下列分析正确的是( )
A. 滤液中一定不含有硝酸银
B. 滤液中一定含有硝酸铜
C. 滤出的固体中一定没有铁
D. 滤出的固体中含有铜6.4g
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙试管中各盛有10.0g水,向其中一支试管中加入3.0g Na2CO3粉末,另一支试管中加入3.0gNaCl粉末,按图1、2进行实验。下列说法正确的是
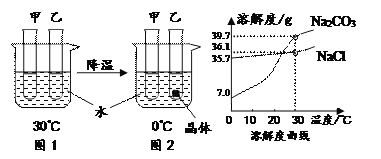
A. 甲中加入的粉末是Na2CO3
B. 0℃时,甲中溶液一定不饱和,乙中溶液一定饱和
C. Na2CO3中含有少量NaCl,可用冷却热饱和溶液的方法提纯Na2CO3
D. 30℃时,若使图1中甲、乙试管内的溶液恰好变为相应饱和溶液,甲中加入对应的溶质质量大于乙中加入对应的溶质质量
查看答案和解析>>
科目: 来源: 题型:
【题目】某有机物64g在氧气中充分燃烧,经测定生成44g二氧化碳、28g一氧化碳和72g水,则该有机物的化学式可能是下列物质中的( )
A. CH3OHB. C2H2C. C2H5OHD. CH4
查看答案和解析>>
科目: 来源: 题型:
【题目】达菲是治疗甲型HIN1流感的有效药品之一,其主要制作原料是八角茴香中的莽草酸(C7H10O5).下列关于莽草酸的说法中,正确的是( )
A. 莽草酸的含碳质量分数约为48.28%
B. 莽草酸由7个碳原子、10个氢原子、5个氧原子构成
C. 莽草酸的相对分子质量为174克
D. 莽草酸中碳氢氧三种元素的质量比为7:10:5
查看答案和解析>>
科目: 来源: 题型:
【题目】某兴趣小组用下图所示流程制取氧气,并回收提纯氯化钾和二氧化锰。
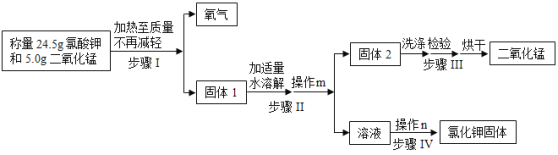
(1)在溶解固体1的过程中需要控制水的用量,原因有__________(填标号)。
A提高实验效率 B保证固体1全部溶解 C节约能源
(2)若整个流程中物质的量无损耗,则最后所得二氧化锰的质量为________g。
(3)根据化学方程式计算,理论上可回收得到氯化钾的质量是______。
(4)实验结束后,称得回收到的氯化钾的质量比理论值小,可能的原因____________________(写一点)。
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究性学习小组对中和反应进行探究,请你参与实验。
(探究活动1)证明酸和碱发生了反应。
稀盐酸和NaOH溶液混合没有明显现象,小丽同学首先向盛有适量NaOH溶液的试管中滴加了2~3滴酚酞试液,接着向试管中逐滴加入稀盐酸,当观察到_________________________的现象时,证明了盐酸和NaOH溶液发生化学反应。反应的化学方程式是____________________________。
(探究活动2):证明酸碱反应有水生成
(设计实验)小明同学取变色硅胶、无水醋酸和氢氧化钠固体进行下图所示的三个实验。
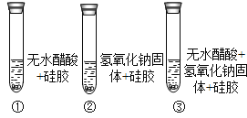
(小资料)a变色硅胶吸水后由蓝色变为红色; b醋酸是一种酸,常温下为无色液体。
(1)实验①、②的实验目的是___________________________;
(2)加入试剂后,要迅速塞紧橡胶塞的原因是__________________________________;
(3)能证明酸和碱反应有水生成的现象是_____________________________________。
(探究活动3)探究酸和碱反应过程中溶液pH、温度的变化
研究性小组的同学在老师指导下,取一定量的稀盐酸,逐滴匀速滴加NaOH溶液,用电子传感器实时获得溶液的pH、温度曲线如下图。
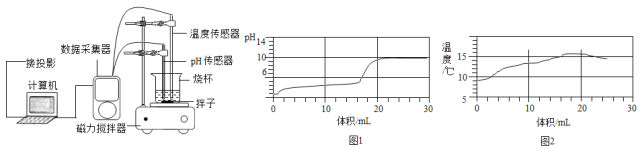
(1)由图1分析,酸和碱发生反应的依据是_________________,当滴入NaOH溶液体积约______mL时,溶液的pH为7。
(2)由图2分析,酸和碱的反应是__________反应(填“吸热”或“放热”)。
(探究活动4)酸碱中和反应的微观实质
研究性小组的同学查阅资料,以NaOH和HCl、KOH和HCl为例,通过右图说明酸碱反应的微观过程。请你分析下图,酸碱中和反应的实质是____。
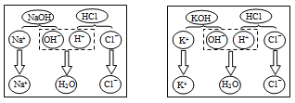
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com