
科目: 来源:江西省模拟题 题型:单选题
 Ca2+(aq)+2OH-(aq),下列说法正确的是
Ca2+(aq)+2OH-(aq),下列说法正确的是查看答案和解析>>
科目: 来源:模拟题 题型:单选题
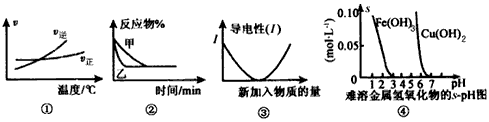
 2AB3(g)的△H>0
2AB3(g)的△H>0 3C(g)+D(s)的影响,乙的压强大
3C(g)+D(s)的影响,乙的压强大查看答案和解析>>
科目: 来源:湖南省模拟题 题型:填空题
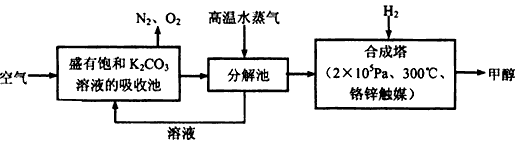
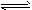 HCO3-+H+的平衡常数 K=____。(已知:10-5.6=2.5×10-6)
HCO3-+H+的平衡常数 K=____。(已知:10-5.6=2.5×10-6) 查看答案和解析>>
科目: 来源:专项题 题型:单选题
 Ca2+(aq) +2OH-(aq),加入少量下列固体物质,可使Ca(OH)2减少的是
Ca2+(aq) +2OH-(aq),加入少量下列固体物质,可使Ca(OH)2减少的是 查看答案和解析>>
科目: 来源:专项题 题型:单选题
查看答案和解析>>
科目: 来源:专项题 题型:单选题
查看答案和解析>>
科目: 来源:专项题 题型:单选题
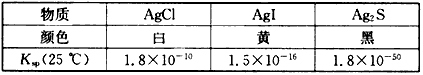
查看答案和解析>>
科目: 来源:专项题 题型:单选题
查看答案和解析>>
科目: 来源:同步题 题型:单选题
查看答案和解析>>
科目: 来源:专项题 题型:单选题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com