
科目: 来源: 题型:
研究发现,空气中少量的NO2能参与硫酸型酸雨的形成,反应过程如下:
①SO2 + NO2 = SO3 + NO ②SO3 + H2O = H2SO4 ③2NO + O2 = 2NO2
NO2在上述过程中的作用,与下列物质在相应变化中的作用相似的为
A.铂铑合金:处理汽车发动机尾气
B.浓硫酸:潮湿的二氧化硫通过盛有浓H2SO4的洗气瓶
C.生石灰:用于工业生产中二氧化硫废气的处理
D.饱和硫氢化钠溶液:将混有HCl的H2S通过盛有饱和硫氢化钠溶液的洗气瓶
查看答案和解析>>
科目: 来源: 题型:
实验室一瓶久置的白色粉末,元素分析证明它由钾、硫、氧三种元素组成,钾和硫的质量比为39∶16,下列结论正确的是
A.根据元素分析结果推测该粉末为纯净物
B.将粉末溶于水,加入氯化钡溶液,观察到有白色沉淀生成,证明原粉末是硫酸钾
C.将粉末加入盐酸中,产生气泡,证明原粉末是亚硫酸钾
D.将粉末溶于水,加入氯化钡溶液和盐酸,观察到有白色沉淀和气泡生成,证明原粉末是硫酸钾和亚硫酸钾的混合物
查看答案和解析>>
科目: 来源: 题型:
下列叙述不正确的是
A.《维也纳公约》和《蒙特利尔议定书》决定减少并逐步停止氟氯代烷的生产和使用,以保护臭氧层
B.空气中硫的氧化物和氮的氧化物随雨水降下,就会形成酸雨w.w.w.k.s.5.u.c.o.m
C.光导纤维的主要成分为晶体硅,是一种高质量的导光材料
D.汽车尾气中排放的氮氧化合物是造成光化学烟雾的主要因素
查看答案和解析>>
科目: 来源: 题型:
(8分)NO很容易与许多分子迅速发生反应,科学家发现在生命体中会不断地产生NO,用于在细胞和细胞间传递信息;NO还参与心血管系统、免疫系统以及中枢和外围神经系统的调控。
![]() (1)写出实验室用金属铜和稀硝酸制取NO的离子方程式: 。
(1)写出实验室用金属铜和稀硝酸制取NO的离子方程式: 。
![]() (2)甲同学利用如图Ⅰ所示装置进行铜和稀硝酸反应实验,实际上看到的气体却是红棕色的原因是(填化学方程式): 。
(2)甲同学利用如图Ⅰ所示装置进行铜和稀硝酸反应实验,实际上看到的气体却是红棕色的原因是(填化学方程式): 。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
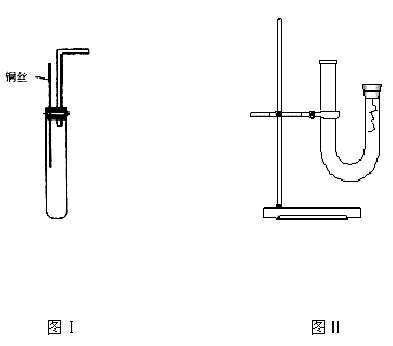
(3)丙同学采用如图II所示的装置进行实验,证明了铜与稀硝酸反应生成NO。该学的步骤如下:①从U形管左端加入稀硝酸,直至充满U形管右端;②用附有铜丝的胶塞塞住U形管右端(胶塞用锡箔纸包住),观察现象;③等反应停止后用注射器注入适量空气,观察实验现象。该同学确认铜与稀硝酸反应生成NO的实验现象是 。
(4)以下收集NO气体的各种装置中,合理的是 (填选项代号)。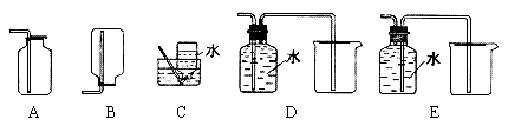
查看答案和解析>>
科目: 来源: 题型:
(9分)(Ⅰ)开发新型替代燃料成为各国关注的重要科研项目,中国现已成为世界第三大利用植物秸秆(主要成分纤维素)生产燃料乙醇的国家。已知在25℃条件下,2.3g乙醇完全燃烧生成CO2和液态H2O时放出68.34kJ的热量,写出乙醇燃烧的热化学方程式: 。

(Ⅱ)乙醇的催化氧化反应在有机合成工业有着广泛的用途。某同学用如下图所示的方法进行乙醇的催化氧化实验:向试管中加入3-4mL无水乙醇,浸入50℃左右的热水中,将铜丝烧热,迅速插入乙醇中,反复多次
(1)在上述实验过程中,铜丝绕成螺旋状的作用是 。
(2)铜丝的颜色先后发生的变化是 ;请写出相应的两个化学方程式 、 。
查看答案和解析>>
科目: 来源: 题型:
有机物A由碳、氢、氧三种元素组成。现取6.0g A与8.96L氧气(标准状况)在密闭容器中燃烧,燃烧后生成二氧化碳、一氧化碳和水蒸气(反应物和氧气都没有剩余)。将反应生成的气体依次通过浓硫酸和碱石灰,浓硫酸增重7.2g,碱石灰增重8.8g。回答下列问题:
![]() (1)求燃烧产物中一氧化碳的质量。
(1)求燃烧产物中一氧化碳的质量。
![]() (2)求该有机物中所含碳原子、氢原子、氧原子的物质的量之比。
(2)求该有机物中所含碳原子、氢原子、氧原子的物质的量之比。
![]() (3)请问:根据题给数据能否确定该有机物的分子式?若认为不能确定该有机物的分子式,请补充需要的数据: ;若认为能确定该有机物的分子式,请写出该有机物的分子式,并说明理由: 。
(3)请问:根据题给数据能否确定该有机物的分子式?若认为不能确定该有机物的分子式,请补充需要的数据: ;若认为能确定该有机物的分子式,请写出该有机物的分子式,并说明理由: 。
查看答案和解析>>
科目: 来源: 题型:
(12分)已知A、B、C、D、E均为短周期元素,它们的原子序数依次递增。 A单质是自然界中密度最小的气体,C元素原子的最外层电子数是次外层的3倍,D原子的最内层电子数和最外层电子数之和等于其次外层电子数,E单质性质活泼;B和C可形成多种气态化合物。A、B、C三种元素可以形成离子化合物甲,甲是一种常见的化肥,甲可以和氢氧化钠反应放出无色刺激性气味气体乙,乙能使湿润的红色石蕊试纸变蓝。请回答下列问题:
(1)写出C元素在周期表中的位置 。
(2)写出B单质分子的电子式 ;乙分子的结构式 。
(3)化肥甲的俗称是 ;甲晶体中含有的化学键类型有 。
(4)元素D与元素E相比,非金属性较强的是 (用元素符号表示) ,例举能证明这一结论的两个事实 、 。
(5)往甲的浓溶液中加入NaOH的浓溶液并加热,反应的离子方程式是查看答案和解析>>
科目: 来源: 题型:
(10分)分别按下图甲、乙所示装置进行实验,图中两个烧杯里的溶液为同浓度的稀硫酸,乙中G为电流计。请回答下列问题:
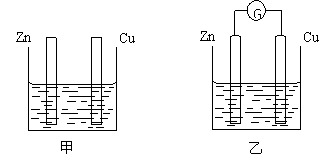
(1)以下叙述中,正确的是
A.甲中锌片是负极,乙中铜片是正极
B.两烧杯中铜片表面均有气泡产生
C.两烧杯中溶液的pH均增大
D.产生气泡的速度甲中比乙中慢
E.乙的外电路中电流方向Zn→Cu
(2)变化过程中能量转化的形式主要是:甲为 ;乙为 。
(3)在乙实验中,某同学发现不仅在铜片上有气泡产生,而且在锌片上也产生了气体,分析原因可能是 。
(4)在乙实验中,如果把硫酸换成硫酸铜溶液,请写出铜电极的电极反应方程式: 。
(5)如果要使甲装置中的铜片溶解而锌片不溶解,请在下图中完成实验装置图。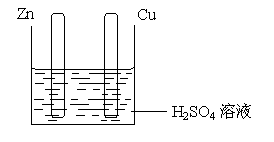
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com