

科目: 来源:2011-2012学年湖北省襄阳市高三3月调研考试理科综合试卷(化学部分) 题型:填空题
(14分)短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和无色、有臭鸡蛋气味的气体E,D既能溶于强酸,也能溶于强碱。E分子含18个电子,在足量空气中燃烧生成G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
(1)组成单质A的元素位于周期表中第 周期第 族;
(2)化合物H的电子式为 ;
(3)B与氢氧化钠溶液反应的离子方程式为: ;
(4)G与氯酸钠溶液反应可生成消毒杀菌剂二氧化氯。写出对应的离子方程式:
(5)溶液F在空气中长期放置生成H的化学反应方程式为: ;
(6)写出F溶液中各离子浓度由大到小的关系为: ;
查看答案和解析>>
科目: 来源:2011-2012学年湖北省襄阳市高三3月调研考试理科综合试卷(化学部分) 题型:填空题
(14分)
(1)反应Fe(s)+CO2(g) FeO(s)+CO(g)
△H1,平衡常数为K1
FeO(s)+CO(g)
△H1,平衡常数为K1
反应Fe(s)+H2O(g) FeO(s)+H2(g) △H2,平衡常数为K2
FeO(s)+H2(g) △H2,平衡常数为K2
在不同温度时K1、K2的值如下表:
|
|
700℃ |
900℃ |
|
K1 |
1.47 |
2.15 |
|
K2 |
2.38 |
1.67 |
①反应 CO2(g) + H2(g) CO(g) + H2O(g) △H
,平衡常数K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应
CO(g) + H2O(g) △H
,平衡常数K,则△H= (用△H1和△H2表示),K= (用K1和K2表示),且由上述计算可知,反应
CO2(g) + H2(g) CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
CO(g) + H2O(g)是 反应(填“吸热”或“放热”)。
②能判断CO2(g) + H2(g) CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
CO(g) + H2O(g)达到化学平衡状态的依据是 (填序号)。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)= v逆(H2O) D.c(CO)= c(CO2)
(2)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,发生反应Fe(s)+CO2(g) FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示:
FeO(s)+CO(g) △H > 0,CO2的浓度与时间的关系如图所示:
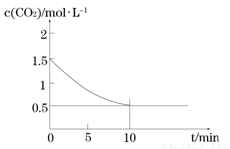
① 该条件下反应的平衡常数为 ;若铁粉足量,CO2的起始浓度为2.0 mol·L-1,则平衡时CO2的浓度为 mol·L-1。
②下列措施中能使平衡时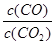 增大的是 (填序号)
增大的是 (填序号)
A.升高温度
B.增大压强
C.充入一定量的CO2
D.再加入一定量铁粉
查看答案和解析>>
科目: 来源:2011-2012学年湖北省襄阳市高三3月调研考试理科综合试卷(化学部分) 题型:实验题
(15分)某化学小组拟采用如下装置(夹持和加热仪器等已略去)来电解饱和食盐水,

并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时验证氯气的氧化性。
(1)写出甲中反应的离子方程式 。
(2)为完成上述实验,正确的连接顺序为A连 ,B连 (填接口字母)。
(3)乙装置中X试剂可以是 ,丙装置中Y试剂的作用是 。
(4)测定Cu的相对原子质量。将w g CuO置于硬质玻璃管中,足量的H2与之充分反应后,按以下两个方案测得的数据计算Cu的相对原子质量。
|
方 案 质 量 |
方案一 |
方案二 |
|
U型管+固体 |
硬质玻璃管+固体 |
|
|
反应前质量/g |
a |
c |
|
完全反应后质量/g |
b |
d |
你认为方案 较佳,另一个方案得到的Cu的相对原子质量会 (填“偏低”、“偏高”)。按较佳方案计算,得到Cu的相对原子质量是 。
查看答案和解析>>
科目: 来源:2011-2012学年湖北省襄阳市高三3月调研考试理科综合试卷(化学部分) 题型:填空题
【化学——选修2:化学与技术】(15分)
以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:

(1)沸腾炉中发生反应的化学方程式为 ;接触室中发生反应的化学方程式是 。
(2)沸腾炉出来的炉气需要精制,如果不经过精制,对SO2催化氧化的影响是
(3)硫酸工业是一种易造成多种形式污染的工业,工业上常采用氨—酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理: ;对矿渣的合理利用方法是 。
(4)某工厂用500t 含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是 t。
查看答案和解析>>
科目: 来源:2011-2012学年湖北省襄阳市高三3月调研考试理科综合试卷(化学部分) 题型:填空题
【化学——选修3:物质结构与性质】(15分)
用黄铜矿(主要成分是CuFeS2)生产粗铜的反应原理如下:
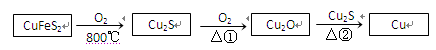
(1)已知在反应①、②中均生成相同的气体分子,该气体具有漂白性。请分别写出反应①、
②的化学方程式是 、 。
(2)基态铜原子的核外电子排布式为 ,硫、氧元素相比,第一电离能较大的是 。
(3)反应①和②生成的气体分子的中心原子的杂化类型是 ,分子的空间构型是 。
(4)某学生用硫酸铜溶液与氨水做了一组实验,CuSO4溶液中加氨水生成蓝色沉淀,再加氨水沉淀溶解,得到深蓝色透明溶液,最后向该溶液中加入一定量乙醇,析出[Cu(NH3)4]SO4·H2O晶体,请解释加入乙醇后析出晶体的原因 ;在该晶体中存在化学键的种类有 。
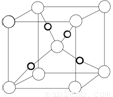
(5)Cu2O的晶胞结构如图所示,该晶胞的边长为a cm,则Cu2O的密
度为 g·cm-3(用NA表示阿伏加德罗常数的数值)。
查看答案和解析>>
科目: 来源:2011-2012学年湖北省襄阳市高三3月调研考试理科综合试卷(化学部分) 题型:填空题
【化学——选修5:有机化学基础】(15分)
已知某有机物A为烃类化合物,其相对分子质量为70,各物质之间的转化关系如下图所示,其中B、D、E的结构中均含有2个甲基,且核磁共振氢谱都有4个峰。
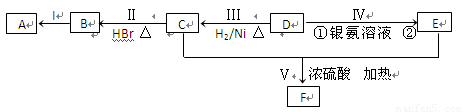
(1)A的分子式为 ,D中所含官能团的名称为 。
(2)I的反应条件为 ,Ⅲ的反应类型为 。
(3)写出反应Ⅳ中①的化学方程式 。
(4)写出反应Ⅴ的化学方程式 。
(5)E有多种同分异构体。其中:
①能发生银镜反应,又能与金属钠反应生成氢气,但不能发生消去反应: ;
②能在酸性条件下水解,且两种水解产物相对分子质量相同: 。
查看答案和解析>>
科目: 来源:2011-2012学年湖北省高三起点考试化学试卷 题型:选择题
发展低碳经济、减少能源消耗、走可持续的发展之路,这对中国经济发展既是机遇也是挑战,下列说法不正确的是 ( )
A.积极开发风能发电和水力发电。
B.尽量用纯液态有机物代替水作溶剂。
C.提高原子利用率,发展绿色化学
D.积极开发半导体节能灯具
查看答案和解析>>
科目: 来源:2011-2012学年湖北省高三起点考试化学试卷 题型:选择题
化学已渗透到人类生活的各个方面。下列说法不正确的是 ( )
A.人造纤维、合成纤维和光导纤维都是有机高分子化合物
B.可以用Si3N4、Al2O3制作高温结构陶瓷制品
C.地球上CH4、CO2等气体含量上升容易导致温室效应加剧,进而引发灾难性气候
D.禁止使用四乙基铅作汽油抗爆震剂,可减少汽车尾气污染
查看答案和解析>>
科目: 来源:2011-2012学年湖北省高三起点考试化学试卷 题型:选择题
若NA表示阿伏加德罗常数,下列说法正确的是 ( )
A.0.2 mol过氧化氢完全分解转移的电子数目为0.4 NA
B.12.8g Cu与足量HNO3反应生成NO和NO2,转移电子数目为0.2 NA'
C.1 mol C3OH62分子中含有共价键的数目为91 NA
D.1 mol SiO2晶体中含有NASiO2个分子
查看答案和解析>>
科目: 来源:2011-2012学年湖北省高三起点考试化学试卷 题型:选择题
下列液体均处于25℃,有关叙述正确的是 ( )
A.某物质的溶液pH <7,则该物质一定是酸或强酸弱碱盐
B.AgCl在相同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
C.pH=5.6的CH3COOH与CH3COONa混合溶液中,c(Na+)> c(CH3COO一)
D.pH=4.5的番茄汁中c(H+)是pH=6.5的牛奶中c(H+)的100倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com