
科目: 来源: 题型:
下列变化肯定属于化学变化的是 ( )
①物质发生爆炸 ②由铝原子变成铝离子 ③酒精的燃烧
④火柴梗蘸一点儿浓硫酸变黑 ⑤汽油挥发
A.②③④ B.①②④ C.①④⑤ D.③⑤
查看答案和解析>>
科目: 来源: 题型:
小明发现家中一枚戒指生满了铜绿,他和同学利用这枚戒指展开了研究性学习。
[查阅资料]真金在空气中不会生锈,生满铜绿的“金戒指”材质为铜锌合金;
铜长期露置在潮湿的空气中能生成铜绿,其主要成分是碱式碳酸铜,碱式碳酸铜受热易分解生成CuO、H2O和CO2 。
据上述资料可推知,碱式碳酸铜由 种元素组成。
[实验探究]将该枚戒指加入过量稀盐酸中,有气泡产生,溶液由无色逐渐变为蓝绿色。
(1)小明认为:气体中除了含有CO2,还可能含有少量 。
(2)小红认为蓝绿色溶液中的溶质只有氯化锌。小华认为溶液中的溶质除了氯化锌外,
还应该含有 、 。他取适量上述蓝绿色溶液,加入光亮的铁片,观察到了现象:① ,② ,证实了自己的观点。
(3)小娟取适量新制的FeCl2溶液,加入锌粒,一时间后,溶液颜色变浅。结合小华的实验可推知:铁、锌、铜三种金属的活动性由弱到强的顺序是 。
(4)小明想进一步探究“金戒指”中铜元素的含量,取一枚同材质的“金戒指”,称得质量为3.8g。在老师的指导下,将“金戒指”经浓硝酸氧化、碱化等步骤处理后,最终得到纯净的氧化铜,称得质量仍然为3.8g(实验过程中铜元素损失忽略不计)。则“金戒指”中铜元素的质量分数是多少?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
课外活动小组的同学在测定由NaCl和Na2CO3形成的固体混合物组成时,进行了以下实验:取40 g固体混合物配成溶液,平均分为四份,然后分别加入一定质量分数的CaCl2溶液,实验数据见下表:
| 实验一 | 实验二 | 实验三 | 实验四 | |
| 原固体混合物质量 | 10g | 10g | 10g | 10g |
| 加入CaCl2溶液质量 | 10g | 20g | 30g | 40g |
| 生成的沉淀的质量 | 2g | m | 5g | 5g |
请分析
表中数据回答并计算[(4)要求写计算过程 ]
(1)生成的沉淀是(填写化学式) 。 (2)10g原固体混合物配成的溶液和足量CaCl2溶液反应,最多生成沉淀质量为 g。
(3)m= g。
(4)原固体混合物中NaCl的质量分数是多少?
查看答案和解析>>
科目: 来源: 题型:
现代生活中,人们越来越注意微量元素的摄入。血红蛋白中的铁是人体内氧的输送者,缺铁易患贫血。
(1)一种添加了营养剂的“铁强化”酱油已经面市。根据卫生部铁强化剂添加标准,每100mL酱油中铁营养剂添加量是200mg,该营养铁元素质量分数为12.5%。根据实验测得,酱油中铁只有10%能被人体吸收,以某人一天使用16mL该酱油计算,他一天从酱油中吸收的铁元素是多少毫克?
(2)某贫血患者除正常饮食吸收铁元素外,还需服用含铁元素的某种药物。若治疗一个疗程需补充1.12g铁元素,则服用药物中的铁元素相当于需要硫酸亚铁晶体(FeSO4•7H2O)多少克?
查看答案和解析>>
科目: 来源: 题型:
人体的汗液有咸味。小庭和小怡同学猜测汗液中可能含有氯化钠,为此她们准备做探究实验。她们想到两种提取汗液的方法,方法一:用胶头滴管直接吸取足量汗液转移到烧杯中,再加入适量蒸馏水稀释;方法二:用出汗的手在盛有自来水的容器中清洗,再将清洗后的自来水部分转移到烧杯中。其中方法 是正确的。
在老师指导下,她们用正确的方法提取汗液,进行以下实验:
(1)用试管取适量提取液,滴入硝酸钡溶液,没有出现白色沉淀,说明汗液中 (填:“有”或“无”)硫酸和硫酸盐。
(2)用试管取适量提取液,滴入硝酸银溶液,发现有白色沉淀出现,加入稀硝酸后沉淀不溶解。由此可推测该白色沉淀物的化学式是 。
(3)将适量提取液倒入蒸发皿中加热蒸发,出现类似食盐的小颗粒。
你认为她能否仅凭上述三步实验得出“这些小颗粒就是氯化钠”?
查看答案和解析>>
科目: 来源: 题型:
由于大量使用一次性塑料方便袋而造成的“白色污染”已成为一个严重的社会问题。某化学研究小组的同学对某种塑料袋的组成进行分析研究(资料显示该塑料只含C、H两种元素)。他们设计了图18所示的实验装置,使该塑料试样在纯氧中完全燃烧,观察实验现象、分析有关数据、推算元素含量。
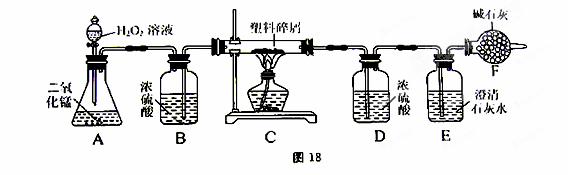 (1)实验装置中有一处明显错误,请指出错误处,并写出(或在答题卷上画出正确图并用字母标注上哪一个装置)改正方法 ▲
(1)实验装置中有一处明显错误,请指出错误处,并写出(或在答题卷上画出正确图并用字母标注上哪一个装置)改正方法 ▲
(2) 装置F的作用是 ▲ .
(3) 若装置C的玻璃管中放入的塑料试样质量为5.9g,塑料试样充分燃烧后,装置D增重7.2g,则该塑料试样中含氢元素的质量为 ▲ g;假设塑料的组成为CxHy,则装置C的玻璃管中反应的化学方程式为 ▲ (化学计量数用含x、y的代数式表示,且可以是分数)
(4)若装置中没有连接装置B,将使该塑料试样中氢元素的质量测算结果 ▲ ( 填“偏小”、“ 偏大”或“无影响” )
查看答案和解析>>
科目: 来源: 题型:
有一包固体混合物,可能由硝酸钠、硝酸钡、氯化钙、碳酸钾中的一种或几种混合而成。为了确定其组成成分,进行如下实验:
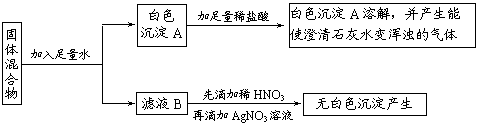 |
请分析上述实验,完成下列问题:
(1)原固体混合物中一定含有的物质是 ▲ 。
(2)白色沉淀A中加入稀盐酸的化学反应方程式为 ▲ 。
(3)原固体混合物中一定不含有的物质是 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
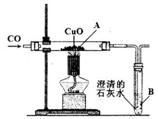
某同学设计右图所示的实验装置,进行一氧化碳还原氧化铜的实验。试回答:
(l)该装置存在的一个主要问题是 ▲ 。
(2) 实验开始时,是先给氧化铜加热,还是先通人一氧化碳? ▲
(3)实验过程中,图中A处能观察到的实验现象是 ▲ 。发生反应的化学方程式为 ▲ 。
查看答案和解析>>
科目: 来源: 题型:
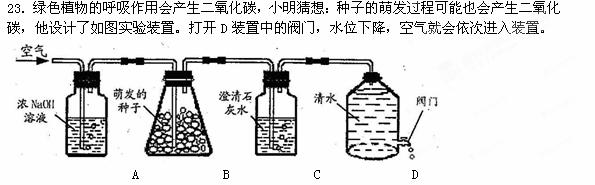 (1)按照实验设计意图,如果观察到C装置中澄清石灰水变浑浊现象,则小明的猜想是正确的。但思维严密的小庭却认为实验还有漏洞,她建议在 ▲ (选填:AB、BC或CD)之间再增加一个C装置,就可以弥补上图实验设计的不足,那么,改进后的实验装置中,当观察到 ▲ 现象时才能证明小明的猜想是正确的。
(1)按照实验设计意图,如果观察到C装置中澄清石灰水变浑浊现象,则小明的猜想是正确的。但思维严密的小庭却认为实验还有漏洞,她建议在 ▲ (选填:AB、BC或CD)之间再增加一个C装置,就可以弥补上图实验设计的不足,那么,改进后的实验装置中,当观察到 ▲ 现象时才能证明小明的猜想是正确的。
(2)请指出D装置的一个优点: ▲ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com