
科目: 来源:同步题 题型:填空题
 NaCl(l)+ K(g)- Q 该反应的平衡常数可表示为:K = C(K)各物质的沸点与压强的关系见下表。
NaCl(l)+ K(g)- Q 该反应的平衡常数可表示为:K = C(K)各物质的沸点与压强的关系见下表。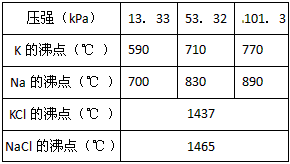
查看答案和解析>>
科目: 来源:期末题 题型:单选题
 2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是
2SO3(g);ΔH=-Q kJ·mol-1(Q>0)。下列说法正确的是 查看答案和解析>>
科目: 来源:期末题 题型:单选题
 Ur-(尿酸根离子)+H3O+;
Ur-(尿酸根离子)+H3O+; NaUr(s) 下列对反应②的叙述中正确的是
NaUr(s) 下列对反应②的叙述中正确的是查看答案和解析>>
科目: 来源:期末题 题型:单选题
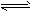 gZ(g)的ΔH<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是
gZ(g)的ΔH<0,在恒容密闭容器中反应达到平衡时,下列说法正确的是 查看答案和解析>>
科目: 来源:期末题 题型:填空题
 2C(g)
2C(g)查看答案和解析>>
科目: 来源:期末题 题型:单选题
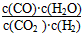 ,恒容时,温度升高,H2浓度减小。下列说法正确的是
,恒容时,温度升高,H2浓度减小。下列说法正确的是 CO2 + H2
CO2 + H2 查看答案和解析>>
科目: 来源:期末题 题型:单选题
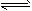 N2(g)+CO2(g)ΔH=-373.4kJ·mol-1在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是
N2(g)+CO2(g)ΔH=-373.4kJ·mol-1在恒容的密闭容器中,反应达到平衡后,改变某一条件,下列示意图正确的是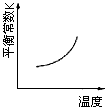

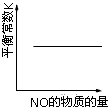
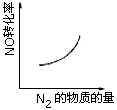
查看答案和解析>>
科目: 来源:期末题 题型:填空题
 N2O4(g) ΔH<0,在一定条件下已经达到平衡。若恒容条件下升温,平衡 移动___________(填“向左”“向右”或“不”);若只缩小体积气体颜色将_________(填“加深”、“变浅”或“不变”);若在恒温、恒压条件下向平衡体系中通入氩气,平衡_________移动(填“向左”“向右”或“不”);使用催化剂_________反应的ΔH(填“增大”“减小”或“不改变”)。
N2O4(g) ΔH<0,在一定条件下已经达到平衡。若恒容条件下升温,平衡 移动___________(填“向左”“向右”或“不”);若只缩小体积气体颜色将_________(填“加深”、“变浅”或“不变”);若在恒温、恒压条件下向平衡体系中通入氩气,平衡_________移动(填“向左”“向右”或“不”);使用催化剂_________反应的ΔH(填“增大”“减小”或“不改变”)。  PtF6-(g) ΔH2= - 771.1 kJ·mol-1
PtF6-(g) ΔH2= - 771.1 kJ·mol-1 查看答案和解析>>
科目: 来源:期末题 题型:填空题
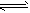 H2(g)+I2(g),H2物质的量随时间的变化如图所示。
H2(g)+I2(g),H2物质的量随时间的变化如图所示。
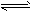 2HI(g)的平衡常数K=_________。
2HI(g)的平衡常数K=_________。查看答案和解析>>
科目: 来源:期末题 题型:填空题
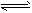 2NH3(g) 已知298K时:正反应的△H=-92.4KJ/mol,△S=-198.2J/mol/K。
2NH3(g) 已知298K时:正反应的△H=-92.4KJ/mol,△S=-198.2J/mol/K。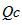 )
)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com