
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
在t℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。又知t℃时AgCl的Ksp=4×10-10,下列说法不正确的是( )

A.在t℃时,AgBr的Ksp为4.9×l0-13
B.在AgBr饱和溶液中加入NaBr固体,可使溶液由c点到b点
C.图中a点对应的是AgBr的不饱和溶液
D.在t℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl- (aq)的平衡常数K≈816
AgBr(s)+Cl- (aq)的平衡常数K≈816
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
分子式为C9H12的所有带苯环结构的异构体中,在催化剂条件下与液溴发生取代反应,其苯环上的一溴代物为三种的结构有( )
A.1种 B.2种 C.3种 D.4种
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
室温下,用0.100mol·L-1 NaOH溶液分别滴定20.00ml 0.100mol·L-1 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是( )
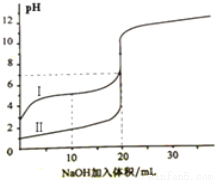
A. Ⅰ表示的是滴定盐酸的曲线
B.PH=7时,滴定醋酸消耗V(NaOH)小于20ml
C.V(NaOH) =20ml时,两份溶液中C(Cl—)== C(CH3COO—)
D.V(NaOH) =10ml时,醋酸溶液中:C(Na+ )> C(CH3COO—)> C(H+ )> C(OH—)
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
我国古代青铜器工艺精湛,有很高的艺术价值和历史价值,但出土的青铜器大多受到环境腐蚀,故对其进行修复和防护具有重要意义。 如图为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。下列说法不正确的是( )

A.腐蚀过程中,负极是c
B.正极反应是O2 + 4e-+2H2O=4OH-
C.若生成4.29 g Cu2(OH)3Cl,则理论上耗氧体积为0.224L(标准状况)
D.环境中的Cl扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl,其离子方程式为2Cu2++3OH-+Cl-=Cu2 (OH)3Cl↓
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
在2 L的密闭因为生成是Cu2(OH)3Cl沉淀,因此总电极反应式为:容器中,发生以下反应:2A(g)+B(g) 2C(g)+D(g)。若最初加入的A和B都是4 mol,在前10 s A的反应速率为 0.12 mol/(L·s),则10 s时,容器中B的物质的量是( )
2C(g)+D(g)。若最初加入的A和B都是4 mol,在前10 s A的反应速率为 0.12 mol/(L·s),则10 s时,容器中B的物质的量是( )
A.1.6mol B.2.8mol C.2.4mol D.1.2mol
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:推断题
下图中,A~L为常见物质或该物质的水溶液,B在A气体中燃烧产生棕黄色烟,B、G为中学化学中常见的金属单质,E的稀溶液为蓝色,I的焰色反应为黄色,组成J的元素原子核内只有一个质子,F为无色、有刺激性气味的气体,且能使品红溶液褪色。

请回答下列问题:
(1)框图中所列物质中属于非电解质的物质是_____________;
(2)将D的水溶液蒸干并灼烧得到的固体物质的化学式为___ _______;
(3)在一定物质的量浓度的硝酸铵溶液中滴加适量的K溶液,使溶液的pH=7,则溶液中c(Na+)_______c(NO3―)(选填“>”“=”或“<”)。
(4)①4 g J在纯氧中完全燃烧生成液态化合物,放出热量为QkJ,写出表示J燃烧热的热化学方程式 。
②A是重要的化工原料,工业上制取A的反应的化学方程式为___________。
(5)与F组成元素相同的一种-2价酸根离子M,M中两种元素的质量比为4∶3,已知1 mol A单质与含1 mol M的溶液能恰好完全反应,反应时仅观察到有浅黄色沉淀产生。取反应后的上层清液加入盐酸酸化的氯化钡溶液,有白色沉淀产生。则A单质与含M的溶液反应的离子方程式为:_______ 。
(6)25℃时,若Ksp(H)=2.2×10-20,向0.022mol/L的E溶液中逐滴滴入溶液K,当开始出现沉淀时,溶液中的c(OH-)= 。
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:推断题
甲苯是有机化工生产的基本原料之一。利用乙醇和甲苯为原料,可按下列路线合成分子式均为C9H10O2的有机化工产品E和J。

请回答:
(1)写出下列反应方程式
①B+D→E_____________________________。
②G→H_______________________________。
(2)①的反应类型为__________;②的反应类型为________;F的结构简式为__________。
(3)E、J有多种同分异构体,写出符合下列条件的4种同分异构体的结构简式。要求:①与E、J属同类物质②苯环上有两个取代基且苯环上的一氯代物只有两种。___________________
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:填空题
为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要。
(1)在汽车排气管内安装催化转化器,可将汽车尾气中主要污染物转化为无毒的大气循环物质。
已知:① N2(g) + O2(g)  2NO(g) △H1=+180.5 kJ·mol-1
2NO(g) △H1=+180.5 kJ·mol-1
② C和CO的燃烧热(△H)分别为-393.5 kJ·mol-1和-283 kJ·mol-1
则2NO(g) + 2CO(g)  N2(g) + 2CO2(g)的△H=_____kJ·mol-1
N2(g) + 2CO2(g)的△H=_____kJ·mol-1
(2)将0.20 mol NO和0.10 mol CO充入一个容积为1L的密闭容器中,反应过程中物质浓度变化如图所示。
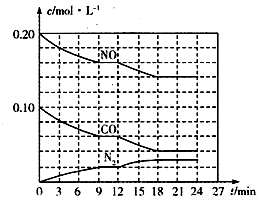
①CO在0-9min内的平均反应速率v(CO)=________mol·L-1·min-1(保留两位有效数字);第12 min时改变的反应条件可能为________。
A.升高温度 B.加入NO C.加催化剂 D.降低温度
②该反应在第24 min时达到平衡状态,CO2的体积分数为________(保留三位有效数字),化学平衡常数值为________(保留两位有效数字)。
(3)烟气中的SO2可用某浓度NaOH溶液吸收,若将一定量的SO2气体通入到300mL NaOH的溶液中,再在所得溶液中逐滴加入稀盐酸至过量,产生的气体与反应的HCl两者物质的量的关系如图所示(气体的溶解和HCl的挥发忽略,NaHSO3水溶液为酸性):
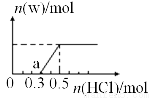
①O点溶液中所含溶质的化学式为_________________;
②a点溶液中各离子溶度大小关系为______________;
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:填空题
NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品中;NH4HSO4在分析试剂、医药、电子工业中用途广泛,请回答下列问题:
(1)相同条件下,pH相同的NH4Al(SO4)2中c(NH4+)_________(填“=”、“>” 或“<”)NH4HSO4中c(NH4+)。
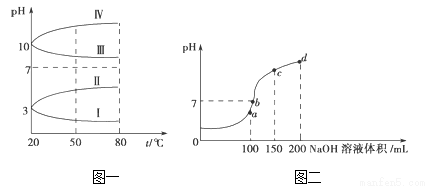
(2)如图1是0.1 mol•L﹣1电解质溶液的pH随温度变化的图象。
①其中符合0.1 mol•L﹣1 NH4Al(SO4)2的pH随温度变化的曲线是_______(填写字母);
②室温时,0.1 mol•L﹣1 NH4Al(SO4)2中2c(SO42-)﹣c(NH4+)﹣3c(Al3+)=________ mol•L﹣1(填数值)
(3)室温时,向100 mL 0.1mol•L﹣1 NH4HSO4溶液中滴加0.1mol•L﹣1 NaOH溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图2所示。
试分析图中a、b、c、d四个点,水的电离程度最大的是_____;在c点,溶液中各离子浓度由大到小的排列顺序是_________________。
查看答案和解析>>
科目: 来源:2017届江西省南五校高三上学期第一次模拟考试化学试卷(解析版) 题型:填空题
(I)甲烷在一定条件下可生成以下微粒:
A.碳正离子(CH3+) B.碳负离子(CH3—)
C.甲基(—CH3) D.碳烯 (︰CH2)
①四种微粒中,键角为120°的是 (填序号)。
②碳负离子(CH3—)的空间构型为 ,与CH3—互为等电子体的一种分子是 (填化学式)
(II )在制取合成氨原料气的过程中,常混有一些杂质,如CO会使催化剂中毒。除去CO的化学方程式为(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3=Cu(NH3)3(CO)Ac。请回答下列问题:
①C、N、O的电负性由大到小的顺序为 。
②写出Cu的核外电子排布式 。
③化合物Cu(NH3)3(CO)Ac中,金属元素的化合价为 。
④在一定条件下NH3和CO2能合成尿素CO(NH2)2,尿素中C原子轨道的杂化类型为 ;1mol尿素分子中, σ 键的数目为 。
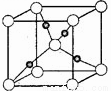
⑤Cu2O晶体的晶胞结构如图所示,若阿伏伽德罗常数为NA,晶胞的边长为a pm,则晶体的密度为___ g·cm—3。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com