
科目: 来源: 题型:
. 完全燃烧标准状况下某气态烷烃和气态烯烃的混合物2. 24L, 生成CO26.6g, 水4.05g.
(1)混合气体的平均相对分子质量是____ _______.
(2)混合气体的成份是_______、_________;其体积分数分别为_______%___ ___%。
查看答案和解析>>
科目: 来源: 题型:
下列说法错误的是
A.石油中含有C5~C11的烷烃,可以通过石油的分馏得到汽油
B.含C18以上烷烃的重油经过催化裂化可以得到汽油
C.煤是由有机物和无机物组成的复杂的混合物
D.煤中含有苯和甲苯,可以用先干馏后分馏的方法把它们分离出来
查看答案和解析>>
科目: 来源: 题型:
下列各溶液中,微粒的物质的量浓度关系正确的是
A.等体积、等物质的量浓度的CH3COONa与CH3COOH溶液混合:
2c(Na+)=c(CH3COO-)+c(CH3COOH)
B.0.1mol/L pH为10的NaHB溶液中:c(HB-)>c(B2-)>c(H2B)
C.常温下,将pH=10的NaOH溶液和pH=4的CH3COOH溶液等体积混合:
c(Na+)=c(CH3COO-)>c(H+)=c(OH-)
D.等物质的量浓度的(NH4)2SO4和(NH4)2CO3溶液中的c(![]() ):前者<后者
):前者<后者
查看答案和解析>>
科目: 来源: 题型:
某工厂废水中含游离态氯,通过下列实验测定其浓度。
①取水样10.00mL于锥形瓶中,加入10.00mL KI溶液(足量),滴入指示剂2~3滴。
②取一只碱式滴定管依次用自来水、蒸馏水洗净,然后注入0.010 mol·L-1 Na2S2O3溶液,调整液面,记下读数。
③将锥形瓶置于滴定管下进行滴定,发生的反应为:I2+2Na2S2O3=2NaI+Na2S4O6。
试回答下列问题:
(1)步骤①加入的指示剂是 。
(2)滴定时,眼睛应注视____________________,
判断到达滴定终点的现象是 ,
若耗去Na2S2O3溶液20.00mL,则废水中Cl2的物质的量浓度为__________________。
(3)Cl2的实际浓度比所测浓度应__________________(“偏大”、“偏小”或“相等”),造成误差的原因是 。(若认为没有误差,此问不答)
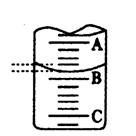
(4)右图表示50mL滴定管中液面的位置,若A与C刻度间相差1mL,A处的 刻度为25,滴定管中液面读数应为 mL,设此时液体体积读
数为a ml ,滴定管中液体的体积 V (=、>、<) ( 50-a )ml
(5)滴定结束时俯视刻度线读取滴定终点时Na2S2O3溶液的体积,会导致测定结果 (“偏大”、“偏小”或“不影响”)。
查看答案和解析>>
科目: 来源: 题型:
已知0.1 mol/L的醋酸溶液中存在电离平衡:CH3COOH![]() CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
CH3COO-+H+,要使溶液中c(H+)/c(CH3COOH)值增大,可以采取的措施是
A.加少量烧碱溶液 B.降低温度 C.加少量冰醋酸 D.加水
查看答案和解析>>
科目: 来源: 题型:
M是生产某新型塑料的基础原料之一,分子式为C10H10O2,其分子结构模型如图,所示(图中球与球之间连线代表化学键单键或双键)。
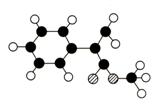
拟从芳香烃![]() 出发来合成M,其合成路线如下:
出发来合成M,其合成路线如下:
已知:M在酸性条件下水解生成有机物F和甲醇。

(1)根据分子结构模型写出M的结构简式
(2)写出②、⑤反应类型分别为 、
(3)D中含氧官能团的名称为 ,E的结构简式
(4)写出反应⑥的化学方程式(注明必要的条件) 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
能源开发、环境保护、资源利用等是当今社会的热门话题。请根据所学化学知识回答下列问题:
(1)汽车上安装催化转化器,可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应,生成无毒物质,减少汽车尾气污染。
已知:N2(g) + O2(g)=2NO(g) △H=+180.5 kJ · mol-1;
2C(s)+ O2(g)=2CO(g) △H=-221.0 kJ · mol-1;
C(s)+ O2(g)=CO2(g) △H=-393.5 kJ · mol-1
则尾气转化反应2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H=________________。
(2)汽车尾气分析仪对CO的含量分析是以燃料电池为工作原理,其装置如下图所示,该电池中电解质为氧化钇-氧化钠,其中O2-可以在固体介质中自由移动。

下列说法中正确的是_____________(填字母序号)。
A.负极的电极反应式为:CO + O2-―2e-=CO2
B.工作时电子由电极a通过传感器流向电极b
C.工作时电极b作正极,O2-由电极a通过固体介质向电极b迁移
D.传感器中通过的电流越大,尾气中CO的含量越高
(3)某硝酸厂利用甲醇处理废水。在一定条件下,向废水中加入CH3OH,将HNO3还原成N2。若该反应消耗32 g CH3OH转移6 mol电子,则参加反应的还原剂和氧化剂的物质的量之比为______________。
(4)煤的间接液化是先转化为CO和H2,再在催化剂作用下合成甲醇。若在一定温度下,向1 L密闭容器中加入CO和H2,发生反应CO(g)+2H2(g) ![]() CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
CH3OH(g),经10 min反应达到平衡时测得各组分的浓度如下:
| 物 质 | CO | H2 | CH3OH |
| 浓度/(mol·L-1) | 1.2 | 1.0 | 0.6 |
查看答案和解析>>
科目: 来源: 题型:
下列反应既是氧化还原反应,而且△H>0的是
A. 铝片与稀H2SO4反应 B. Ba(OH)2·8H2O与NH4Cl的反应
C. 灼热的炭与CO2反应 D. 甲烷在O2中的燃烧反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com