
科目: 来源:不详 题型:填空题
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.0.1mol?L-1NaHSO4溶液中:c(Na+)+c(H+)=c(SO42-)+c(OH-) |
| B.中和pH和体积都相同的盐酸和醋酸,消耗NaOH的物质的量之比为1:1 |
| C.pH=3的盐酸和pH=3的FeCl3溶液中,水电离的c(H+)不相等 |
| D.0.1mol?L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
查看答案和解析>>
科目: 来源:凯里市模拟 题型:问答题
查看答案和解析>>
科目: 来源:西城区一模 题型:填空题
| 溶质 | Na2CO3 | NaHCO3 | Na2SiO3 | Na2SO3 | NaHSO3 | NaClO |
| pH | 11.6 | 9.7 | 12.3 | 10.0 | 4.0 | 10.3 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
A.电解稀硫酸不可能发生的反应是Cu+H2SO4
| ||||
| B.李比希燃烧法、钠熔法、铜丝燃烧法、纸层析法都是元素定性分析法 | ||||
C.用0.1mol/LNaOH溶液分别滴定相同物质的量浓度和相同体积的盐酸和醋酸(如图),其中实线表示的是滴定盐酸的曲线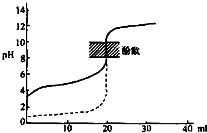 | ||||
| D.VLamol?L-1的氯化铁溶液中,若Fe3+的数目为NA,则Cl-的数目大于3NA |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| A.0.1mol?L-1CH3COONa溶液中:c(Na+)=c(CH3COO-)+c(OH-) |
| B.一定量Na2S溶液中各离子浓度存在以下关系:2c(Na+)=c(HS-)+c(H2S)+c(S2-) |
| C.中和PH与体积均相等的盐酸和醋酸溶液,消耗NaOH的物质的量相等 |
| D.若NH4HCO3溶液、NH4HSO4溶液和NH4NO3溶液中c(NH4+)相等,则c(NH4HSO4)<c(NH4NO3)<c(NH4HCO3) |
查看答案和解析>>
科目: 来源:不详 题型:多选题
| A.同温度下完全中和相等pH相等体积的氨水、NaOH、Ba(OH)2,所需相同浓度的盐酸体积相等 |
| B.某温度下0.1mol?L-1的NaHB溶液中,c(Na+)=0.1mol?L-1≥c(B2-) |
| C.在0.1mol?L-1醋酸铵溶液中,(CH3COOH)+c(H+)=c(NH3?H2O)+c(OH-) |
| D.0.1mol/L(NH4)2Fe(SO4)2溶液中,c(NH4+)>c(SO42-)>c(Fe2+)>c(H+)>cOH-) |
查看答案和解析>>
科目: 来源:不详 题型:填空题
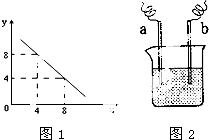
查看答案和解析>>
科目: 来源:东城区二模 题型:问答题

查看答案和解析>>
科目: 来源:同步题 题型:不定项选择题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com