
科目: 来源: 题型:
下列叙述中错误的是
A.油脂和蛋白质都是能发生水解反应的高分子化合物
B.一定条件下,Cl2 可在甲苯的苯环或侧链上发生取代反应
C.乙醇、乙酸和乙酸乙酯能用饱和碳酸钠溶液鉴别
D.加热时,乙醇在 Ag 催化下可被 O2 氧化为乙醛
查看答案和解析>>
科目: 来源: 题型:
溴乙烷是一种重要的有机化工原料,其沸点为38.4℃。制备溴乙烷的一种方法是乙醇与氢溴酸反应,该反应的化学方程式是
。
实际通常是用溴化钠与一定浓度的硫酸和乙醇反应。某课外小组欲在实验室制备溴乙烷的装置如右图,实验操怍步骤如下:

①检查装置的气密性;
②在圆底烧瓶中加入95%乙醇、80%硫酸,然后加入研细的溴化钠粉末和几粒碎瓷片;
③小心加热,使其充分反应。
请问答下列问题。
(1)装置A的作用是 。
(2)反应时若温度过高,则有![]() 生成,同时观察到还有一种红棕色气体产生,该气体的分子式是 。
生成,同时观察到还有一种红棕色气体产生,该气体的分子式是 。
(3)反应结束后,得到的粗产品呈棕黄色。为了除去粗产品中的杂质,可选择下列试剂中的 (填写上正确 选项的字母)。
a.稀氢氧化钠溶液 b.乙醇 c.四氯化碳
该实验操作中所需的主要玻璃仪器是 (填仪器名称)。
(4)要进一步制得纯净的溴乙烷,司继续用蒸馏水洗涤,分液后,再加入无水![]() ,
,
然后进行的实验操作是 (填写正确选项的字母)。
a.分液 b.蒸馏 c.萃取
(5)为了检验溴乙烷中含有溴元素,不能直接向溴乙烷中滴加硝酸银溶液来检验,其原因是 。
通常采用的方法是取少量溴乙烷,然后 (按实验的操作顺序选填
下列序号)。
①加热 ②加入![]() 溶液 ③加入稀
溶液 ③加入稀![]() 酸化 ④加入NaOH溶液
酸化 ④加入NaOH溶液
查看答案和解析>>
科目: 来源: 题型:
括号内物质为杂质,下列除去杂质的做法不正确的是
A.乙酸乙酯(乙酸和乙醇):用饱和Na2CO3溶液洗涤后分液
B.乙烷(乙烯):用浓溴水洗气
C.乙醇(乙酸):用NaOH溶液中和后分液
D.乙醇(水):用生石灰吸水后蒸馏
查看答案和解析>>
科目: 来源: 题型:
有机物X(C4H6O5)广泛存在于许多水果内,尤以萍果、葡萄、西瓜、山渣内为多,该化合物具有如下性质:
(1)1molX与足量的金属钠反应产生1.5 mol气体
(2)X与醇或羧酸在浓H2SO4和加热的条件下均生成有香味的产物
(3)X在一定程度下的分子内脱水产物(不是环状化合物)可和溴水发生加成反应
根据上述信息,对X的结构判断正确的是
A.X中肯定有碳碳双键 B.X中可能有三个羟基和一个 一COOR官能团
C.X中可能有三个羧基 D.X中可能有两个羧基和一个羟基
查看答案和解析>>
科目: 来源: 题型:
某小组同学欲制备SO2并探究其性质:
(一)实验室中需要SO2气体22.4 L(标准状况)。依据化学方程式Zn + 2 H2SO4(浓)![]() ZnSO4 + SO2↑ + 2 H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g/mL)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有杂质。
ZnSO4 + SO2↑ + 2 H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g/mL)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有杂质。
(1)所制得的气体中混有的杂质气体可能是 (填分子式)。产生这种杂质的主要原因是 (用化学方程式表达)。
(2)为证实相关分析,组装了如下装置,对所制取的气体进行探究。
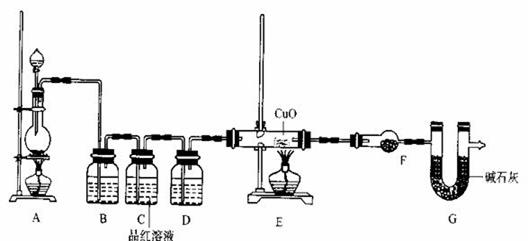
①装置B中加入的试剂是 ,作用是 。
②装置D中加入的试剂是 ,装置F中加入的试剂 是 。
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有该杂质气体的实验现象是 。
(二)利用下图所示的装置探究S![]() O2的性质:
O2的性质:
已知:熔点![]() :SO2 - 76.1℃,SO3 16.8℃;沸点:SO2 - 10℃,SO3 45℃
:SO2 - 76.1℃,SO3 16.8℃;沸点:SO2 - 10℃,SO3 45℃
| |
|
|
(1)装置I模拟工业生产SO3的反应,其化学方程式是 。
(2)甲同学按I、II、III、IV的顺序连接装置,装置II的作用是
;装置III中溶液![]() 逐渐褪色,有Mn2+生成,同时溶液酸性
逐渐褪色,有Mn2+生成,同时溶液酸性![]() 增强,则该反应的离子方程式是 。
增强,则该反应的离子方程式是 。
(3)乙同学按I、II、IV的顺序连接装置,若装置IV中有40 mL 2.5 mol??L-1 NaOH溶液,反应后溶液增重 4.8 g,则反应后溶液中含有的溶质有
(填化学式),对应溶质物质的量之比为 。
查看答案和解析>>
科目: 来源: 题型:
巳知某溶液中存在较多的H+、SO42—、NO3—,则该溶液中还可能大量存在的离子组是 ( )
A.Al3+、Fe2+、Cl— B.Mg2+、Ba2+、Br—
C.Mg2+、Cl—、I— D.Na+、NH4+、Cl—
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com