
科目: 来源: 题型:
2012年2月新华网报道,加拿大开发出生产医用放射性同位素99 43Tc的简单方法。下列关于 99 43Tc 的叙述正确的是 ( )
A.原子序数是99 B.质量数是43 C.中子数是99 D.电子数是43
查看答案和解析>>
科目: 来源: 题型:
硼酸(H3BO3)是一种片层状结构的白色晶体(下图),有滑腻感,可做润滑剂。硼酸对人体受伤组织有缓和和防腐作用,故可以用于医药和食品防腐等方面。回答下列问题:
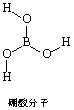

B原子结构示意图为_______________________。
硼酸为一元弱酸,在水中电离方程式为H3BO3+H2O![]() [B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_______________________________________________。
[B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_______________________________________________。
下列有关硼酸晶体的说法正确的是_______________。
A.H3BO3分子的稳定性与氢键有关
B.平均1 mol H3BO3的晶体中有3 mol氢键
C.硼酸晶体中层与层之间作用力是范德华力
D.B为sp2杂化,同一层内主要作用力是共价键和氢键
根据对角线规则,与B性质相似的元素是________。
含氧酸的通式为(HO)mROn,根据非羟基氧原子数判断,与H3BO3酸性最接近的是______。
A.HClO B.H4SiO4 C.H3PO4 D.HNO2
一种硼酸盐的阴离子为B3O6n-,n=______;B3O6n-结构中只有一个六元环,B的空间化学环境相同,O有两种空间化学环境,画出B3O6n-的结构图(注明所带电荷数):
____________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
前四周期元素X、Y、Z、W核电荷数依次增加,核电荷数之和为58;Y 原子的M层p轨道有3个未成对电子;Z与Y同周期,且在该周期中电负性最大;W原子的L层电子数与最外层电子数之比为4∶1,其d轨道中的电子数与最外层电子数之比为5∶2。
X的元素符号为_______,Z元素位于周期表第_______周期第________族。
Y与X形成共价化合物A,Z与X形成共价化合物B,A与B还原性较强的是________(写分子式)。
Z的最高价氧化物的水化物的化学式为________________。
12.4 g单质Y4与0.3 mol O2在一定条件下恰好完全反应生成0.1 mol化合物C,一个C分子中所含有的![]() 键数目为 。
键数目为 。
含W元素的最高化合价的含氧酸根离子是___________,该含氧酸根离子在分析化学中有重要作用,请写出在酸性条件下该含氧酸根离子与Fe2+反应的离子方程式:
______________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
X、Y、Z、W、Q、R六种短周期主族元素,原子序数依次增大,Z基态原子核外有三个未成对电子,Y、Z、W分别与X形成常见化合物的分子结构依次为正四面体、三角锥形和V形,Q的各级电离能如下表,W与R是同族元素。
| Q | I1 | I2 | I3 | I4 | I5 | … |
| 电离能(kJ/mol) | 496 | 4562 | 6912 | 9543 | 13353 | … |
回答下列有关问题:
W原子的价电子排布图为_______________________________。
化合物Q2W2的电子式_________________,化合物XYZ的结构式________________。
Y、Z、W分别与X形成常见化合物的沸点由高到低的顺序是____________________(用分子式表示)。
RW3分子中的键角___________,W3分子的立体构型是_______________形。
根据等电子原理,指出与YW2互为等电子体且含有Z原子的微粒有 、
(要求写一种分子和一种离子)。
查看答案和解析>>
科目: 来源: 题型:
钛(Ti)被誉为“21世纪的金属”。工业上将TiO2与焦炭混合,通入Cl2高温下制得TiCl4;再将TiCl4提纯后,在氩气保护下与镁高温反应制得Ti。其反应如下:
①TiO2+2Cl2+2C![]() TiCl4+2CO
TiCl4+2CO
②TiCl4+2Mg![]() Ti+2MgCl2
Ti+2MgCl2
回答下列问题:
Ti元素原子的价电子排布式为_____________________。
与CO互为等电子体的分子是___________。
已知TiCl4在通常情况下是无色液体,熔点为–37℃,沸点为136℃;TiCl4在潮湿空气中易水解产生白雾,同时产生H2TiO3固体。
① TiCl4为______化合物(填“离子”或“共价”)。
② TiCl4分子为正四面体形,则Ti为________杂化。
③ TiCl4在潮湿空气中水解的化学方程式是_____________________________________。
④ TiO2、Cl2和C反应制得的TiCl4最好的提纯方法是____________ (填操作名称)。
配离子[TiCl(H2O)5]2+的中心离子化合价为 ,中心离子配位数为 。
查看答案和解析>>
科目: 来源: 题型:
回答下列问题
CH4、CO2、COCl2和![]() 四种分子中,碳原子为sp2杂化的分子是_______________________________________________。
四种分子中,碳原子为sp2杂化的分子是_______________________________________________。
NH3分子的立体构型是___________形,联氨(N2H4)可视为是NH3分子中的一个氢原子被氨基(-NH2)取代所形成的物质,写出联氨加入足量盐酸反应的化学方程式_________________________________________________________________。
H2O、H2O2 、OF2和SCl2四种分子中各原子均达8电子结构的分子是________________。
N2H4与H2O2反应:N2H4(l)+2H2O2=N2(g)+4H2O(g) ,若该反应中有4 mol N—H键断裂,则形成![]() 键有_______mol和形成
键有_______mol和形成![]() 键有_______mol。
键有_______mol。
H2O熔沸点都比H2S高,其原因是___________________________________________。
查看答案和解析>>
科目: 来源: 题型:
下表为周期表的一部分,表中所列的字母分别代表一种化学元素。

用化学用语回答下列问题:
写出元素f的基态原子核外电子排布式___________________________。
在c6a6分子中,元素c为 杂化,该分子是 分子(填“极性”或“非极性”)。
ci2分子的电子式为_________________________,ci2与ce2比较,沸点较高的是_____________(写分子式)。
第一电离能:h______i;电负性:g______b(填“>”、“<”或“=”)。
下列关于元素在元素周期表中的位置以及元素原子的外围电子排布特点的有关叙正确是 。
A.j位于元素周期表中第四周期、ⅠB族,属于ds区元素
B.d的基态原子中,2p能级为半充满,属于p区元素
C.最外层电子排布式为4s1,一定属于ⅠA族
D.最外层电子排布式为ns2np1,该元素可能是ⅢA族或ⅢB族
将氨水滴入到j的硫酸盐溶液中,先产生蓝色沉淀,然后沉淀逐渐溶解并得到深蓝色溶液,显深蓝色的离子是____________________,写出蓝色沉淀溶解在氨水中的离子方程式______________________________________________________________________。
j的金属晶体的晶胞如图所示,则一个晶胞中j原子的个数是_______个。

查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z和W的原子序数依次增大。X原子的最外层电子数是内层电子数的2倍,Y与X同主族,Z和W原子中未成对电子数之比为2∶1。下列说法错误的是( )
A.XW4为非极性分子
B.Y、Z、W的最高价氧化物的水化物酸性强弱顺序是Y<Z<W
C.X、Y的最高价氧化物由固态转化为气态时,克服相同的作用力
D.XW4、YW4、ZW2分子中的中心原子均为sp3杂化
查看答案和解析>>
科目: 来源: 题型:
短周期主族元素A、B形成AB3型分子,下列有关叙述正确的是( )
A.若A、B为同一周期元素,则AB3分子一定为平面正三角形
B.若AB3分子中的价电子个数为24个,则AB3分子为平面正三角形
C.若为A、B为同一主族元素,,则AB3分子一定为三角锥形
D.若AB3分子为三角锥形,则AB3分子一定为NH3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com