
科目: 来源: 题型:
【题目】如下图是甲、乙两物质的溶解度曲线,下列说法正确的是
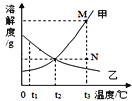
A. 两种物质的溶解度大小顺序为甲﹥乙
B. 若要将M点的甲溶液转变为N点的甲溶液,降温即可
C. 分别将甲、乙的饱和溶液从t3℃降温至t2℃时,所得溶液溶质质量分数大小关系是甲﹥乙
D. t3℃时,将甲、乙的饱和溶液各蒸发50g水,析出晶体质量甲﹥乙
查看答案和解析>>
科目: 来源: 题型:
【题目】(6分)某校同学开展了如下“溶液酸碱性的检验”的实验活动:
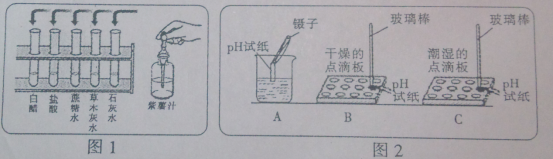
(1)把自制的紫色紫薯汁按图1所示分别滴加到试管中,观察到的现象如下表所示:
溶液 | 白醋 | 盐酸 | 蔗糖水 | 草木灰水 | 石灰水 |
加入紫薯汁后的颜色 | 红色 | 红色 | 紫色 | 绿色 | 绿色 |
①图1中存放紫薯汁的仪器名称 ;
②据上表推测,紫薯汁能做酸碱指示剂,遇到稀硫酸溶液可能显示的颜色是 ;
(2)用PH试纸测定图1中部分溶液的酸碱度:草木灰水pH>7,属于 (填“酸性”“中性”或“碱性”)溶液,白醋pH (填“>””<”或”=”)7;
(3)图2是三位同学分别测定土壤酸碱度的操作示意图,其中正确的是 (填“A”“B”或“C”,下同),可能导致北侧溶液pH数值发生改变的错误操作是 。
查看答案和解析>>
科目: 来源: 题型:
【题目】向盛有稀硫酸的小烧杯中慢慢滴加10%的Ba(OH)2溶液至过量,有关量的变化情况见下图(横坐标表示氢氧化钡溶液的质量,纵坐标表示小烧杯中量的变化)。其中错误的是( )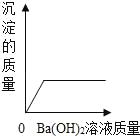
A. A B. B C. C D. D
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组探究盐酸和氢氧化钠反应过程中溶液pH的变化规律,得到如图所示曲线.下列有关该实验事实的说法正确的是( )
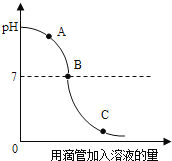
A.该实验是将氢氧化钠溶液滴入盐酸中
B.B点表示盐酸和氢氧化钠恰好完全反应
C.A点时的溶液能使酚酞试液变红
D.C点时,溶液中的溶质只有氯化钠
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙、丙三位同学为一家化工厂的污水设计排污方案。请你就他们的探究过程回答有关问题。
Ⅰ.首先用pH试纸检测污水的酸碱性。三位同学分别进行如下实验:
甲:取pH试纸于玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上,测得pH<7。
乙:取pH试纸于玻璃片上,先用蒸馏水润湿,再用玻璃棒蘸取待测液滴到pH试纸上,测得pH<7。
丙:取pH试纸直接浸入待测液中,测得pH<7。
(1)三位同学的操作正确的是________,该污水显________。
Ⅱ.利用中和反应原理测定污水中污染物(盐酸)的质量分数。甲、乙两位同学设计的实验方案图示如下:
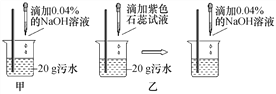
(2)甲同学取少量反应后的溶液于试管中,滴加几滴无色酚酞试液,酚酞试液变红,于是得出“两种物质已恰好中和”的结论。你认为他的结论是否正确?________,理由是_________。
(3)当乙同学观察到_________现象时即恰好完全反应。若此时消耗NaOH溶液2 g,则污水中HCl的质量分数为________。
(4)实验过程中,NaOH溶液必须用胶头滴管逐滴加入,且要用玻璃棒不断搅拌,目的是_________。丙同学利用接在传感器上的计算机绘制出了如下图所示的pH随所加的NaOH溶液体积变化的曲线,从曲线上可知污水的pH=______,M点表示的含义是__________。

(5)除去污水中的盐酸,你建议选用的原料是________。
A.NaOH B.Ca(OH)2 C.CuO D.Fe
查看答案和解析>>
科目: 来源: 题型:
【题目】实验室模拟炼铁的实验装置如下图所示。
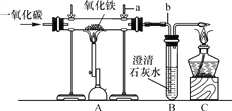
试回答下列问题:
(1)写出有标号仪器的名称:a.________,b.________。
(2)实验中看到的实验现象为:玻璃管中的粉末_________;试管里的澄清石灰水____________。
(3)玻璃管中反应的化学方程式为__________________。
(4)加热氧化铁之前,先通一会儿一氧化碳的作用是______________。
(5)该实验设计装置C的目的是______________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】某同学用下图装置进行CO与Fe2O3的反应。下列说法错误的是

A.该实验装置应增加尾气处理装置
B.加热前应先通入一段时间的CO以排尽装置内的空气
C.NaOH溶液应改为Ca(OH)2溶液以检验产生的CO2气体
D.反应后的固体是Fe和Fe2O3的混合物,可以采用加入盐酸并过滤的方法得到Fe
查看答案和解析>>
科目: 来源: 题型:
【题目】分析处理图表的信息是学习化学的一种重要方法。下表是氯化钠和碳酸钠在不同温度时的溶解度,根据此表回答:
温度/℃ | 10 | 20 | 30 | 40 | |
溶解度/g | 氯化钠 | 35.8 | 36.0 | 36.3 | 36.6 |
碳酸钠 | 12.2 | 21.8 | 39.7 | 53.2 | |
(1)40 ℃时,氯化钠的溶解度为________g。
(2)碳酸钠的溶解度随温度的升高而________(填“增大”或“减小”)。在20 ℃时,在100 g的水中加入30 g碳酸钠,充分搅拌后得到的是________(填“饱和溶液”或“不饱和溶液”),将上述溶液升温到30 ℃,该溶液的溶质质量分数为________(计算结果精确到0.1%)。
(3)10 ℃时,分别配制表中两种物质的饱和溶液,其中溶质质量分数较小的物质是________________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】氯化铵在部分温度下的溶解度见下表,下列说法正确的是( )
温度/℃ | 20 | 40 | 60 | 80 |
溶解度/g | 40 | 50 | 58 | 68 |
A. 20 ℃时,氯化铵饱和溶液中氯化铵的质量分数是25%
B. 20 ℃时,70 g氯化铵的饱和溶液升温至40 ℃后得到的是不饱和溶液
C. 40 ℃时,75 g氯化铵的饱和溶液加入25 g水后氯化铵的质量分数为30%
D. 80 ℃时,84 g氯化铵饱和溶液降温至60 ℃时有10 g氯化铵析出
查看答案和解析>>
科目: 来源: 题型:
【题目】小张同学用某固体物质进行如图所示的实验,根据实验判断下列说法不正确的是( )
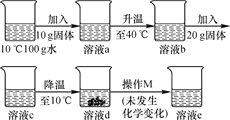
A. 该固体物质的溶解度随温度的升高而增大
B. 溶液b一定是不饱和溶液
C. 溶液d中溶质质量一定大于溶液e中的溶质质量
D. 溶液d和溶液e的溶质质量分数可能相同
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com