

科目: 来源: 题型:
下列条件下两瓶气体所含原子数一定相等的是( )
A.同质量、不同密度的N2和CO B.同温度、同体积的H2和N2
C.同压强、同密度的C2H4和C3H6 D.同压强、同体积的N2和CO2
查看答案和解析>>
科目: 来源: 题型:
下列各组物质相互反应,无论哪种过量,都可用同一个离子方程式表示的是( )
A.偏铝酸钾溶液和盐酸 B.氨水和硝酸银溶液
C.二氧化硫和氢氧化钠溶液 D.碳酸氢钠溶液和盐酸
查看答案和解析>>
科目: 来源: 题型:
下列有关生活中的化学叙述正确的是( )
A.双氧水可在医疗上作消毒杀菌剂
B.提倡使用乙醇汽油主要是为了提高汽油的燃烧效率
C.纤维素和蛋白质水解的最终产物均为葡萄糖
D.变质的油脂难闻的特殊气味,是由于油脂发生了水解反应
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F、C、H均为含有苯环的有机物。B与PeCl3溶液混合没有颜色变化,F、H除苯环外还有一个含有氧的六元环(该六元环与苯环共用2个碳原子)。
它们之间的转化关系如下:

(1)除苯环外,化合物A还含有的官能团是_____。
(2)物质D不可能具有的性质是_____ (填写字母)。
A.使溴水褪色 B.使酸性KMnO4溶液褪色
C.能与Na2CO3溶液反应
D.能发生酯化反应
E.能与新制的Cu(0H) 2反应 F.能使PeCl3溶液变色
(3)写出反应①的化学方程式____。
(4)写出同时符合下列两项要求的C的两种同分异构体的结构简式
①化合物是1,3,5一三取代苯
②苯环上的三个取代基中必须含有醇羟基、酚羟基和醛基这三种结构_____。
查看答案和解析>>
科目: 来源: 题型:
已知:表I是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
表I

表Ⅱ是一些气态基态原子的第一、二、三、四级电离能(kJ?mol-1):
表Ⅱ
| 锂 | X | Y | |
| 第一电离能 | 519 | 502 | 580 |
| 第二电离能 | 7296 | 4570 | 1820 |
| 第三电离能 | 11799 | 6920 | 2750 |
| 第四电离能 | 9550 | 11600 |
请根据上述信息,回答下列问题:
(1)为什么锂原子失去核外第二个电子时所需的能量要远远大于失去第一个电子所需的能量_____。
(2)表中Y可能为以上13种元素中的_____ (填写字母)元素。用元素符号表示 X和j形成的化学键种类最多的一种化合物的化学式_____。
(3)根据构造原理,用电子排布式表示e的特征电子构型_____。
(4)以上13种元素中,_____ (填写字母)元素原子失去核外第一个电子需要的能量最多。
(5)i元素另一元素形成的化合物其晶体有两种结构,其中一种结构与金刚石相似,该结构的晶体属_____晶体,若使其熔化,需破坏的作用力为_____。
查看答案和解析>>
科目: 来源: 题型:
烧碱和氯气都是重要的基本化工原料,它们大多来自氯碱工业,氯碱工业的工艺流程如下图所示:
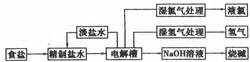
(1)电解饱和食盐水的总反应方程式为______,阳极发生的电极反应为_______。
(2)工业生产用的食盐水进入电解槽之前需精制,请简要说明需要精制的原因。
(3)目前氯碱工业主要采用的方法有三种,它们各有特点(见表)。
| 方法 | 电解槽特点 | 产品中氯 化钠含量 | 电解液中氢 氧化钠含量 | 总能耗 (kW.h?t-1) | 其他 |
| 隔膜法 | 使用石棉纤维制成的隔膜隔开阴阳极 | 较大 | 低 | 高 | 细微石棉吸入人的肺内有损健康,目前正被离子膜交换法取代 |
| 汞法 | 由独立的电解室和解汞室构成,氯气和氢气在不同的室产生 | 低 | 很高 | 高 | 汞易对环境造成污染,在我国已经被淘汰 |
| 离子交换膜法 | 使用能选择性通过离子的离子膜替代隔膜法中石棉隔膜 | 很低 | 较高 | 低 | 占地少、生产能力大、能连续生产,是氯碱工业的发展方向 |
请比较三种方法的优缺点,指出哪些方面的主要因素不断促进着电解槽革新。
(4)氯碱化工厂的选址比较特殊,如通常不会单独建氯碱化工厂,而是与农药厂、有机化工、制药厂、盐酸厂等建在一起,请分析这种建厂方式的原因和所带来的好处
查看答案和解析>>
科目: 来源: 题型:
已知可逆反应:![]()
请回答下列问题:
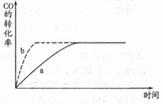
(1)图中曲线a表示反应进行过程中CO的转化率随时间变化的关系,若要改变起始条件,使反应过程按b曲线进行,可采取的措施是_____ (填序号)
A.升高温度 B.加催化剂 C.加压 D.增加CO的用量 E.扩大容器的体积
(2)830K时,若起始时c(CO)=2m01.L-1,c(H20)=3m01.L-1,经5min后该反应达到平衡,此时CO的转化率为60%,该时间段内,此反应的平均速率v(CO)=____;若起始时,c(CO)=4m01.L-1,c(H2O)____,达到平衡时,反应体系中各组分的百分含量与上述情况相同,此时该反应的化学平衡常数为___。
(3)830K时,若起始时,c(CO)=2m01.L-1,c(H2O)=6m01.L-1,达到化学平衡后,水蒸气的转化率为____。
(4)TK时,起始浓度为:c(CO)=am01.L-1,c(H2O)=bm01.L-1,达到化学平衡后,c(H2)=cm01.L-1;若a、b、c之间的关系满足:ab>(a+b)?c,则此时T____830。(填“大于”“等于”或“小于”)
查看答案和解析>>
科目: 来源: 题型:
A、B、C、D、E、F六种短周期主族元素,其核电荷数依次增大,已知元素A和C可形成两种常温下均为液体的化合物,B原子最外层电子数是最内层电子数的两倍,A与D、C与F分别处于同一主族且A、D质子数之和是C、F质子数之和的一半,18gE与足量盐酸反应生成标准状况下的H222.4L。
请按要求回答:
(1)由A、C、D三种元素形成的化合物X中含有的化学键类型为_______。
(2)A、D、F三种元素形成的化合物Y溶液中的微粒浓度之间存在如下关系(请填写下式中的空白,每空只填一种微粒浓度的符号)。
c(H+)+_______:c(OH―)+ _______。
(3)E、F构成的化合物能与水反应,写出化学方程式_______。
(4)①写出单质D与乙醇反应的化学方程式_______。
②A、B、C三种元素可以形成最简式为A4B2C的有机物,该有机物与足量X水溶液反应得到的两种产物中含有相同数目的B原子。写出该反应的化学方程式_____。
(5)A和B组成的化合物M,每个分子中含有18个电子,常温常压下,0.5molM完全燃烧放出780kJ的热量,请写出表示M完全燃烧的热化学方程式____。
查看答案和解析>>
科目: 来源: 题型:
I.下图是一个制取氯气并以氯气为原料进行特定反应的装置。
试回答下列问题:
(1)实验开始时,先点燃A处的酒精灯,打开旋塞K,让![]() 充满整个装置,再点燃D处的酒精灯,连接上E装置,
充满整个装置,再点燃D处的酒精灯,连接上E装置,![]() 通过C瓶后进入D,D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为
通过C瓶后进入D,D装置的硬质玻璃管内盛有炭粉,发生氧化还原反应,其产物为![]() 和HCl,试写出D中发生反应的化学方程式_______,装置C的作用是_______。
和HCl,试写出D中发生反应的化学方程式_______,装置C的作用是_______。
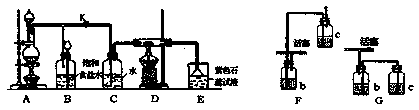
(2)在E处石蕊试液由紫色变为红色,再变为五色,其原因是_______。
(3)若将E处烧杯中的溶液改为澄清石灰水,反应过程中的现象为_______。
(选填序号)
A.有白色沉淀生成 B.无明显现象 C.首先生成白色沉淀而后白色沉淀消失
(4)在选取试剂正确且适量前提下,反应开始后当关闭活塞K时,发现B的长颈漏斗中的液面上升不明显,你认为可能的原因是_______,证实该原因的操作方法是_______。
(5)把制得的足量![]() 通到
通到![]() 溶液时反应的离子方程式为_______。
溶液时反应的离子方程式为_______。
Ⅱ.若采用A、B,用![]() ,固体与体积比浓度为1:1的硫酸制取
,固体与体积比浓度为1:1的硫酸制取![]() 气体。
气体。
(1)此时,B中的液体一般应选用_______。
(2)用F或C代替B部分是否可行?若不可行,简要说明理由。_______。
Ⅲ.若将![]() 和
和![]() 分别通人滴有酚酞的NaOH溶液中,红色均褪去。请你设计一个实验,说明
分别通人滴有酚酞的NaOH溶液中,红色均褪去。请你设计一个实验,说明![]() 和
和![]() 使该溶液褪色的原理是不同的。
使该溶液褪色的原理是不同的。
查看答案和解析>>
科目: 来源: 题型:
关于下列装置图的叙述中,不正确的是 ( )
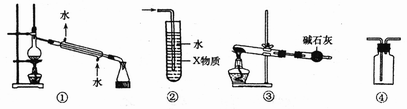
A.装置①常用于分离沸点差别较大,且互相溶解的液体混合物
B.装置②中X若为四氯化碳,可用此装置吸收![]() 或HCl,并防止发生倒吸
或HCl,并防止发生倒吸
C.以![]() 为原料,在实验室中可用装置③制备少量
为原料,在实验室中可用装置③制备少量![]()
D.装置④可用于收集![]() 等气体
等气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com