
科目: 来源: 题型:
下列判断错误的是
A.稳定性:NH3>PH3>AsH3
B.原子半径:N>P>As
C.酸性:HClO4>H2SO4>H3PO4
D.碱性:NaOH>Mg(OH)![]() 2>Al(OH)3
2>Al(OH)3
查看答案和解析>>
科目: 来源: 题型:
实验题:(8分)增加反应物浓度可以加快化学反应速率。已知:反应Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O出现浑浊的快慢与浓度有关。现有0.1mol/L的Na2S2O3溶液和0.1mol/L的H2SO4溶液和蒸馏水;实验用品有:烧杯、试管、量筒、胶头滴管、秒表等,请设计一个实验通过较明显的实验事实证明上述结论(说明实验操作、现象及结论)。
查看答案和解析>>
科目: 来源: 题型:
830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g)![]() CO2(g)+H2(g) △H<0
CO2(g)+H2(g) △H<0
试回答下列问题:
(1)若起始时c(CO)=2 mol·L-1,c(H2O)=3 mol·L-1,达到平衡时CO的转化率为60%,则在该温度下,该反应的平衡常数K= .
(2)在相同温度下,若起始时c(CO)=1 mol·L-1,c(H2O)=2 mol·L-1,反应进行一段时间后,测得H2的浓度为0.5 mol·L-1,则此时该反应是否达到平衡状态 (填“是”与“否”),此时v(正) v(逆)(填“大于”“小于”或“等于”),你判断的依据是
(3)若降低温度,该反应的K值将 ,该反应的化学反应速率将 (均填“增大”“减小”或“不变”)。
查看答案和解析>>
科目: 来源: 题型:
在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系.
Cr2O72-+H2O![]() 2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
2CrO42-+2H+,把K2Cr2O7溶于水配成稀溶液是橙色。
(1)向上述溶液中加入NaOH溶液,溶液呈 色,因为 。
(2)向已加入NaOH溶液的(1)中再加入过量稀H2SO4,则溶液呈 色,
因为 。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡 ,溶液颜色将 。
查看答案和解析>>
科目: 来源: 题型:
(1)化学反应可视为旧键断裂和新键形成的过程。化学键的键能是形成(或拆开)1 mol化学键时释放(或吸收)的能量。已知:N≡N键的键能是948.9kJ·mol-1,H-H键的键能是436.0 kJ·mol-1;由N2和H2合成1molNH3时可放出46.2kJ的热量。
根据上述数据可计算:N-H键的键能是 。
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8 kJ·mol-1
3Fe2O3(s)+ CO(g)==2Fe3O4(s)+ CO2(g) △H=-47.2 kJ·mol-1
Fe3O4(s)+CO(g)==3FeO(s)+CO2(g) △H=+640.5 kJ·mol-1
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
_________________ 。
查看答案和解析>>
科目: 来源: 题型:
化学能和电能的相互转化,是能量转化的重要方式之一,右图两个实验装置是实现化学能和电能相互转化的装置。

(1)把化学能转化为电能的装置是 (填“甲”或“乙”);
(2)④电极上的电极反应式为
(3)①电极上的电极反应式为 ,
检验该电极反应产物的方法是
(4)写出装置甲的反应总化学方程式 。
查看答案和解析>>
科目: 来源: 题型:
二氧化氮存在下列平衡:2NO2 ![]() N2O4(g) ;△H<0,在测定NO2 的相对分子质量时,下列条件较为适宜的是
N2O4(g) ;△H<0,在测定NO2 的相对分子质量时,下列条件较为适宜的是
A、温度130℃、压强3.03×105Pa B.温度25℃、压强1.01×105Pa
C、 温度0℃、压强5.05×104Pa D、 温度130℃、压强5.05×104Pa
查看答案和解析>>
科目: 来源: 题型:
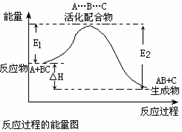
某反应过程中体系的能量变化如图所示,下列说法错误的是
A、反应过程可表示为 A+BC—→[A…B…C] —→AB+C
(反应物)(过渡态) (产物)
B、此图中逆反应的热效应△H=E1—E2,为吸热反应
C、正反应的热效应为△H=E1—E2,且E2>E1,所以正反应为放热反应
D、E1为反应物的平均能量与过渡态的能量差,称为正反应的活化能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com