
科目: 来源: 题型:
如图是可逆反应A+2B![]() 2C+3D的化学反应速率与
2C+3D的化学反应速率与![]() 化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断
化学平衡随外界条件改变(先降温后加压)而变化的情况,由此可推断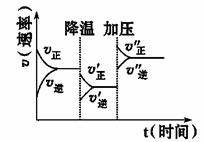
A.正反应是吸热反应
B.若A、B是气体,则D是液体或固体
C.逆反应是放热反应
D.A、B、C、D均为气体
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是:
A. 对于反应CO(g)+H2O(g) ![]() CO2(g)+H2(g),增大气体压强,反应物活化分子百分数增加
CO2(g)+H2(g),增大气体压强,反应物活化分子百分数增加
B. 对于平衡CO(g)+H2O(g) ![]() CO2(g)+H2(g),增大反应物浓度,平衡正向移动,平衡常数增大
CO2(g)+H2(g),增大反应物浓度,平衡正向移动,平衡常数增大
C. 对于平衡CO(g)+H2O(g) ![]() CO2(g)+H2(g),平衡常数
CO2(g)+H2(g),平衡常数
D.以上说法均不正确。
查看答案和解析>>
科目: 来源: 题型:
强酸与强碱的稀溶液发生中和反应的热效应为H+(aq)+OH-(aq)==H2O(l) ΔH=-57.3 kJ·mol-1。实验中因为下列措施使求得的中和热数值变大的是
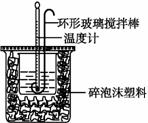
A. 烧杯间填满金属碎末
B. 大烧杯上不盖硬纸板
C. 用相同浓度和体积的氨水代替NaOH溶液进行实验
D.用浓硫酸代替稀盐酸
查看答案和解析>>
科目: 来源: 题型:
图甲A、B两容器里,分别收集着两种互不作用的理想气体。若将中间活塞打开(如图乙),两种气体分子立即都分布在两个容器中。这是一个不伴随能量变化的自发过程。关于此过程的下列说法不正确的是
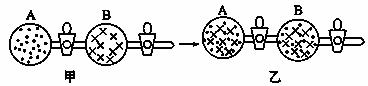
A.此过程为混乱程度小的向混乱程度大的方向的变化过程,即熵增大的过程
B.此过程为自发过程,而且没有热量的吸收或放出
C.此过程从有序到无序,混乱度增大
D.此过程是自发可逆的
查看答案和解析>>
科目: 来源: 题型:
室温下,溶液的pH可能大于7的是
A. 0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液等体积混合
B. 存在醋酸分子的溶液
C. pH=4的醋酸溶液和pH=10的氢氧化钠溶液混合后溶液中c(Ac-) =c(Na+)
D. pH=4的盐酸和pH=l0的氨水混合后溶液中c(Cl-) >c(NH4+)
查看答案和解析>>
科目: 来源: 题型:
减小压强时,对已达到化学平衡的反应2X(g)+Y(g) ![]() 2Z(g)产生的影响是
2Z(g)产生的影响是
A.逆反应速率增大,正反应速率减小,平衡向逆反应方向移动
B.逆反应速率减小,正反应速率增大,平衡向正反应方向移动
C.正、逆反应速率都减小,平衡向逆反应方向移动
D.正、逆反应速率都增大,平衡向正反应方向移动
查看答案和解析>>
科目: 来源: 题型:
下列叙述正确的是
A.用惰性电极电解滴有紫色石蕊试液的饱和食盐水,阴极区附近溶液先变红
B.镀锌的铁制品,镀层部分受损后,露出的铁表面易被腐蚀
C.用惰性电极电解CuSO4溶液,在电解后溶液中加Cu(OH)2固体能使CuSO4溶液恢复到电解前浓度
D.配置FeCl3时,可先将其溶解在盐酸中,再用蒸馏水稀释
查看答案和解析>>
科目: 来源: 题型:
据报道,全球每年因发生金属腐蚀而造成的直接经济损失达数千亿美元。下列各电极反应式中,能表示铁的电化学腐蚀的是
①Fe-2e-==Fe2+ ②2H++2e-==H2↑ ③Fe-3e-==Fe3+
④2H2O+O2+4e-==4OH- ⑤4OH--4e-==2H2O+O2↑
A.①②⑤ B.②③④ C.①②④ D.①③⑤
查看答案和解析>>
科目: 来源: 题型:
下列有关化学反应速率的说法正确的是
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B.100 mL 2 mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.SO2的催化氧化是一个放热的反应,所以升高温度,反应速率减慢
D.汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率减慢
查看答案和解析>>
科目: 来源: 题型:
下列事实中,不能用勒沙特列原理解释的是
A.开启啤酒瓶后,瓶中立刻泛起大量泡沫 B.在FeSO4溶液中加入少量铁粉
C.实验室中常用排饱和食盐水的方法收集Cl2 D.加热纯碱溶液,其去污能力增强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com