
科目: 来源: 题型:
将磁性氧化铁放入稀HNO3中发生反应:
3Fe3O4+ 28HNO3=9Fe(NO3)x+ NO↑+14H2O 。下列判断合理的是 ( )
A.Fe(NO3)x中的x为2
B.反应中每生成0.2 mol 还原产物,就有0.6 mol 电子转移
C.稀HNO3 在反应中只作氧化剂
D.磁性氧化铁中的铁元素全部被氧化
查看答案和解析>>
科目: 来源: 题型:
三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体。它无色、无臭,在潮湿的空气中能发生下列反应:3NF3+5H2O=2NO+HNO3+9HF, 下列有关说法正确的是( )
A.反应中NF3是氧化剂,H2O是还原剂
B.NF3在潮湿空气中泄漏会产生白雾、红棕色气体等现象
C.若反应中生成0.2mol HNO3,则反应共转移0.2mol e-
D.反应中被氧化与被还原的原子物质的量之比为2:1
查看答案和解析>>
科目: 来源: 题型:
二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如右下图所示。常温下,S2Cl2遇水易反应,并产生能使品红褪色的气体。下列说法一定错误的是( )
A.S2Cl2与H2O反应的化学方程式可能为:
2S2Cl2+2H2O=SO2↑+3S↓+4HCl
B.S2Cl2中含有极性键和非极性键
C.S2Br2与S2Cl2结构相似,熔沸点:S2Br2>S2Cl2
D.S2Cl2的电子式为:![]()

查看答案和解析>>
科目: 来源: 题型:
在BaCl2溶液中通入SO2气体,溶液仍澄清;若将BaCl2溶液分盛到两支试管中,其中一支加入硝酸,另一支加入烧碱溶液,然后再通入SO2气体,结果两支试管都有白色沉淀生成。由此得出下列结论合理的是:①氯化钡有两性 ②两支试管中生成的白色沉淀均是亚硫酸钡 ③SO2有还原性和溶于水显酸性 ④烧碱溶液使SO2水溶液中SO32-的浓度增大 ( )
A.①② B.②③ C.③④ D.①④
查看答案和解析>>
科目: 来源: 题型:
四支试管分别充满O2、NO2、C12、NH3四种气体,把它们分别倒立于盛有下列各种液体的水槽中,发生的现象如下图所示,其中充满C12的试管是 ( )
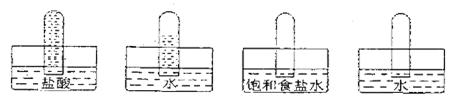
A B C D
查看答案和解析>>
科目: 来源: 题型:
如图所示,在注射器中加入少量Na2SO3晶体,并吸入少量浓硫酸(以不接触纸条为准),则下列有关说法不正确的是 ( )

A.蓝色石蕊试纸变红后不褪色
B.NaOH溶液可用于除去实验中多余的SO2
C.湿润KI-淀粉试纸未变蓝,说明SO2的氧化性弱于I2
D.品红试纸、沾有KMnO4溶液的滤纸均褪色,才证明了SO2有漂白性
查看答案和解析>>
科目: 来源: 题型:
能正确表示下列反应的离子方程式是 ( )
A.向Fe(NO3)2稀溶液中加入盐酸: 3Fe2++4H++NO===3Fe3++NO↑+2H2O
B.铜片与浓HNO3: Cu+NO+4H+===Cu2++NO↑+2H2O
C.碳酸氢铵溶液与足量的NaOH溶液混合后加热: NH+OH-NH3↑+H2O
D.AlCl3溶液中滴加足量氨水: Al3++4NH3·H2O===AlO+4NH+2H2O
查看答案和解析>>
科目: 来源: 题型:
几种短周期元素的原子半径及某些化合价见下表。分析判断下列说法正确的是( )
| 元素代号 | A | B | D | E | G | I | J | K |
| 化合价 | –1 | –2 | +4、–4 | –1 | +5、–3 | +3 | +2 | +1 |
| 原子半径/nm | 0.071 | 0.074 | 0.077 | 0.099 | 0.110 | 0.143 | 0.160 | 0.186 |
A.A的单质能将E单质从IE的溶液中置换出来
B.A、I、J的离子半径由大到小顺序是A>J>I
C.G元素的单质不存在同素异形体
D.J在DB2中燃烧生成两种化合物
查看答案和解析>>
科目: 来源: 题型:
有一瓶Na2SO3溶液,由于它可能部分被氧化,某同学进行如下实验:取少量溶液,滴
入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。
对此实验下述结论正确的是 ( )
A.Na2SO3已部分被空气中的氧气氧化
B.加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4
C.此实验不能确定Na2SO3是否部分被氧化
D.加硝酸后的不溶沉淀一定是BaSO3ks5u
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com