
科目: 来源: 题型:
三氧化二铁和氧化亚铜都是红色粉末,常用作颜料。某校一化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料
Cu2O溶于稀硫酸生成Cu和CuSO4, 在空气中加热生成CuO
提出假设
假设1:红色粉末是Fe2O3
假设2:红色粉末是Cu2O
假设3:红色粉末是Fe2O3、Cu2O的混合物
设计探究实验
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 试剂。
(1)若假设1成立,则实验现象是 。
(2)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁你认为这种说法合理吗? 。(填“合理” 或 “不合理” )
(3)若固体粉末完全溶解无固体存在 , 滴加 KSCN 试剂时溶液不变红色 , 则证明原固体粉末是 ,写出发生的离子反应方程式 ;
; 。
探究延伸
(4)若经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg( b > a),则混合物中Cu2O的质量分数为 。
查看答案和解析>>
科目: 来源: 题型:
某混合物A,含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下
图所示的物质之间的变化:
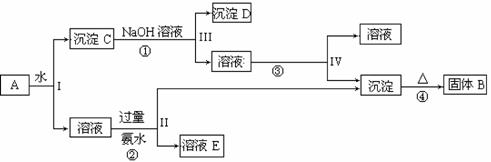 |
据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是 。
(2)根据上述框图反应关系,写出B、D所含物质的化学式。固体B ;
沉淀D 。
(3)试剂③是 (填化学式)
(4)写出①的化学反应方程式 ;
②的离子反应方程式 。
查看答案和解析>>
科目: 来源: 题型:
某待测液中可能含有Ag+、Fe3+、K+、Ba2+、SiO32-、NO3-、 CO32-等离子,进行如下实验:
①加入过量稀盐酸,有白色沉淀生成。
②过滤,在滤液中加入过量的稀硫酸,又有白色沉淀生成。
③过滤,取少量滤液,滴入2滴KSCN溶液,没有明显的现象出现。
根据实验现象回答:
(1)待测液中一定含有 离子,一定不含有 离子;(2)步骤②发生反应的离子方程式为 ;
(3)不能确定是否存在的离子是 ,要检验该离子是否存在的实验方法是 。
查看答案和解析>>
科目: 来源: 题型:
配制物质的量浓度为0.2 mol/L的NaOH溶液500 mL,填空并请回答下列问题:
(1)填写①②对应的问题
| 应称量NaOH的质量/g | 已给仪器 | 除已给仪器外还需要的玻璃仪器 |
| ① | 烧杯、量筒、胶头滴管、500 mL容量瓶 | ② |
(2)下列操作中,容量瓶所具备的功能有________(填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.用来加热溶解固体溶质
(3)下列操作对配制的NaOH溶液浓度有偏高影响的是________。
A.称量NaOH固体时,露置在空气的时间过长
B.选用的容量瓶内有少量的蒸馏水
C.在烧杯中溶解NaOH后,立即将所得溶液注入容量瓶中
D.在定容时仰视容量瓶刻度线
查看答案和解析>>
科目: 来源: 题型:
实验室制备Cl2的反应原理为:MnO2+ 4HCl(浓) MnCl2+Cl2↑+2H2O
(1)当标准状况下生成11.2L氯气时转移电子的物质的量为 。
(2)在此反应中氧化产物是 ,氧化剂与还原剂的物质的量的比
为 。
(3)比较氧化性Cl2 MnO2 (填 >、 < 或 = )
查看答案和解析>>
科目: 来源: 题型:
将一定质量的镁和铝混合物投入200 mL硫酸中,固体全部溶解后,向所得溶液中加
入NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V的变化如下图所
示。则下列说法不正确的是
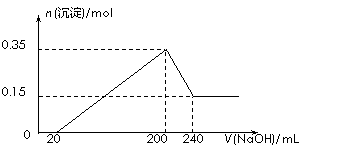 |
B.最初20 mLNaOH溶液用于中和过量的硫酸
C.硫酸的物质的量浓度为2.5 mol·L–1
D.生成的氢气在标准状况下的体积为11.2 L
查看答案和解析>>
科目: 来源: 题型:
下列离子方程式书写正确的是
A.铝粉投入到NaOH溶液中:2Al+2OH-══ 2AlO2-+H2↑
B.AlCl3溶液中加入足量的氨水:Al3++ 3OH- ══ Al(OH)3↓
C.三氯化铁溶液中加入铁粉:![]()
D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl-
查看答案和解析>>
科目: 来源: 题型:
24 mL 浓度为0.05 mol / L的Na2SO3溶液恰好与20 mL 浓度为0.02 mol / L的K2Cr2O7溶液完全反应。已知Na2SO3被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价是
A.+1 B. +2 C.+3 D.+4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com