
科目: 来源: 题型:
下列哪个选项不能说明金属A比金属B活泼 ( )
A.A常温下可以与水反应,B不与水反应
B.B不能从任何含A的盐中置换出金属A
C.用氨水可以制取B对应的碱,却不能制取A对应的碱
D.A在空气中比B耐腐蚀
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是 ( )
A.原子的最外层电子数相同的元素,一定属于同一族
B.元素周期表中元素排序的依据是原子的核电荷数
C.简单离子的核电荷数与最外电子层上的电子数不可能相等
D.电子层数相同的粒子,对应元素一定属于同一周期
查看答案和解析>>
科目: 来源: 题型:
在一定温度下的定容密闭容器中,发生反应:A(s)+2B(g)![]() C(g)+D(g),当下列物理量不再变化时,并不能表明反应已达平衡的是 ( )
C(g)+D(g),当下列物理量不再变化时,并不能表明反应已达平衡的是 ( )
A.混合气体的压强 B.混合气体的密度
C.混合气体的平均相对分子质量 D. B的物质的量浓度
查看答案和解析>>
科目: 来源: 题型:
下列变化中属于吸热反应的是 ( )
①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④氯酸钾分解制氧气
⑤生石灰跟水反应生成熟石灰
A.①②③④ B.②④⑤ C.①②④ D.②④
查看答案和解析>>
科目: 来源: 题型:
下面是四个化学反应,你认为理论上不可用于设计成原电池的化学反应是 ( )
A.2Al+2NaOH+2H2O===2NaAlO2+3H2↑ B.2H2+O2===2H2O
C.Mg3N2+6H2O===3Mg(OH)2+2NH3↑ D.CH4+2O2===CO2+2H2O
查看答案和解析>>
科目: 来源: 题型:
如下图所示的“能源分类相关图”中,全部符合图中阴影部分能源选项的是 ( )

A.煤炭、石油、沼气
B.水能、潮汐能、天然气
C.太阳能、风能、生物能
D.地热能、海洋能、核能
查看答案和解析>>
科目: 来源: 题型:
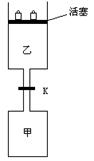 如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+2B(g)
如图所示,当关闭阀门K时,向甲中充入1.5 mol A、3.5 mol B,向乙中充入3 mol A、7 mol B,起始时,甲、乙体积均为V L。在相同温度和有催化剂存在的条件下,两容器中各自发生下列反应:3A(g)+2B(g)![]() C(g)+2D(g);ΔH<0
C(g)+2D(g);ΔH<0
达到平衡(Ⅰ)时,V(乙)=0.86V L。请回答:
(1)乙中B的转化率为
(2)甲中D和乙中C的物质的量比较: (填“相等”、“前者大”、“后者大”);
(3)打开K,过一段时间重新达平衡(Ⅱ)时,乙的体积为 (用含V的代数式表示,连通管中气体体积忽略不计。)
查看答案和解析>>
科目: 来源: 题型:
食醋分为酿造醋和配制醋两种。国家标准规定酿造食醋总酸含量不得低于3.5g/100mL。
(1)某研究小组利用滴定分析法测定某品牌食醋中醋酸的含量,下列说法正确的是 。
a.用NaOH溶液滴定时反应的离子方程式为:H++OH-=H2O
b.食醋试样需稀释一定倍数后再进行滴定
c.用NaOH溶液滴定食醋,可使用酚酞或甲基橙作指示剂
d.若测得该品牌食醋的物质的量浓度为0.75mol·L-1,则该食醋的总酸量为4.5g/100mL。
(2)研究小组的同学仔细观察了该品牌食醋的标签,发现其中还含有苯甲酸钠作为食品添加剂,他想用资料法验证醋酸与食品添加剂(苯甲酸钠C6H5COONa)不会发生离子互换反应,需查找在一定温度下的醋酸与苯甲酸的 (填写序号)。
a.pH b.电离度 c.电离常数 d.溶解度
(3)常温下,用0.1000 mol·L-1NaOH溶液分别滴定20.00mL 0.1000 mol·L-1HCl溶液和20.00mL 0.1000 mol·L-1CH3COOH溶液,得到2条滴定曲线,如下图所示。
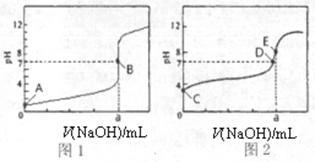
①滴定醋酸溶液的曲线是 (填“图l”或“图2”);滴定曲线中a= mL;
②E点pH>8的原因用离子方程式表示 。
(4)现欲粗略测定一未知浓度的CH3COOH溶液的电离度,应做的实验和所需的试剂(试纸)是 。
a.电解,NaOH溶液 b.蒸馏,Na2CO3溶液
c.酯化反应,石蕊试液 d.中和滴定,pH试纸
查看答案和解析>>
科目: 来源: 题型:
在温度T1和T2下,X2(g)和 H2反应生成HX的平衡常数如下表:
化学方程式 | K (T1 ) | K (T2) |
F2+H2 | 1.8 ×1036 | 1.9 ×1032 |
Cl2+H2 | 9.7 ×1012 | 4.2 ×1011 |
Br2+H2 | 5.6 ×107 | 9.3 ×106 |
I2+H2 | 43 | 34 |
(1)仅依据K的变化,可以推断出:随着卤素原子核电荷数的增加,_______(选填字母)
a.在相同条件下,X2的平衡转化率逐渐降低 b. X2与H2反应的剧烈程度逐渐减弱
c. HX的稳定性逐渐减弱 d. HX的还原性逐渐减弱
 (2)在容积为3L的密闭容器中,由I2(g)和H2(g)合成HI(g),在其他条件不变的情况下,研究温度对反应的影响,HI的物质的量的变化情况如下图所示。
(2)在容积为3L的密闭容器中,由I2(g)和H2(g)合成HI(g),在其他条件不变的情况下,研究温度对反应的影响,HI的物质的量的变化情况如下图所示。
①温度为T1时,在0~tAmin内,H2的消耗速率v (H2)=__________
②分析右图所示图像,下列说法正确的是________(填序号)
a.温度为T2,容器内气体密度不变时,反应到达B点所示状态
b.平衡状态从A点移动到B点,n(HI)/n(H2)增大
c.该反应为放热反应
(3)加水稀释0.1mol·L-1的HF溶液,下列各量中增大的是________(填序号)
a.c(H+) b. Ka(HF) c. c(F-)/c(H+) d. c(H+) / c(HF)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com