

科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
已知X、Y元素同周期,且电负性X>Y,下列说法错误的是
A.X与Y形成的化合物,X可以显负价,Y显正价
B.第一电离能可能Y小于X
C.最高价含氧酸的酸性:X对应的最高价含氧酸酸性弱于Y对应的最高价含氧酸的酸性
D.气态氢化物的稳定性:HmY小于HnX
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
在容积可变的密闭容器中存在如下反应:CO(g)+H2O(g)  CO2(g)+H2(g)
△H<0
CO2(g)+H2(g)
△H<0
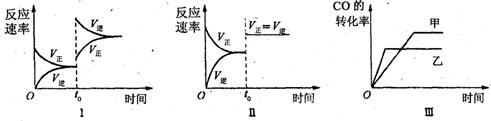
下列分析中不正确的是
A、图Ⅰ研究中的是t0时升高温度对反应速率的影响
B、图Ⅱ研究的是t0时增大压强(缩小体积)或使用催化剂对反应速率的影响
C、图Ⅲ研究的是催化剂对化学平衡的影响,且甲使用了催化剂
D、图Ⅲ研究的是温度对化学平衡的影响,且乙的温度较高
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
下列分子中的中心原子杂化轨道的类型相同的是
A、CO2和SO2 B、CH4 和NH3 C、BeCl2 和BF3 D、C2H4 和C2H2
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
T°C时,将体积为VAL、浓度为a mol/L的一元酸HA与体积为VBL、浓度为b mol/L的一元碱BOH混合,混合液恰好呈中性,则下列判断正确的是
A.混合液的pH=7 B.a=b
C.混合液中Kw=[c(H+)]2 D.a=b,VA=VB
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
下列说法中正确的是
A.乙烯中C=C的键能是乙烷中C-C的键能的2倍
B.氮气分子中含有1个s键和2个p键
C.N-O键的极性比C-O键的极性大
D.NH4+中4个N-H键的键能不相同
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
目前,人们正在研究开发一种高能电池---钠硫电池,它是以熔融的钠和硫为两极,以Na+
导电的β′—Al2O3陶瓷作固体电解质,反应式如下:Na2Sx 2Na+xS,以下说法正确的是
2Na+xS,以下说法正确的是
A、放电时,Na 作正极,S极发生还原反应
B、充电时钠极与外电源的正极相连
C、当用该电池电解AgNO3溶液时,阳极上产生标准状况下气体11.2L时,消耗金属钠2.3g
D、充电时,阳极发生的反应为:Sx2--2e— = xS
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
下列热化学方程式中,正确的是
A.甲烷的燃烧热ΔH=- 890.3 kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:
CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH=-890.3 kJ·mol-1
B.500 ℃、30 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为: N2(g)+3 H2(g) 2 NH3(g) ΔH = -38.6
kJ·mol-1
2 NH3(g) ΔH = -38.6
kJ·mol-1
C.HCl和NaOH反应的中和热ΔH= -57.3 kJ·mol-1,则H2SO4和Ca(OH)2反应的中和热ΔH=2×(-57.3)kJ·mol-1
D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2 H2(g)+O2(g)=2 H2O(l) ΔH= -571.6 kJ·mol-1
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
今有室温下四种溶液,有关叙述不正确的是
|
|
① |
② |
③ |
④ |
|
pH |
11 |
11 |
3 |
3 |
|
溶液 |
氨水 |
氢氧化钠溶液 |
醋酸 |
盐酸 |
A.①、②中分别加入适量的氯化铵晶体后,两溶液的pH均减小
B.分别加水稀释10倍,四种溶液的pH①>②>④>③
C.①、④两溶液等体积混合,所得溶液中c(Cl-)>c(NH4+)>c(OH-)>c(H+)
D.VaL④与VbL②溶液混合后,若混合后溶液pH=4,则Va∶Vb=11∶9
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:选择题
某物质的实验式为PtCl4·2NH3,其水溶液不导电,加入AgNO3溶液反应也不产生沉淀,以强碱处理并没有NH3放出,则关于此化合物的说法中正确的是
A.配合物中中心原子的电荷数和配位数均为6
B.该配合物可能是平面正方形结构
C.Cl— 和NH3分子均与Pt4+配位
D.配合物中Cl—与Pt4+配位,而NH3分子不配位
查看答案和解析>>
科目: 来源:2013届湖北武汉部分重点学校高二下学期期末统考化学卷(解析版) 题型:填空题
(10分)美国Bay等工厂使用石油热裂解的副产物甲烷来制取氢气,其生产流程如右图:

(1)此流程的第II步反应为:CO(g)+H2O(g) H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
;反应的平衡常数随温度的变化如下表:
H2(g)+CO2(g),该反应的化学平衡常数表达式为K=
;反应的平衡常数随温度的变化如下表:
|
温度/℃ |
400 |
500 |
830 |
1000 |
|
平衡常数K |
10 |
9 |
1 |
|
从上表可以推断:此反应是 (填“吸”或“放”)热反应。在830℃下,若开始时向恒容密闭容器中充入CO与H2O均为1mo1,则达到平衡后CO的转化率为 。
(2)在830℃,以下表的物质的量(单位为mol)投入恒容反应器发生上述第II步反应,其中反应开始时,向正反应方向进行的有 (填实验编号);
|
实验编号 |
n(CO) |
n(H2O) |
n(H2) |
n(CO2) |
|
A |
1 |
5 |
2 |
3 |
|
B |
2 |
2 |
1 |
1 |
|
C |
0.5 |
2 |
1 |
1 |
(3)在一个不传热的固定容积的容器中,判断此流程的第II步反应达到平衡的标志是 。
①体系的压强不再发生变化 ②混合气体的密度不变
③混合气体的平均相对分子质量不变 ④各组分的物质的量浓度不再改变
⑤体系的温度不再发生变化 ⑥v(CO2)正=v(H2O)逆
(4)右图表示此流程的第II步反应,在t1时刻达到平衡、在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件是(写出两种) 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com