
科目: 来源: 题型:022
![]() 是一种白色晶体,加热到160℃时可升华为蒸气,测知180℃时的蒸气密度(已折合成标况)为9.3 g·
是一种白色晶体,加热到160℃时可升华为蒸气,测知180℃时的蒸气密度(已折合成标况)为9.3 g·![]() ,分子没有极性,P-Cl键长为204 pm和211
pm两种,继续加热到250℃时测知压力为相同条件下初始蒸气的两倍.
,分子没有极性,P-Cl键长为204 pm和211
pm两种,继续加热到250℃时测知压力为相同条件下初始蒸气的两倍.![]() 在加压下于148℃液化,形成一种能导电的熔体,测知P-Cl键长为198
pm和206 pm两种.回答下列问题:
在加压下于148℃液化,形成一种能导电的熔体,测知P-Cl键长为198
pm和206 pm两种.回答下列问题:
(1)180℃时的![]() 蒸气中存在________分子,其主体结构为________.
蒸气中存在________分子,其主体结构为________.
(2)250℃时的![]() 蒸气存在________分子,其主体结构为___________________.
蒸气存在________分子,其主体结构为___________________.
(3)![]() 熔体导电的原因是________,导电微粒是________,电离方程式为________.
熔体导电的原因是________,导电微粒是________,电离方程式为________.
(4)![]() 气态分子的结构与
气态分子的结构与![]() 相似,它的熔融体也能导电,
相似,它的熔融体也能导电,
经测知其中只存在一种P-Br键长,则导电的微粒是________,电离方程式为________.
查看答案和解析>>
科目: 来源:浙江省温州中学2011-2012学年高一下学期期末考试化学理科试题 题型:022
电解原理在化学工业中有广泛应用.下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则电解池中
①X极上的电极反应式为________,在X极附近观察到的现象是________.
②Y极上的电极反应式为________,检验该电极反应产物的方法是________.
(2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是________,电极反应式是________.
②Y电极的材料是________,电极反应式是________.(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目: 来源:河北省冀州中学2011-2012学年高一下学期期中考试化学理科试题(A)卷科 题型:022
某研究性学习小组将下列装置如图连接,E、F、X、Y均为石墨电极.向装置乙中滴入酚酞试液,将电源接通后F极附近显红色.试回答下列问题:

(1)题中采用的电源是铅蓄电池,电池总反应式为:Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O,则图中电源放电时A极的电极反应式是________;
2PbSO4+2H2O,则图中电源放电时A极的电极反应式是________;
(2)用甲装置实现粗铜精炼,则C电极的材料应该是________,D电极上的反应式为________.
(3)用丙装置实现铜上镀银,则G电极的材料应该是________(填名称).电解质溶液的主要成分是________.(填化学式)
(4)检验E极电解产物的方法:________,当装置电路中有6.02×1021个电子通过时,乙中溶液(假设体积为100 mL)的pH是________.
(5)装置丁的U形管中为硫酸铜溶液,初始阶段电解反应的化学方程式是________.继续通电一段时间后,向所得溶液中加入0.2 mol Cu(OH)2,恰好恢复到电解前的浓度和pH,则电路中通过电子数为________mol.
查看答案和解析>>
科目: 来源:河北省冀州中学2011-2012学年高一下学期期中考试化学理科试题(B)卷科 题型:022
某研究性学习小组将下列装置如图连接,E、F、X、Y均为石墨电极.向装置乙中滴入酚酞试液,将电源接通后F极附近显红色.试回答下列问题:

(1)题中采用的电源是铅蓄电池,电池总反应式为:Pb+PbO2+4H++2SO42-![]() 2PbSO4+2H2O,则图中电源放电时A极的电极反应式是________;
2PbSO4+2H2O,则图中电源放电时A极的电极反应式是________;
(2)用甲装置实现粗铜精炼,则C电极的材料应该是________,D电极上的反应式为________.
(3)用丙装置实现铜上镀银,则G电极的材料应该是________(填名称).电解质溶液的主要成分是________(填化学式)
(4)检验E极电解产物的方法:________,当装置电路中有6.02×1021个电子通过时,乙中溶液(假设体积为100 mL)的pH是________.
(5)装置丁的U形管中为硫酸铜溶液,初始阶段电解反应的化学方程式是________.继续通电一段时间后,向所得溶液中加入0.2 mol Cu(OH)2,恰好恢复到电解前的浓度和pH,则电路中通过电子数为________mol
查看答案和解析>>
科目: 来源:浙江省金华一中2011-2012学年高一下学期期中考试化学试卷 题型:022
X、Y、Z三种强电解质,它们在水中电离出的离子如下表所示:
下图所示装置中,甲、乙、丙三个烧杯依次分别盛放250 mL足量的X溶液、足量的Y溶液、足量的Z溶液,电极均为石墨电极.

接通电源,经过一段时间后,测得乙中c电极质量增加.常温下各烧杯中溶液的pH与电解时间t的关系图如上.据此回答下列问题:
(1)M为电源的________极(填写“正”或“负”).
(2)甲烧杯中电极b上发生的电极反应为________.
(3)乙烧杯电解的总反应离子方程式为________,电解一段时间后停止电解(此时溶液中还有原溶质),若要将乙烧杯中的溶液恢复到原状态,则需要加入________(填化学式).
(4)若经过一段时间后,丙装置中两极附近均滴酚酞,________极附近变红,其原因是________.
查看答案和解析>>
科目: 来源:四川省南山中学2011-2012学年高二下学期期中考试化学试题 题型:022
下图表示一个电解池,装有电解液a、X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:

(1)若X、Y都是惰性石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,在X极附近观察到的现象是________;Y电极上的电极反应式是________,将Y电极反应产物通入Na2S溶液观察到的现象是________.电解NaCl溶液的离子方程式是________.某厂现有50台电解槽,每台平均每天消耗2.925×105 g食盐,电解生成的Cl2与H2按体积比1∶1.15合成质量分数为36.5%的盐酸.不考虑损耗,理论上一天可生产36.5%的盐酸________t.(保留三位有效数字)
(2)若要在铁制品上镀一定厚度的Ag,Y电极反应式为________,工作一段时间后pH将________(填“增大”或“减小”或“不变”)
(3)若X、Y都是铂电极,电解某金属M的氯化物(MCl2)溶液,当收集到1.12 L氯气时(标准状况),阴极增重3.2 g.该金属的相对原子质量是________.
查看答案和解析>>
科目: 来源:江苏省扬州中学2012届高三11月练习化学试题 题型:022
联碱法(候氏制碱法)和氨碱法的生产流程简要表示如下图:


(1)沉淀池中发生反应的化学方程式为________;
(2)X是________,Y是________(填化学式);
(3)从理论上分析,在氨碱法生产过程中________(填“需要”、“不需要”)补充氨气,从原料到产品,氨碱法总反应过程用化学方程式表示,可写为________;
(4)根据联碱法中从母液中提取氯化铵晶体的过程推测,所得结论正确是________;
a.常温时氯化铵的溶解度比氯化钠小
b.通入氨气目的是使氯化铵更多析出
c.加入食盐细粉目的是提高Na+的浓度,促进碳酸氢钠结晶析出
(5)相比于氨碱法,指出联碱法的一项优点________.
查看答案和解析>>
科目: 来源:山东省临清三中2011-2012学年高二11月学分认定测试化学理科试题 题型:022
(1)25℃,柠檬水的pH是3,其中c(OH-)=________
(2)下列溶液中,c(H+)由小到大的排列顺序是________
①0.1 mol/L HCl溶液
②0.1 mol/L H2SO4溶液
③0.1 mol/L NaOH溶液
④0.1 mol/L CH3COOH溶液
(3)在25℃时,1 mol·L-1的
①(NH4)2SO4
②CH3COONH4
③(NH4)2Fe(SO4)2
④NH4Cl的溶液中,c(NH4+)由大到小的顺序为________
(4)pH=3盐酸和pH=11氨水等体积混合后溶液呈________性(选填“酸”、“中”或“碱”),溶液中c(NH4+)________c(Cl-)(选填“>”“=”“<”).
查看答案和解析>>
科目: 来源:山东省日照市2012届高三12月月考化学试题 题型:022
| |||||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:辽宁省沈阳二中2011-2012学年高二上学期12月月考化学试题 题型:022
惰性电极电解NaCl溶液或CuSO4溶液都得到三种产物A、B、C,各物质之间的转化关系如下图所示(图中参与反应和生成的水都已略去).已知甲是短周期元素的单质,它是日常生活中常用的包装材料.
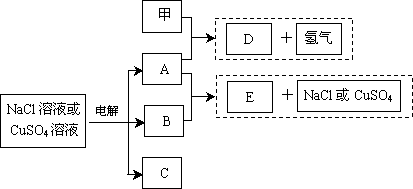
回答下列问题:
(1)若电解的是NaCl溶液:
①甲与A反应的化学方程式是________.
②A与B反应的离子方程式是________.
③常温下,若电解100 mL 0.1 mol/L NaCl溶液,阴、阳两极各产生112 mL气体(标准状况),则所得溶液的pH为________(忽略反应前后溶液的体积变化及气体溶于水的影响).
(2)若电解的是CuSO4溶液,加热时,A的浓溶液可与B发生反应:
①A的浓溶液与B反应过程中,A的浓度随时间变化的图像正确是________.



②E的化学式是________;电解时阳极的电极反应式是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com