
科目: 来源:山东省日照市2011届高三一模理综化学试题 题型:058
美日科学家因研发“有机合成中的钯催化的交叉偶联”而获得2010年度诺贝尔化学奖.有机合成常用的钯/活性炭催化剂长期使用,催化剂会被杂质(如:铁、有机物等)污染而失去活性,成为废催化剂,故需对其回收再利用.一种由废催化剂制取氯化钯(PdCl2)的工艺流程如下:

(1)甲酸在反应中的作用是________(选填:“氧化剂”或“还原剂”);
(2)加浓氨水时,钯元素转变为可溶性[Pd(NH3)4]2+,此时铁元素的存在形式是________(写化学式);
(3)王水是浓硝酸与浓盐酸按体积比1∶3混合而成的,钯在王水中溶解的过程中有化合物A和一种无色、有毒气体B生成.
①气体B的化学式为________,
②经测定,化合物A由3种元素组成,有关元素的质量分数为Pd:42.4%,H:0.8%.则A的化学式为________;
(4)700℃“焙烧1”的目的是________,550℃“焙烧2”的目的是________.
查看答案和解析>>
科目: 来源:北京市朝阳区2011届高三一模理综化学试题 题型:058
KClO3在农业上用作除草剂,超细CaCO3广泛用于消光纸、无炭复写纸等.某同学在实验室模拟工业过程,利用制乙炔产生的残渣制备上述两种物质,过程如下:
Ⅰ.![]()
①电石与水反应的化学方程式是________.
②残渣中主要成分是Ca(OH)2和________.
Ⅱ.将Ⅰ中的部分灰浆配成浊液,通入Cl2,得到Ca(ClO3)2与CaCl2物质的量之比为1∶5的溶液,反应的化学方程式是________.
Ⅲ.向Ⅱ所得溶液中加入KCl,发生复分解反应,经蒸发浓缩,冷却结晶,过滤得KClO3晶体.你认为能得到KClO3晶体的原因是________________.
Ⅳ.将Ⅰ中的残渣溶于NH4Cl溶液,加热,收集挥发出的气体再利用.向所得CaCl2溶液中依次通入NH3、CO2,便可获得超细CaCO3,过程如下:
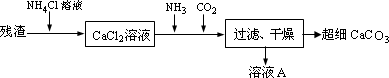
①根据沉淀溶解平衡原理,解释残渣中难溶盐的溶解原因________________.
②CaCl2溶液中通入两种气体后,生成超细CaCO3的化学方程式是________.
③图示的溶液A可循环使用,其主要成分的化学式是________.
查看答案和解析>>
科目: 来源:河北省张家口市涿鹿中学2011届高三上学期第一次月考化学试题 题型:058
现有一定量含有Na2O杂质的Na2O2试样,用下图的实验装置测定Na2O2试样的纯度.(可供选用的反应物只有CaCO3固体、6 mol/L盐酸、6 mol/L硫酸和蒸馏水)
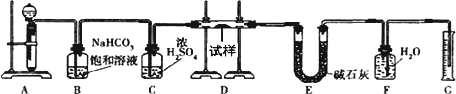
回答下列问题:
(1)实验前必须检查装置的气密性.仪器连接好后,在________中加适量的水,关闭A中分液漏斗活塞后微热试管,若看到________说明装置气密性好.
(2)装置A中液体试剂选用盐酸而不用硫酸,理由是________.
(3)装置B的作用是________;装置C的作用是________;装置E中碱石灰的作用是________.
(4)装置D中发生反应的化学方程式是:________,________.
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则Na2O2试样的纯度为________.
查看答案和解析>>
科目: 来源:福建省三明市泰宁一中2011届高三第一次月考化学试题 题型:058
| |||||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:浙江省杭州市西湖高级中学2011届高三上学期开学考试化学试题 题型:058
某研究性学习小组查阅资料得知,漂白粉与硫酸反应可以制得氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4![]() 2CaSO4+2Cl2↑+2H2O.他们设计了如下制取氯气并验证其性质的实验.
2CaSO4+2Cl2↑+2H2O.他们设计了如下制取氯气并验证其性质的实验.
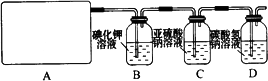
试回答:
(1)该实验中A部分的装置是________(填写装置的序号).
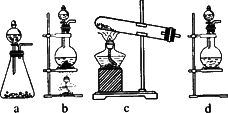
(2)请你设计一个实验,证明洗气瓶C中的Na2SO3已经被氧化(简述实验步骤):________.
(3)写出D装置中发生反应的离子方程式________.
(4)该实验存在明显的缺陷,请你提出改进的方法________.
(5)该小组又进行了如下实验:称取漂白粉2.0 g,研磨后溶解,配制成250 ml溶液,取25 ml加入到锥形瓶中,再加入过量的KI溶液和过量的H2SO4溶液,静置.待完全反应后,用0.1 mol/L的Na2S2O3溶液作标准溶液滴定反应生成的碘,已知反应式为:
2Na2S2O3+I2![]() Na2S4O6+2NaI
Na2S4O6+2NaI
反应完成时,共用去Na2S2O3 20.0 ml.则该漂白粉中Ca(ClO)2的质量分数为:________
查看答案和解析>>
科目: 来源:福建省福州市八中2011届高三年级上学期第一次月考试题化学试卷 题型:058
某研究性学习小组为测定某Na2CO3样品的纯度(其中只含NaHCO3杂质),选用下图所示的仪器装置进行实验(②装置未画全).试回答有关问题:

实验一:测定Na2CO3样品中NaHCO3分解放出CO2体积:连接装置的正确顺序是⑦①③④⑤⑥
(1)写出加热时发生反应的化学方程式________.
(2)完成该实验尚缺的仪器是________(填名称);产生气体从装置④的________进入,从装置⑤的________进入(填接口序号).
实验二:测定上述实验完成后剩余固体与盐酸反应产生CO2的体积.
(3)应将实验一的装置作哪些调整?________.
(4)当实验一加热至样品不再产生气体时,产生CO2体积为a L(已换算成标况下的体积,下同),则样品中NaHCO3的质量为________;实验二在加入盐酸至无气体产生时,生成CO2体积为b L,则Na2CO3样品的纯度为________.
误差分析:
(5)有同学建议将⑤中的水改用饱和的NaHCO3溶液,可以使测定结果更准确,请用平衡移动观点解释:________,同学为何没建议改用Na2CO3饱和溶液?请用离子方程式说明原因:________.
(6)有同学发现在实验一读取CO2体积时,⑥中液体的液面低于⑤中液体的液面,但未做任何处理,则a值________(填“偏大”、“偏小”或“无影响”).
查看答案和解析>>
科目: 来源:甘肃省天水三中2009-2010学年高一下学期第二阶段测试化学试题 题型:058
实验室用N2、H2合成氨气,并用酚酞试液检验生成的氨气,用锌与盐酸反应制取氢气;用NaNO2饱和溶液和NH4Cl饱和溶液共热制取氮气:
NaNO2+NH4Cl=NaCl+NH4NO2 NH4NO2![]() N2↑+2H2O.
N2↑+2H2O.
制取装置如图所示:
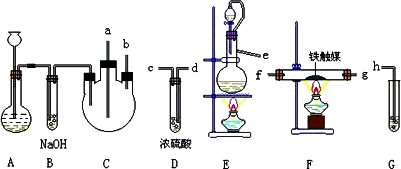
(1)装置A用于制取________
(2)装置E中分液漏斗上方常用导管与园底烧瓶相通,作用是________.装置E与装置C直接相连,连接时导管口连接方法为e接________.
(3)装置C的另一接口与其他仪器装置相连接时,导管口的连接顺序为:另一接口________接________,________接________,________接________.
(4)装置D的作用为________.装置F导出的气体的成分为________
(5)装置G内滴有酚酞的试液,用于检验氨气的生成,该装置中导管口能否插入液面以下________(填“能”或“不能”),理由是________.
(6)从充分利用原料的角度看,装置G应装双孔塞,此时另一接口应与________相连为佳.
查看答案和解析>>
科目: 来源:浙江省嘉兴一中2010-2011学年高二10月月考化学试题 题型:058
| |||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:浙江省杭州市西湖高级中学2011届高三上学期10月月考化学试题 题型:058
| |||||||||||||||||||||||||||||||||||
查看答案和解析>>
科目: 来源:辽宁省沈阳二中2010-2011学年高二10月月考化学试题 题型:058
在如图用石墨作电极的电解池中,放入500 mL含一种溶质的某蓝色硫酸盐溶液进行电解,观察到A电极表面有红色的固态物质生成,B电极有无色气体生成.请回答下列问题:
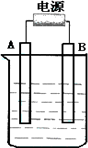
(1)请写出B极板的名称:________ 电极反应式________.
写出电解时反应的总离子方程式________.
(2)若当溶液中的原有溶质完全电解后,停止电解,取出A电极,洗涤、干燥、称量、电极增重1.6 g.电解后溶液的pH为________;要使电解后溶液恢复到电解前的状态,则需加入________,其质量为________g.(假设电解前后溶液的体积不变)
(3)若原溶液为1 L K2SO4、CuSO4的混合溶液,且c(SO42-)=2.0 mol/L;如图装置电解,当两极都收集到22.4 L气体(标准状况)时,停止电解.
则原溶液中的c(K+)=________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com