

科目: 来源:知识精讲与能力训练 高三化学 题型:058
现有一定量的含有Na2O杂质的Na2O2试样,请从下图中选用适当的实验装置,设计一个最简单的实验,测定Na2O2试样的纯度(可供选用的反应物只有CaCO3固体、6mol/L盐酸和蒸馏水).
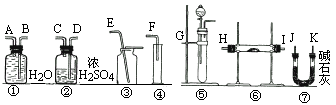
请填写下列空白:
(1)写出在实验中Na2O和Na2O2分别发生反应的化学方程式________.
(2)应选用的装置是(只要求写出图中装置的标号)________.
(3)所选用装置的连接顺序是________.
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
某课外活动小组加热炭粉(过量)和氧化铜的混合物,再用下图装置,对获得的铜粉(含炭)样品进行实验.图中铁架台等装置已略去.请你帮助他们完成下列实验报告.
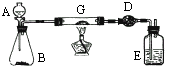
(一)实验目的:________.
(二)实验用品:仪器、天平、分液漏斗、锥形瓶、硬质玻璃管、干燥管、酒精灯、洗气瓶等.药品:红褐色铜粉(含炭)样品、过氧化氢溶液、二氧化锰、碱石灰、浓硫酸等
(三)实验内容:
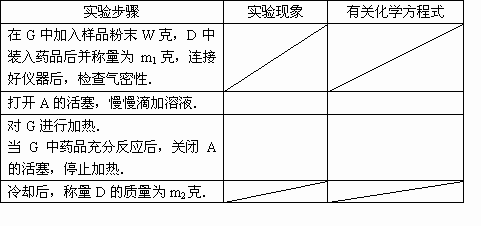
(四)计算:样品中铜的质量分数=________(用含W、m1、m2的代数式表示)
(五)问题和讨论:
实验完成后,老师评议说:按上述实验设计,即使G中反应完全、D中吸收完全,也不会得出正确的结果.经讨论,有同学提出在B与G之间加入一个装置.再次实验后,得到了较正确的结果.那么,原来实验所测得的铜的质量分数偏小的原因可能是________.在B与G之间加入的装置可以是________,其中盛放的药品是________.
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
实验室用下图所示装置制取溴化亚铁.其中A为CO2发生装置,D和d中均盛有液溴,E为外套电炉丝的不锈钢管.e是两只耐高温的瓷皿,其中共盛有56g细铁粉.实验开始时先将铁粉加热至600℃~700℃,然后将干燥、纯净的CO2气流通入D中,E管中反应开始,最后将d中液溴滴入100℃~120℃的D中,经过几小时的连续反应,在铁管的一端沉积有黄绿色鳞片状溴化亚铁80g.
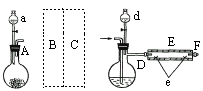
请回答:
(1)如何检查用塞子(插有导管和仪器)塞紧的D的气密性________.
(2)若导入的CO2不干燥,会在E中发生副反应,其化学方程式为________;若在A中盛固体CaCO3,a中盛6mol/L盐酸,为使导入D中的CO2为干燥纯净的气体,则图中B、C处的装置和其中的试剂应是:B为________,C为________.
(3)实验时,装置D和E的橡皮塞最好用铅箔包住,原因是________.
(4)反应过程中要不断通入CO2,其主要作用是①________,②________.
(5)E中的反应为:2Fe+3Br2![]() 2FeBr3,2FeBr3
2FeBr3,2FeBr3![]() 2FeBr2+Br2↑,求此实验中FeBr2的产率________.
2FeBr2+Br2↑,求此实验中FeBr2的产率________.
(6)为防止污染空气,实验时应在F处连接盛________的尾气吸收装置.
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
为了测定某烷烃样品(丁烷,并含少量丙烷等气态烃)的平均分子量,设计了下面的实验:

①取一个配有合适胶塞的洁净、干燥的锥形瓶,准确称量,得到质量m1
②往锥形瓶中通入干燥的该烷烃样品,塞好胶塞,准确称量;重复操作,直到前后两次称量结果基本相同,得到质量m2
③往锥形瓶内加满水,塞好胶塞,称量得到质量m3
已知实验时的温度T(K),压强P(kPa),水的密度ρ水(g·L-1),空气的平均分子量29.0,密度ρ空气(g·L-1),回答下面问题:
(1)本实验的原理是(具体说明)_________.
(2)步骤②中为什么要重复操作,直到前后两次称量结果基本相同?
(3)具体说明本实验中怎样做到每次测量都是在相同体积下进行的?
(4)本实验中收集气体样品的操作,可选用的方法是(填图中标号)_________.
(5)锥形瓶内空气的质量(m空气)是________(列出算式)
(6)瓶中样品的质量(m样品)是________.(列出算式)
(7)由实验测得该烷烃的平均分子量是________(列出算式)
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
已知SnCl4、SiCl4、AlCl3、PCl3等氯化物在潮湿的空气中打开瓶塞后,都有白雾生成.为清楚地观察磷在Cl2中燃烧,达到PCl3和PCl5分步生成的目的.可预先把干燥的Cl2贮存在100mL的注射器内,再把火柴头大小的红磷置于玻璃燃烧匙上烘干后,组成如图所示的装置.操作时打开弹簧夹,缓缓推动注射器的针塞,待磷燃烧出现白雾时,立即关闭弹簧夹,停止推入Cl2,片刻后,可见到试管内白雾凝成无色液滴附着在试管内壁.然后再打开弹簧夹,继续推入Cl2,就可看到管壁上液滴逐渐消失,管内出现白烟,最后白烟凝结成白色固体附着在试管内壁上.试回答:
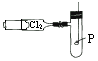
(1)该实验选择玻璃燃烧匙,不选其他金属燃烧匙的原因是________;
(2)该实验的关键是,使用的Cl2和红磷必须干燥,(请用必要的文字和化学方程式说明原因)________;
(3)第二次推入Cl2时发生的反应是(用化学方程式表示)________,故第一次推入Cl2之所以要缓缓进行的原因是________.
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
某种碱式碳酸铜是孔雀绿色固体粉末,其组成可表示为Cu2(OH)2CO3·xH2O.
在加热的条件下,它在失去结晶水的同时发生分解,反应方程式是
Cu2(OH)2CO3·xH2O![]() 2CuO+CO2↑+(x+1)H2O
2CuO+CO2↑+(x+1)H2O
现取一定量该固体样品,不准确称量其质量,用两套仪器装置,先后进行两个实验:
实验(Ⅰ)测定该碱式碳酸铜粉末组成中结晶水x的值;实验(Ⅱ)用实验(Ⅰ)结束后的残留固体与乙醇蒸气反应,并检验反应产物.

试回答下列问题:
(1)现已装配好下面一套仪器装置(参见图示),装置中必要的铁架台、铁夹、铁圈、酒精灯、石棉网在图中均已略去),这套装置是用来完成上述的实验________的.(填标号).
(2)用图示的仪器(必要的铁架台、铁夹、酒精灯均在图中略去)组装完成另一个实验的实验装置.组装好仪器按气流方向从左到右连接顺序是________→________→________→________.
在这套实验装置中,干燥管H的作用是________.
(3)实验开始时,碱式碳酸铜放在仪器(填装置对应字母)________中,乙醇放在仪器(填装置对应字母)________中.
(4)这两套装置中,在实验时需要加热的仪器是(填装置对应字母)________.
(5)实验结束后可见试管D的内壁有银白色金属析出.实验中试管A内发生反应的化学方程式是________,从试管A通入试管D的导管中气体的成分是(写名称,其中水蒸气不必写出)________.
(6)这两套装置中,在实验前后均要连同所盛试剂一起准确称量的仪器是(填装置对应字母)________;若用托盘天平称量,其中某次称量记录的数据是51.12g.这样记录是否合理?________(填“合理”或“不合理”).
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
用下列仪器、药品验证由铜和适量浓硝酸反应产生的气体中含NO(仪器可选择使用,N2和O2的用量可自由控制),已知:①NO+NO2+2OH-![]() 2NO2-+H2O;②气体液化温度:NO2-21℃,NO-152℃.
2NO2-+H2O;②气体液化温度:NO2-21℃,NO-152℃.
试回答:
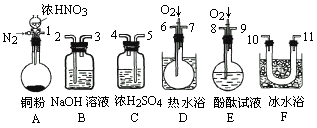
(1)仪器的连接顺序(按从左到右连接,填各接口的编号)为________.
(2)反应前先通入N2,目的是________.
(3)确认气体中含NO的现象是________.
(4)装置F的作用是________.
(5)如果O2过量,则装置B中发生反应的化学方程式为________.
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
如图(尚有部分仪器未画),有一蒸馏烧瓶与注射器相连接,向蒸馏烧瓶中先加入0.384g铜片和18mL、2.5mol/L的稀硝酸溶液,立即用锡箔包住的橡胶塞封住烧瓶瓶口,实验装置内的空气在标准状况下为500mL(其中注射器内不少于其体积1/2,见图示).

(1)欲提高Cu与HNO3反应的速率可采用多种不同措施.
①若采用加化学试剂法,可加入的试剂为________;
A.蒸馏水
B.无水醋酸钠
C.块状石墨
②若用升高温度法,请在上述示意图空缺处画出必需的仪器.
(2)当烧瓶中的Cu和HNO3反应开始后,可观察到的现象有________.
(3)待Cu与HNO3反应停止后,通过轻轻推拉注射器活塞,使装置内气体与气体、气体与液体之间充分反应,若忽略液体体积变化,最终溶液中NO3-的物质的量浓度与开始时相比是否有变化________(填“有变化”或“不变”).
(4)在上述反应过程中,曾经被还原的硝酸为________mol.
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
“卤块”的主要成分为MgCl2(含Fe2+、Fe3+、Mn2+等杂质离子),若以它为原料,按如下工艺流程图,即可制得轻质氧化镁.如果要求产品尽量不含杂质离子,而且成本较低.流程中所用试剂或pH控制可参阅下表确定.
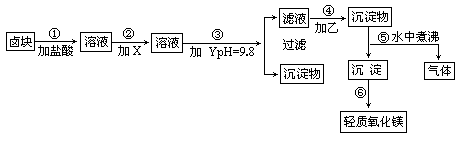
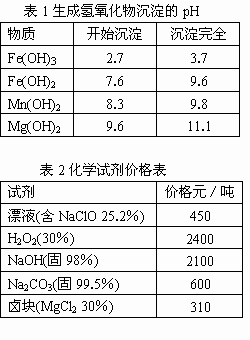
注:
Fe2+氢氧化物呈絮状,不易从溶液除去,所以常将它氧化成为Fe3+生成Fe(OH)3沉淀而除去.
请填写以下空白:
(1)在步骤②加入的试剂X,最佳选择应________,其作用是________.
(2)在步骤③加入的试剂Y,应是________之所以要控制pH=9.8,其目的是________.
(3)在步骤⑤时发生的化学方程式是________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com