

科目: 来源: 题型:058
下图所示的装置制取氢气,在塑料隔板上放粗锌粒,漏斗,和带支管的试管中装有稀硫酸,若打开弹簧夹,则酸液由漏斗流下,试管中液面上升与锌粒接触,发生反应,产生的氢气由支管导出;若关闭弹簧夹,则试管中液面下降,漏斗中液面上升,酸液与锌粒脱离接触,反应自行停止.需要时再打开弹簧夹,又可以使氢气发生.这是一种仅适用于室温下随制随停的气体发生装置.
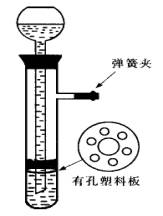
回答下面问题:
(1)为什么关闭弹簧夹时试管中液面会下降?
(2)这种制气装置在加入反应物前,怎样检查装置的气密性?
(3)从下面三个反应中选择一个可以用这种随制随停的制气装置制取的气体,填写下表中的空白.
①大理石与盐酸反应制取二氧化碳;
②黄铁矿与盐酸反应制取硫化氢;
③用二氧化锰催化分解过氧化氢制氧气.
|
气体名称 |
收集方法 |
检验方法 |
|
|
|
|
(4)食盐跟浓硫酸反应制氯化氢不能用这种装置随制随停.试说明理由.
查看答案和解析>>
科目: 来源: 题型:058
如下表,为了证实(Ⅰ)项中的结论,请从(Ⅱ)项中选出相应的实验方法,并从(Ⅲ)项中选出所观察到的相应的实验现象.将每题正确答案的标号填写在答案栏里.
|
(Ⅰ)实验结论 |
(Ⅱ)实验方法 |
(Ⅲ)实验现象 |
答案 |
||
|
(Ⅰ) |
(Ⅱ) |
(Ⅲ) |
|||
|
1.汽油中含有少量水 2.长期放置的FeSO4 溶液变质 3.长期放置的KI酸性 溶液中含有少量碘 4.一种元色有刺激性 气味的气体是SO2 5.粗食盐中含有少量 钾盐 |
A.加BaCl2溶液 B.加淀粉溶液 C.加酚酞溶液 D.加品红溶液 E.加盐酸 F.加无水硫酸铜 G.加AgNO3溶液 H.进行焰色反应 Ⅰ.加饱和氯水 J.加KSCN溶液 |
a.有气泡产生 b.有不溶于酸的白色沉淀产生 c.显蓝色 d.呈黄色 e.显红色 f.红色褪去 g.显紫红色 h.有白色絮状沉淀生成,最后呈红褐色 i.显浅紫色(透过蓝色钴玻璃) j.有不溶于酸的黄色沉淀产生 |
1 |
|
|
查看答案和解析>>
科目: 来源: 题型:058
(1)若CO2中混有CO,除去的方法是________;
(2)若CO2中混有HCl,要得到纯净的CO2,其方法是________________________;
(3)将镁条在空气中点燃后伸入装有纯净CO2的集气瓶中,能观察到的现象是(不必写产物的名称或分子式)________________________________;
(4)在没有现成的CO2气体发生器的情况下,请你选用下图中的部分仪器,装配成一个简易的、能随开随用、随关随停的CO2气体发生装置,应选用的仪器是(填入编号)________;

(5)若用上述装置制取CO2气体,而实验室只有稀硫酸、浓硝酸、水、块状纯碱、块状大理石,比较合理的方案中应选用的药品是________.
查看答案和解析>>
科目: 来源: 题型:058
下图为某学生利用氯酸钾分解制氧气的反应装置,以此来测定氧气的摩尔质量.实验步骤如下:

①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为α g.
②装好实验装置.
③检查装置气密性.
④加热,开始反应,直到产生一定量的气体.
⑤停止加热(如图,导管出口高于液面).
⑥测量收集到的气体体积.
⑦准确称量试管和残留物的质量为bg.
⑧测量实验室的温度.
⑨把残留物倒人指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净.
⑩处理实验数据,求出氧气的摩尔质量.
回答下列问题:
(1)如何检查装置的气密性?
_________________________________________________________________________________________________________________________________________________________.
(2)以下是测量收集到气体体积必须包括的几个步骤:①调整量筒内外液面高度使之相同②使试管和量筒内的气体都冷却至室温 ③读取量筒内气体的体积.这三步操作的正确顺序是_________(请填写步骤代号).
(3)测量收集到的气体体积时,如何使量筒内外液面的高度相同?
_______________________________________________________________________________
(4)如果实验中得到的氧气体积是cL(25℃、1.01×105Pa),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含口a、b、c,不必化简):
M(O2)=__________________________________.
查看答案和解析>>
科目: 来源: 题型:058
测定硫酸铜晶体(CuSO4·5H2O)里结晶水的含量,实验步骤为:①研磨;②称量空坩埚和装有试样的坩埚的质量;③加热;④冷却;⑤称量;⑥重复③至⑤的操作,直到连续两次称量的质量差不超过0.1g为止;⑦根据实验数据计算硫酸铜晶体里结晶水的含量.
请回答下列问题:
(1)现有坩埚、坩埚钳、三脚架、泥三角、玻璃棒、干燥器、药匙、硫酸铜晶体样品等实验用品,进行该实验时,缺少的实验用品的是________________.
(2)该实验中哪一步骤需要使用干燥?使用干燥器的目的是什么?
答:________________________________.
(3)实验步骤⑥的目的是________.
(4)若操作正确而实验测得的硫酸铜晶体中结晶水的含量偏低,其原因可能有(填入选项的编号):________.
A.被测样品中含有热不挥发的杂质
B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水
D.加热前所用的坩埚未完全干燥
查看答案和解析>>
科目: 来源:四中大考卷 高二化学(下册)、合成材料 题型:058
某种橡胶分解产物为碳氢化合物,对这种碳氢化合物进行以下实验:
①若取一定量的橡胶完全燃烧,燃烧后的气体通过干燥管,干燥管增重0.72g,再通过足量的石灰水,石灰水增重2.2g.
②经测定,该碳氢化合物(气体)的密度是相同状况下氢气密度的34倍.
③该碳氢化合物0.1mol能和32g溴起加成反应,经分析,产物中溴原子分布在不同的碳原子上,且溴代物中有一个碳原子在支链上,试推断:
(1)该碳氢化合物的结构简式是________,名称是________.
(2)该橡胶的结构简式是________,名称是________.
查看答案和解析>>
科目: 来源:活题巧解巧练·高考化学(第一轮) 题型:058
古代有一个时期人们曾经把水当成一种元素,后来的研究证明水是一种化合物.请你设计一个化学实验来证明水是一种化合物.
(1)设计的化学实验是________.
(2)使用的实验仪器是________.
(3)发生的化学反应的方程式是________.
查看答案和解析>>
科目: 来源:活题巧解巧练·高考化学(第一轮) 题型:058
用实验确定某酸HA是弱电解质.两同学的方案如下.
甲:①称取一定量的HA配制0.1mol/L的溶液100mL;
②用pH试纸测出该溶液的pH,即可证明HA是弱电解质.
乙:①用已知物质的量浓度的HA溶液、盐酸,分别配制pH=1的两种酸溶液各100mL;
②分别取这两种溶液各10mL,加水稀释为100mL;
③各取相同体积的两种稀释液装入两个试管,同时加入纯度相同的锌粒,观察现象,即可证明HA是弱电解质.
(1)在两个方案的第①步中,都要用到的定量仪器是________.
(2)甲方案中,说明HA是弱电解质的理由是测得溶液的pH________1(选填“>”,“<”,“=”).
乙方案中,说明HA是弱电解质的现象是________.
a.装HCl溶液的试管中放出H2的速率快
b.装HA溶液的试管中放出H2的速率快
c.两个试管中产生气体速率一样快
(3)请你评价:乙方案中难以实现之处和不妥之处________.
(4)请你再提出一个合理而比较容易进行的方案(药品可任取之),作简明扼要表述.________.
查看答案和解析>>
科目: 来源:知识精讲与能力训练 高三化学 题型:058
选用一种试剂鉴别下列各组物质:
①氯化铝、硫酸、硝酸钡、氯化钾四种溶液________
②硝酸银、盐酸、硫酸铝、碳酸氢钠四种溶液________
③氯化镁、硫酸铝、硝酸铵、氯化钠四种溶液________
④碳酸钠、氢氧化钠、硝酸银、硫酸四种溶液________
⑤苯酚、苯乙烯、淀粉碘化钾、硝酸银、乙醇五种液体或溶液________
⑥氯化钡、碳酸钾、偏铝酸钾、硫化钠、盐酸五种溶液________
⑦氯化钾、氢溴酸、碘化钾、硫化钠、硝酸钠、氯水六种溶液________
⑧炭黑、氧化铜、铁粉、硫化亚铁、二氧化锰五种黑色粉末________
⑨乙酸、乙醇、苯、氢氧化钡溶液、氯化铝溶液________
查看答案和解析>>
科目: 来源:高考三人行 化学 题型:058
维生素C是一种水溶性维生素(其水溶液呈酸性),其化学式C6H8O6,人体缺乏则易得坏血症,故称之为抗坏血酸.维生素C易被空气中的氧气氧化.在新鲜的水果、蔬菜、乳制品中都富含维生素C,如新鲜橙汁中维生素C的含量在500mg·L-1左右.
某课外活动小组测定了某牌子的软包装橙汁中维生素C的含量,下面是他们测定实验的分析报告.(请填写有关空白)
(1)实验目的:测定××牌软包装橙汁维生素C的含量,检验该品牌是否符合国家标准.
(2)实验原理:C6H8O6+I2=C6H6O6+2I-+2H+.
(3)实验用品及试剂:
①实验仪器和用品:自选(略).
②试剂:指示剂 ① (填名称)、7.50×10-3mol/L标准碘溶液、蒸馏水等.
(4)实验步骤:
a.洗涤仪器,检查滴定管是否漏液,润洗后装好标准碘溶液待用.
b.打开橙汁包装,目测:颜色![]() 橙黄色,澄清度
橙黄色,澄清度![]() 好.用 ② ;(填仪器名称)向锥形瓶中加入20.00mL待测橙汁,滴入2~3滴指示剂.
好.用 ② ;(填仪器名称)向锥形瓶中加入20.00mL待测橙汁,滴入2~3滴指示剂.
c.用左手控制滴定管的 ③ (填部位名称),右手摇动锥形瓶,眼睛注视 ④ ,直到滴定终点.滴定终点的现象是 ⑤ .
(5)数据记录与处理:在计算维生素C的含量前,应进行怎样的数据处理? ⑥ .若经数据处理,滴定中消耗标准碘溶液的体积是15.00mL,则该橙汁中维生素C的含量是 ⑦ mg/L.
(6)问题与讨论:
a.滴定时能否剧烈摇动锥形瓶? ⑧ .原因是⑨.
b.从分析数据看,该橙汁是否纯天然? ⑩ .制造商可能采取的做法是 ![]() (A.加水稀释天然橙汁;B.天然橙汁被浓缩;C.将维生素C作为添加剂).你是否同意这种做法?(A.同意;B.不同意;C.调查后再作结论).
(A.加水稀释天然橙汁;B.天然橙汁被浓缩;C.将维生素C作为添加剂).你是否同意这种做法?(A.同意;B.不同意;C.调查后再作结论).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com