
科目: 来源:新人教版2011-2012学年高二上学期单元测试(2)化学试题 题型:058
如下图(a)为持续电解稀BaCl2水溶液的装置(以铂为电极,A为电流表),电解一段时间后,从图(b)1小时起将CO2连续通入电解液中,请在图(b)中完成实验(a)中电流对时间的变化关系图,并回答有关问题.

(1)完成实验(a)中电流对时间的变化关系图.
(2)电解时F极发生________反应,电极反应式为________;E极发生________反应,电极反应式为________;电解总方程式为________.
(3)电解池中产生的现象:
①________
②________
③________.
查看答案和解析>>
科目: 来源:山东省莘县实验高中2011-2012学年高二下学期第一次月考化学试题 题型:058
已知pH为4-5的条件下,Cu2+几乎不水解,而Fe3+几乎完全水解.某学生用电解纯净的CuSO4溶液的方法,并根据电极上析出Cu的质量(n)以及电极上产生气体的体积(V mL标准状况)来测定Cu的相对原子质量,过程如下:
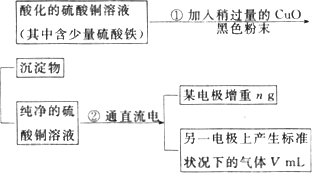
回答下列问题:
(1)加入CuO的作用是________.
(2)步骤②中所用的部分仪器如下图所示,则A、B分别连直流电源的________和________极(填“正”或“负”).
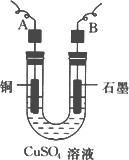
(3)电解开始后,在U形管中可以观察到的现象有:________.电解的离子方程式为________.
(4)下列实验操作中必要的是________(填写字母).
(A)称量电解前的电极的质量;
(B)电解后,电极在烘干称量前,必须用蒸馏水冲洗;
(C)刮下电解后电极上析出的铜,并清洗,称量;
(D)电解后烘干称重的操作中必须按“烘干→称量→再烘干→再称量”进行;
(E)在有空气存在的情况下,烘干电极必须用低温烘干的方法.
(5)铜的相对原子质量为________(用带有m、V的计算式表示).
查看答案和解析>>
科目: 来源:福建省莆田一中2011-2012学年高二第一学段考试化学试题(人教版) 题型:058
某液态卤代烷RX(R是烷基,X是某种卤素原子)的密度是a g/cm3.该RX可以跟稀碱发生水解反应生成ROH(能跟水互溶)和HX.为了测定RX的相对分子质量,拟定的实验步骤如下:
①准确量取该卤代烷b mL,放入锥形瓶中.
②在锥形瓶中加入过量稀NaOH溶液,塞上带有长玻璃管的塞子,加热,发生反应.
③反应完成后,冷却溶液,加稀HNO3酸化,滴加AgNO3溶液,得白色沉淀.
④过滤、洗涤、干燥后称重,得到c g固体.
完成下面问题:
(1)装置中长玻璃管的作用是________.
(2)步骤④中,洗涤的目的是为了除去沉淀物上吸附的________离子.
(3)该卤代烷中所含卤素的名称是________,判断的依据是________.
(4)该卤代烷的相对分子质量是________(列出算式).
(5)如果在步骤③中加入HNO3的量不足,没有将溶液酸化,则步骤④中测得的c值(填下列选项代码)________.
A.偏大
B.偏小
C.不变
D.大小不定
查看答案和解析>>
科目: 来源:山东省宁阳四中2011-2012学年高二上学期期中学分认定化学试题(人教版) 人教版 题型:058
电解原理在化学工业中有广泛应用.下图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导与直流电源相连.请回答以下问题:
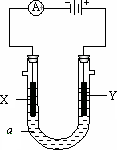
( 1) 若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中X极上的电极反应式为________.在X极附近观察到的现象是________.
②Y电极上的电极反应式为________,检验该电极反应产物的方法是________.
( 2) 如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则
①X电极的材料是________,电极反应式是________.
②Y电极的材料是________,电极反应式是________.(说明:杂质发生的电极反应不必写出)
查看答案和解析>>
科目: 来源:吉林省长春十一中2010-2011学年高一下学期期末考试化学理科试题 题型:058
请从下图中选用必要的装置进行电解饱和食盐水的实验,要求测定产生的氢气的体积,并检验氯气.
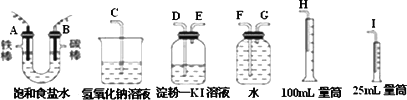
(1)A极发生的电极反应式是________B极发生的电极反应式是________
(2)设计上述气体实验装置时,各接口的正确连接顺序为:A接________、________接________;B接________、________接________.
(3)证明产物中有Cl2的实验现象是________.
(4)已知电解后测得产生的H2的体积为44.8 mL(已经折算成标准状况),电解后溶液的体积为50 mL,此时溶液中NaOH的物质的量浓度为:________.
(5)有一和电解饱和食盐水能量转换相反的装置中,一极通入甲烷,另一极通入氧气,电解质溶液为KOH溶液,负极的反应式为________正极的反应式为________.
查看答案和解析>>
科目: 来源:上海市长宁区2012届高三上学期期末质量抽测化学试题 题型:058
多晶硅主要采用SiHCl3还原工艺生产,其副产物SiCl4的综合利用受到广泛关注.
1.SiCl4可制气相白炭黑(与光导纤维主要原料相同),方法为高温下SiCl4与H2和O2反应,产物有两种,化学方程式为________.
2.SiCl4可转化为SiHCl3而循环使用.一定条件下,在20 L恒容密闭容器中的反应:
3SiCl4(g)+2H2(g)+Si(s)![]() 4SiHCl3(g)
4SiHCl3(g)
达平衡后,H2与SiHCl3物质的量浓度分别为0.140 mol/L和0.020 mol/L,若H2全部来源于离子交换膜法的电解产物,理论上需消耗纯NaCl的质量为________kg.
3.实验室制备H2和Cl2通常采用下列反应:
Zn+H2SO4→ZnSO4+H2↑;MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O
MnCl2+Cl2↑+2H2O
据此,从下列所给仪器装置中选择制备并收集H2的装置________(填代号)和制备并收集干燥、纯净Cl2的装置________(填代号).
可选用制备气体的装置:
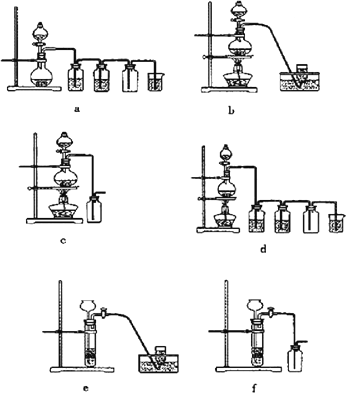
4.采用无膜电解槽电解饱和食盐水,可制取氯酸钠,同时生成氢气,现制得氯酸钠213.0 kg,则生成氢气________m3(标准状况).(忽略可能存在的其他反应)
查看答案和解析>>
科目: 来源:山西省太原五中2011-2012学年高二上学期期末检测化学理科试题 题型:058
某铬盐厂生产过程中排出含Cr2O72-的工业酸性废水.为防止污染环境,现采用下列工艺流程进行处理后再排出.

在整个处理过程中,Cr2O72-被还原为Cr3+,溶液的pH值逐渐升高,最后滤出的沉淀有Cr(OH)3和Fe(OH)3,试分析这个污水处理过程,回答:
(1)电解时,铁电极上的电极反应式:
阳极:________,
阴极:________;
(2)用铁(而不用炭)作电极进行电解的原因:________;
(3)Cr2O72-在酸性环境中被还原剂还原,能除去Cr2O72-.减少溶液酸性是整个工艺流程中关键的一步,这个变化的离子方程式是________;
(4)电解过程中当H+浓度小到一定程度时,便会析出Cr(OH)3、Fe(OH)3沉淀,已知常温下,Cr(OH)3的溶度积Ksp=10-32,要使c(Cr3+)降至10-5 mol/L,溶液的pH应至少为________.
查看答案和解析>>
科目: 来源:山东济宁邹城二中2011-2012学年高二上学期期中质检化学试题 题型:058
下图所示装置中,甲、乙两个烧杯分别依次盛放200 mL饱和食盐水、足量的AgNO3溶液,a、b、c、d四个电极均为石墨电极.接通电源,经过一段时间后,测得乙中d电极质量增加了2.16 g.据此回答问题:
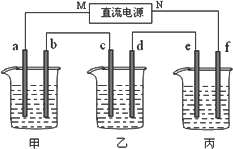
(1)电源的N端为________极;
(2)电极b上发生的电极反应为________;
(3)电极c上生成的气体在标准状态下的体积:________;
(4)甲溶液的氢氧根离子浓度为________(设溶液体积仍为200 mL);
(5)欲在丙烧杯中实现铁的表面镀上一层铜,则电解质溶液为________,e电极的材料是:________,f电极的电极反应式为________.
查看答案和解析>>
科目: 来源:山东省济宁市邹城二中2011-2012学年高二上学期期中质量检测化学试题 题型:058
下图所示装置中,甲、乙两个烧杯分别依次盛放200 mL饱和食盐水、足量的AgNO3溶液,a、b、c、d四个电极均为石墨电极.接通电源,经过一段时间后,测得乙中d电极质量增加了2.16 g.据此回答问题:
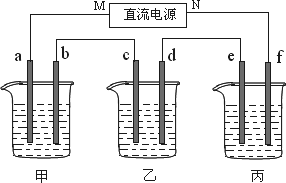
(1)电源的N端为________极;
(2)电极b上发生的电极反应为________;
(3)电极c上生成的气体在标准状态下的体积:________;
(4)甲溶液的氢氧根离子浓度为________(设溶液体积仍为200 mL);
(5)欲在丙烧杯中实现铁的表面镀上一层铜,则电解质溶液为________,e电极的材料是:________,f电极的电极反应式为________.
查看答案和解析>>
科目: 来源:吉林省长春外国语学校2011-2012学年高二第二次月考化学试题 题型:058
由于Fe(OH)2极易被氧化,所以实验室难用亚铁盐溶液与烧碱反应制得白色纯净的Fe(OH)2沉淀.若用下图所法实验装置可制得纯净的Fe(OH)2沉淀.两极材料分别为石墨和铁.

①a电极材料为________,其电极反应式为________.
②电解液d可以是________,则白色沉淀在电极上生成;也可以是________,则白色沉淀在两极之间的溶液中生成.
A.纯水
B.NaCl溶液
C.NaOH溶液
D.CuCl2溶液
③液体c为苯,其作用是________,在加入苯之前,对d溶液进行加热处理的目的是________.
④为了在短时间内看到白色沉淀,可以采取的措施是________.
A.改用稀硫酸做电解液
B.适当增大电源电压
C.适当缩小两电极间距离
D.适当降低电解液温度
⑤若d改为Na2SO4溶液,当电解一段时间,看到白色沉淀后,再反接电源,继续电解,除了电极上看到气泡外,另一明显现象为________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com