
科目: 来源: 题型:
【题目】甲、乙两种固体物质的溶解度曲线如右图所示。下列说法正确的是

A.20℃时,甲溶液中溶质的质量分数一定比乙溶液的大
B.将40℃时甲的一定量饱和溶液降温至20℃,溶液质量不变
C.甲的溶解度大于乙的溶解度
D.40℃时,分别在100g水中各加入30g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学实验小组同学测量氢化钙(CaH2)样品中氢化钙的质量分数。取5g样品于锥形瓶中,加入100g水溶解,待样品不再溶解时,称得锥形瓶剩余物质的质量为104.8g(假设杂质与水不发生反应,CaH2+2H20=Ca(OH)2+2H2↑),请回答下列问题:
(1)反应生成的氢气质量为_______________。
(2)计算样品中氢化钙的质量分数____________。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图中 A、B、C、D、E、F 是初中常见物质,其 中 A、B、C、D、E 是五种不同类别的物质,D 是氧化物, 且 D 中两种元素的质量比为 3:8。图中“—”表示两端物质间能 发生化学反应,“→”表示物质间存在转化关系;反应条件、 部分反应物和生成物已略去。
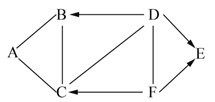
(1)D 物质是_____(填写化学式)。
(2)写出 B 与 C 反应的化学方程式:_____。
(3)写出 F→E 的化学反应方程式:_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】阅读下面科普短文。
一段时间以来,网传隔夜菜、肉类腌制品不能吃,是因为含亚硝酸盐。对于亚硝酸盐大 家有众多疑问。
疑问一:亚硝酸盐是什么东西? 亚硝酸盐是一类无机化合物的总称,主要指亚硝酸钠(NaNO2),它是白色或淡黄色粉末,有咸味,易溶于水。它是一种常见的食品添加剂,广泛用于各种火腿、酱卤肉等熟肉类食品加工,作为防腐剂和护色剂。国家对食品中含有的亚硝酸盐的最大含量限定为:蔬菜4mg/kg,肉类 3mg/kg。
疑问二:亚硝酸盐的“毒”从何来?
亚硝酸盐本身并无致癌效应,它被吸入血液 1~5 分钟后,就已经分解。亚硝酸盐在胃中酸性环境下,易与氨基酸的分解产物发生反应,产生致癌物。当摄入维生素 C 时可以阻止 致癌物产生。
疑问三:隔夜菜中的亚硝酸盐含量会超标吗? 实验人员准备了清炒菠菜、清炒芹菜和小白菜炒肉,三种菜各自被分成 6 份,常温和冷藏条件下各保存一半。实验人员分别取 1 小时后、6 小时后、20 小时后的剩菜,经过捣碎、提取、离心、过滤,取出汤汁。通过比色法逐一测得样品中亚硝酸盐含量,如下图所示。
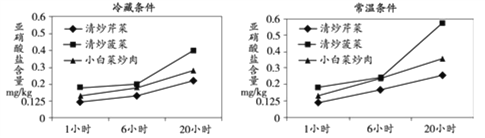
实验结果表明,三种菜在放置 20 小时后,无论常温还是冷藏,亚硝酸盐含量虽均有增 加,但都远未超过国家标准。
疑问四:摄入多少亚硝酸盐会对人体产生危害?
人体对亚硝酸盐的一次性安全摄入量为每千克体重 0.2 mg。我们日常吃的大米、蔬菜、 肉品里面几乎都含有亚硝酸盐。有数据显示,人体摄入的亚硝酸盐 80%来自蔬菜。如果你 体重 50 kg,即使一次性吃 2.5 kg 蔬菜也是安全的。因此,将亚硝酸盐摄入量控制在安全范 围内不会对人体造成危害。
依据文章内容,回答下列问题。
(1)亚硝酸钠中氮元素的化合价为_____。
(2)人体对亚硝酸盐的一次性安全摄入量为____________。
(3)下列有关说法正确的是_____。
A.“吃隔夜菜会致癌”是没有科学依据的
B.常温储存及冷藏储存条件下,亚硝酸盐含量均呈增加趋势
C.适量吃富含维生素的新鲜蔬菜水果,有利于抑制致癌物的产生
D.从实验数据中发现蔬菜类的隔夜菜亚硝酸 盐含量要高于含肉类的隔夜菜
(4)亚硝酸钠是实验室常用的试剂,实验室 一般用亚硝酸钠溶液与氯化铵溶液反应来制 取 N2。N2 的化学性质十分稳定,但在一定条件下能与 H2 部分化合生成 NH3。如图为制取少量 NH3 的装置(获取 H2 的装置已略去):
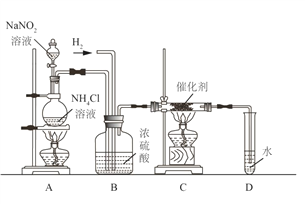
①C 装置的硬质试管中发生反应的化学方程 式为________________。
②反应时 N2 和 H2 的质量比____________如果按此比例进行反应,反应时,D 中导管口有气泡逸出,说明逸出气泡的原因(已知 NH3极易溶于水):_________。
③B 中浓硫酸的作用是________。
④用实验方法证明确实有 NH3 生成________。
查看答案和解析>>
科目: 来源: 题型:
【题目】我国著名的化学家侯德榜发明的“侯氏制碱法”,是向饱和食盐水中通入过量氨气,再通入过量的二氧化碳,即可析出 NaHCO3 固体,将其加热得到纯碱。其原理流程如下 图所示:
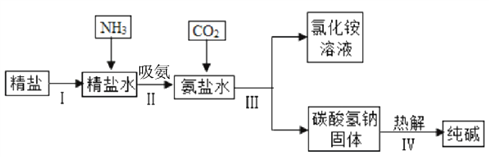
(1)操作Ⅲ的名称是_____。
(2)氨气极易溶于水,向饱和食盐水通入氨气可得到饱和食盐水和氨水的混合盐水(称为 氨盐水)。氨盐水比食盐水更容易吸收二氧化碳,其原因是_____;
(3)写出制取碳酸氢钠的化学方程式_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下列是化学兴趣小组用过氧化氢制取氧气的实验,目的是探究影响化学反应快慢的因素,相关数据如下表所示(“常温”通常是指20℃;“浓度”指溶质的质量分数):
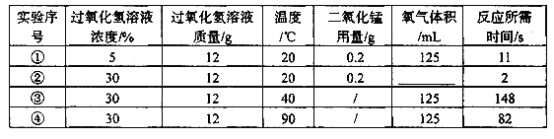
(1)表格中②的氧气体积为____mL,通过以上实验对比可知,化学反应快慢与温度的关系为___________。
(2)由上述实验可知,实验室用过氧化氢制取氧气最适合的条件是___________(填序号)。
(3)定量比较反应快慢,除了表格中的方法外,还可以采用______。写出该反应的化学方程式_____。
(4)如果要证明二氧化锰在化学反应前后的化学性质不变,可用什么实验方法?请写出实验的步骤、现象和结论_________。
(5)查阅资料可知:氧化铜也能加快过氧化氢的分解反应速率,给你一根铜丝、酒精灯、坩埚钳、石棉网、火柴、试管、5%过氧化氢溶液等。请你设计实验探究影响过氧化氢分解速率的因素,并写出实验步骤和实验现象。_________、_____________
查看答案和解析>>
科目: 来源: 题型:
【题目】水和溶液在生产、生活中起着十分重要的作用。请回 答下列问题:
(1)对于静置沉淀、吸附沉淀、过滤、蒸馏等净化水的操作中,单一操作相对净化程度较高的是________。
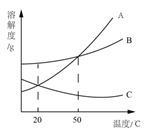
(2)根据右图 A、B、C 三种固体的溶解度曲线回答:
①50℃时,等质量的 A、C 的饱和溶液中溶剂的质量大小关系为: A_____C(填“>”、“=”或“<”)。
②将三种物质饱和溶液的温度分别从 50℃降到 20℃时,溶液中溶质的质量分数最大的 是_____________
(3)若要配制 98g 质量分数为 10%的稀硫酸,需要质量分数为 98%的浓硫酸(密度为1.84g/cm3)_____mL(计算结果保留一位小数)。在实验室用浓硫酸配制稀硫酸的主要步 骤有:计算、量取、_____、冷却至室温装瓶并贴上标签。
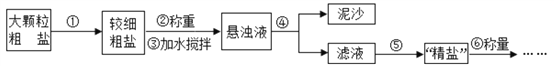
(4)粗盐提纯的步骤如下:
a.操作⑤中用到的仪器有铁架台、玻璃棒、酒精灯、坩埚钳、_________,其中玻璃棒的作用 是______________。
b. 实验结束后称量获得的精盐,并计算精盐的产率,发现产率偏低,其可能的原因是___________。
A、食盐没有全部溶解即过滤 B、蒸发时食盐飞溅剧烈
C、蒸发后,所得精盐很潮湿 D、器皿上沾有的精盐没全部转移到称量纸上
查看答案和解析>>
科目: 来源: 题型:
【题目】请结合下图回答问题:
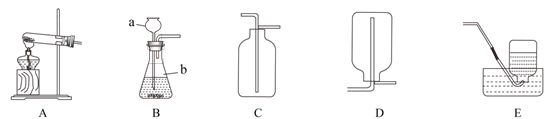
(1)标出仪器 a 的名称_____。
(2)实验室通常利用上图中_____装.置.的.组.合.制取二氧化碳(选填字母),该反应的化学方程式为_____________。
(3)选用 E 装置收集氧气的原因是_____。
(4)工业上煅烧石灰石可制得生石灰和二氧化碳。如果要制取 5.6t 氧化钙,理论上需要含 碳酸钙 80%的石灰石的质量是多少________?
查看答案和解析>>
科目: 来源: 题型:
【题目】下列四个图像不能正确反映其对应实验操作的是( )
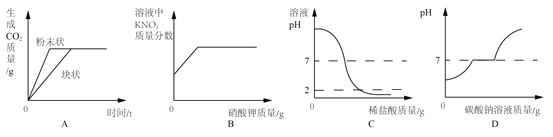
A. 等质量碳酸钙分别与等体积等质量分数的稀盐酸(足量)反应
B. 20℃时,向一定量不饱和的硝酸钾溶液中加入过量的硝酸钾晶体
C. 向一定量的氢氧化钠溶液中逐滴加入 pH=2 的稀盐酸至过量
D. 向盐酸和氯化钙的混合溶液中滴加碳酸钠溶液
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组将打印机墨盒中的墨粉倒出,发现全部是黑色粉末,于是对墨粉的成分进行下列探究:
【提出猜想】该粉末可能含有炭粉、铁粉、氧化铁、四氧化三铁中的一种或几种。
(1)小明认为不可能含有氧化铁,原因是 __________________
【查阅资料】①四氧化三铁具有磁l生,能被磁铁吸引;
②金属氧化物能溶于稀酸。

______________
【进行实验】
(2)用化学方程式表示实验③中澄清石灰水变浑浊的原因________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com