
科目: 来源: 题型:
【题目】自来水消毒过程中常发生下列转化:
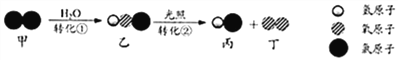
下列说法正确的是 ( )
A. 反应前后分子不可分 B. 转化①是化合反应
C. 转化②中丙和丁的分子个数之比为1︰1 D. 转化①、②中氯元素的化合价都发生变化
查看答案和解析>>
科目: 来源: 题型:
【题目】根据如图物质的溶解度曲线,判断下列说法正确的是

A. 将乙的饱和溶液过滤,能得到不饱和溶液
B. t1℃时,甲溶液、乙溶液的溶质质量相等
C. t2℃185g甲溶液降温至t1℃时,能析出49g晶体
D. 将26%的甲溶液从t2℃降温到t1℃时,溶质质量分数不变
查看答案和解析>>
科目: 来源: 题型:
【题目】海洋是一个远未完全开发的巨大化学资源宝库,海洋资源的综合利用具有非常广阔的前景。工业上从海水中可提取许多广泛应用于生活、生产、科技等方面的物质和原料。
Ι.从海水中获得淡水
下列方法常用于海水淡化的是____________(填字母)。
A.蒸馏法 B.吸附法 C.沉淀法 D.过滤法
Ⅱ.从海水中提取溴(Br2)
工业上通常是将氯气通入海水晒盐后的母液中,将溶液中的溴化钠(NaBr)转化为溴单质(Br2),然后鼓入热空气,使溴单质(Br2)从溶液中挥发出来,冷凝后得到粗溴。该过程中主要反应的化学方程式为_______________________,其反应类型是______________。
Ⅲ.从海水中提取金属镁
镁及其合金是一种用途很广的金属材料,工业上从海水晒盐后的母液中提取镁的主要流程如下:
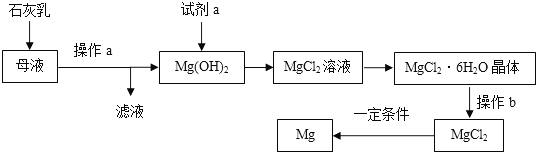
试回答下列问题:
(1)石灰乳主要成分的化学式为_____________。
(2)Mg(OH)2中加入试剂a发生反应的化学方程式为____________________________。
(3)操作b是在HCl气体氛围中高温灼烧进行的。若直接灼烧MgCl2·6H2O晶体,则生成MgO和另外两种化合物,写出有关反应的化学方程式___________________________ 。
Ⅳ.以海水中提取的食盐为原料制备纯碱
制备过程中主要涉及以下三步反应:
① CO2+NH3+H2O ══NH4HCO3
② NH4HCO3 + NaCl══NaHCO3 ↓ + NH4Cl
③ 2NaHCO3 ![]() Na2CO3+ CO2 ↑ + H2O
Na2CO3+ CO2 ↑ + H2O
试回答下列问题:
(1)制备过程中可以直接循环回收利用的物质是H2O和__________________。
(2)在实验室里证明反应③中的NaHCO3已完全分解的具体操作是________。
(3)某化学兴趣小组认为,在碳酸氢钠完全分解的情况下,所得的纯碱中也会混有来自反应②中的杂质,为此他们进行了如下探究:
a.取2.2g纯碱样品,加水完全溶解得100g溶液;
b.配制100g 3.65%的稀盐酸;
c.取上述一种溶液25g于锥形瓶中,再将另一种溶液逐滴加入锥形瓶内,反应后溶液的pH变化情况如下图所示。
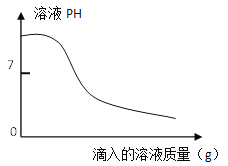
步骤c中当滴入另一种溶液为10g时,锥形瓶内物质恰好完全反应。则纯碱样品中碳酸钠的质量分数为___________(写出计算过程,计算结果保留1位小数)
查看答案和解析>>
科目: 来源: 题型:
【题目】高纯氧化铁可作现代电子工业的材料。以下是以硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程图。
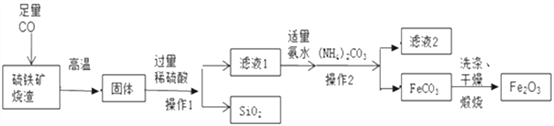
(1)实验室中,操作1、操作2用到的玻璃仪器有玻璃棒、烧杯、_____等。
(2)滤液1中主要的阳离子是 ______________。(写2种)
(3)滤液1中加氨水要适量,若氨水不足,则硫酸不能完全反应;若氨水过量,则__________________。
(4)滤液2中可回收的产品是____________(写化学式)。
(5)写出在空气中煅烧FeCO3的化学反应方程式______________________________
查看答案和解析>>
科目: 来源: 题型:
【题目】请根据下图所示的实验装置图填空。
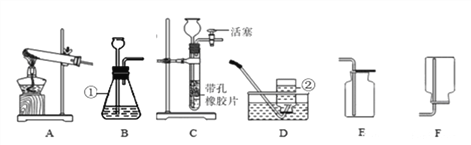
(1)B图中①的仪器名称为___________。
(2)实验室用高锰酸钾制取氧气,选用的发生装置为_______,该装置还应作的的一点改进是__________,该反应的方程式为_________________________。
(3)实验室制取二氧化碳的化学方程式为___________________,在装药品前应先进行的操作是___________。若用C装置制取CO2气体, 在反应过程中,使反应停止的操作是________________________。
(4)实验室常用加热醋酸钠和碱石灰的固体混合物来制取甲烷气体。甲烷是一种无色无味、密度比空气小、极难溶于水的气体,则制取并收集甲烷的装置组合是__________,若用下图装置收集甲烷,气体应从_______端导入(选填“a”或“b”)。

(5)实验室用锌粒和稀盐酸制得的氢气不纯,常含有水蒸气和_______(填化学式)。为制取纯净、干燥的氢气,化学兴趣小组同学对锌粒和稀盐酸制氢气的装置进行补充和完善,实验装置图如下。请回答下列问题。

①H中硝酸银溶液的作用是___________;②I中液体是__________(填名称)
查看答案和解析>>
科目: 来源: 题型:
【题目】“细菌冶金”的原理是利用氧化铁硫杆菌促使黄铁矿(主要成分FeS2)氧化成硫酸铁和硫酸,并为CO2和H2O合成有机物提供能量,流程如下图。下列说法错误的是 ( )
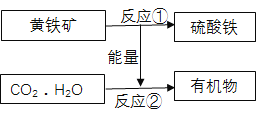
A. 氧化铁硫杆菌在反应①中起催化作用
B. 整个流程提高了能量的利用率
C. 图中有机物可能含碳、氢、氧元素
D. 反应①化学方程式:4FeS2+15O2+2X=2Fe2(SO4)3+2H2SO4,X为H2O2
查看答案和解析>>
科目: 来源: 题型:
【题目】向一定质量AgNO3和Cu(NO3)2的混合溶液中加入Zn,溶液质量与加入Zn的质量关系如图所示,下列说法正确的是 ( )

A. a点溶液中的溶质有2种
B. c点溶液中溶质为Zn(NO3)2
C. 若取b~c段溶液,滴加稀盐酸,有白色沉淀
D. d点存在的金属有Ag和Cu两种
查看答案和解析>>
科目: 来源: 题型:
【题目】自来水消毒过程中常发生下列转化:
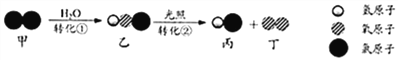
下列说法正确的是 ( )
A. 反应前后分子不可分 B. 转化①是化合反应
C. 转化②中丙和丁的分子个数之比为1︰1 D. 转化①、②中氯元素的化合价都发生变化
查看答案和解析>>
科目: 来源: 题型:
【题目】根据如图物质的溶解度曲线,判断下列说法正确的是

A. 将乙的饱和溶液过滤,能得到不饱和溶液
B. t1℃时,甲溶液、乙溶液的溶质质量相等
C. t2℃185g甲溶液降温至t1℃时,能析出49g晶体
D. 将26%的甲溶液从t2℃降温到t1℃时,溶质质量分数不变
查看答案和解析>>
科目: 来源: 题型:
【题目】某小组同学对碳酸氢钠、碳酸钠、氢氧化钠的某些性质进行探究。
【提出问题】①三种溶液的酸碱性?
②它们与酸反应时溶液的pH如何变化?
【查阅资料】
pH | 2~3 | 4~6 | 7 | 8~9 | 10~11 | 12~14 |
紫甘蓝汁液显示的颜色 | 紫红 | 浅紫 | 紫色 | 蓝色 | 绿色 | 黄色 |
【实验1】向等体积、等浓度的碳酸氢钠、碳酸钠、氢氧化钠溶液中,分别加入几滴紫甘蓝汁液,同时用蒸馏水进行对比实验,观察并记录现象如下:
液体名称 | 蒸馏水 | 碳酸氢钠溶液 | 碳酸钠溶液 | 氢氧化钠溶液 |
紫甘蓝汁液显示的颜色 | 紫色 | 蓝色 | 绿色 | 黄色 |
【实验2】向一定体积、一定浓度的氢氧化钠溶液中,逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图1所示。
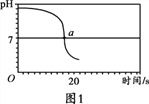
【实验3】向等体积、含等碳原子数的碳酸氢钠和碳酸钠溶液中,分别逐滴加入一定浓度的盐酸,测得pH变化与时间的关系如图2、图3所示。将图2与图3的阴影部分进行叠加,发现两者基本重合。

【解释与结论】
(1)实验1得出三种溶液的碱性由强到弱的顺序为________________。
(2)实验2证明了氢氧化钠能与盐酸发生反应,其理由是_________,实验结束,向反应后的溶液中滴加紫甘蓝汁液,观察到的现象是_________。
(3)实验3中,b点的溶质为_________,c点后发生反应的化学方程式为_________。
(4)依据实验3获取的信息,鉴别Na2CO3和NaHCO3固体的实验方案为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com