
科目: 来源: 题型:
【题目】家庭养观赏鱼时会在鱼缸里放点“鱼浮灵”,可使水中的含氧量迅速增加。“鱼浮灵”
主要成分是过碳酸钠(xNa2CO3 yH2O2),俗称固体双氧水。某化学兴趣小组对其进行探究。
Ⅰ. “鱼浮灵”的性质研究
实验1:取少量“鱼浮灵”于试管中加水,有持续细小气泡缓慢放出;继续向试管中加有少量MnO2粉末,产生大量气泡。将带火星的木条伸入试管,木条_____________,说明有O2生成,该反应的化学方程式为____________________________。
实验2:取实验1中上层清液,测得溶液pH > 7,说明溶液呈____性(填“酸”、“碱”或“中”);向溶液中滴加足量稀盐酸,产生大量气泡,将产生的气体通入澄清石灰水中,出现浑浊现象,说明有_________生成。
结论:过碳酸钠具有Na2CO3和H2O2的双重化学性质。
Ⅱ. “鱼浮灵”的制备研究
“鱼浮灵”的工业制备流程如下:
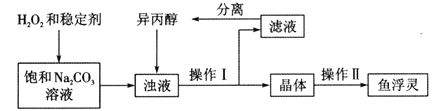
【查阅资料】 异丙醇为有机溶剂,水与异丙醇可以互溶,过碳酸钠在异丙醇中溶解度较小。
稳定剂中MgCl2和 Na2SiO3发生复分解反应,生成一种难溶物将过碳酸钠粒子包裹住,该反应的化学方程式为_________。浊液中加入异丙醇的作用是________。
Ⅲ. “鱼浮灵”的组成研究
利用下图装置进行产品过碳酸钠(xNa2CO3 yH2O2)组成的测定(杂质对测定无影响)。

⑴实验前先缓慢通N2一段时间,加热铜网至红热后,再缓慢滴入过量稀硫酸,直至A中样品完全反应,继续缓慢通N2。继续缓慢通N2的目的是________。
⑵B装置中浓硫酸的作用是_________________________________;
E装置的作用是________________________________________。
⑶若先滴入稀硫酸,后加热铜网,会导致x : y的值__________ (填“偏大”或“偏小”)。
⑷实验测得C装置中铜网增重1.2g,D装置增重2.2g,则x : y =_______。 (写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
【题目】孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。以孔雀石为原料可制备CuSO4 5H2O及纳米材料CaCO3,步骤如下:
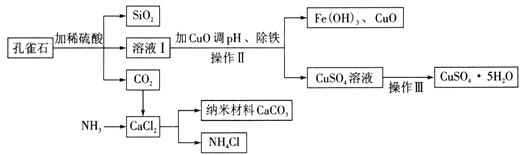
请回答下列问题:
(1)写出Cu2(OH)2CO3与稀硫酸反应的化学方程式:________ 。
(2)操作Ⅱ的名称为 __________ 。
(3)由CuSO4溶液获得CuSO45H2O,需要经过蒸发浓缩、_______ 、过滤、洗涤、干燥等操作。在实验室进行“蒸发浓缩”时,除铁架台、蒸发皿、酒精灯外,还用到另一玻璃仪器,该仪器是_________。
(4)制备纳米材料CaCO3时,应向CaCl2溶液中先通入NH3,后通入CO2。请写出该反应的化学方程式:_______________。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下列实验装置图,回答有关问题。
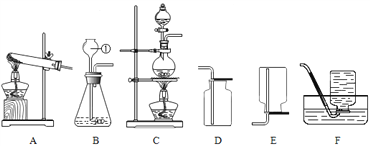
⑴写出仪器①的名称_____。
⑵实验室用A装置加热高锰酸钾制取O2的化学反应方程式为_______,还应对该装置进行的改进是________。实验室常用锌粒和稀硫酸反应制取氢气,若要得到一瓶较纯净的氢气,应选择的装置组合是___________。
⑶张老师要制取一瓶氯气(Cl2),反应原理是:MnO2 + 4HCl(浓) ![]() MnCl2 + Cl2↑ + 2H2O。
MnCl2 + Cl2↑ + 2H2O。
已知常温下,氯气是一种黄绿色有刺激性气味的有毒气体,密度比空气的大,易与水反应生成盐酸和次氯酸(HClO)。张老师应选择的发生装置是____(填装置的字母代号),写出氯气与水反应的化学方程式__________。
⑷兴趣小组在做完盐的性质实验后,发现一瓶碳酸钠固体可能混入了氯化钠、硫酸钠中的一种或两种,为此,他们对这瓶固体的成分进行了探究。
Ⅰ.实验验证:
①取少量该样品于烧杯中,加入适量的水,溶解,得到溶液A。
②取少量溶液A于试管中,先滴入过量的稀硝酸,再滴入过量的硝酸钡溶液,充分反应后,静置。观察到先产生_______,后产生________,说明该固体中混有硫酸钠。
③取步骤②中的上层清液于试管中,滴入几滴硝酸银溶液。观察到产生白色沉淀,说明该固体中还混有_____。该步实验结束所得溶液中一定含有的阳离子是_____。
Ⅱ.实验拓展:兴趣小组还想测定该固体中碳酸钠的质量分数,利用如图所示的实验装置(气密性良好)进行实验,每一步反应均完全进行。
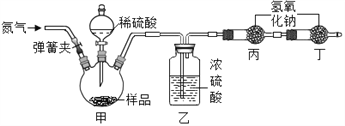
为达到实验目的,首先称取一定质量的该固体样品放入装置甲中,然后进行有关实验操作,正确的顺序是___(填序号,可重复)。
a.称量装置丙
b.打开弹簧夹,通入足量的氮气,关闭弹簧夹
c.打开分液漏斗的活塞,注入足量的稀硫酸,关闭活塞
查看答案和解析>>
科目: 来源: 题型:
【题目】(4分)某地一辆满载浓硫酸的罐车翻倒,导致溶质质量分数为98%的浓硫酸20t泄漏,并向路基两边蔓延。接到报警后消防官兵立即赶来并用石灰浆(主要成分为氢氧化钙)中和硫酸解除了险情。请回答:
(1)溶质质量分数为98%的浓硫酸20t中含H2SO4的质量是 ;
(2)计算中和泄漏的98%浓硫酸20t,理论上需要氢氧化钙的质量。
查看答案和解析>>
科目: 来源: 题型:
【题目】(9分)某研究性学习小组在验证“碱使酚酞试液变红”的实验时,发现一个意外现象:将酚酞试液滴入某NaOH溶液中,溶液变成了红色,可是过一会儿红色却消失。
【提出问题】是什么原因导致滴有酚酞的NaOH溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能是酚酞与O2发生了反应;
乙同学:可能是NaOH溶液与空气中的CO2发生了反应;
丙同学:可能与 大小有关;
【设计实验】三位同学分别设计实验验证自己的猜想:
(1)甲同学设计了如下实验,请你填写下表。
实验步骤 | 设计这一步骤的目的 | 实验现象 | 实验结论 |
①将NaOH溶液加热煮沸 | ① | 溶液变红,过一会儿红色消失 | 甲同学猜想___________(填“正确”或不正确”)新课 |
②向冷却后的溶液中滴人酚酞,并滴一些植物油在其上方 | ② |
(2)乙同学设计如图一装置进行实验,一段时间后,试管中溶液的红色褪去,于是认定自己的猜想正确。写出CO2与NaOH溶液反应的化学方程式: 。
甲同学认为乙同学的实验不够严谨,理由是: 。
(3)丙同学使用了色度传感器测溶液的颜色。他在a、b、c三个比色皿中分别加入等量5%、10%、20%的NaOH溶液,然后各滴加2滴酚酞试液。溶液颜色的变化曲线如图[说明:溶液无色时色度值(透过率)为100%]。请你观察图二写出规律性结论:_____________________ 。
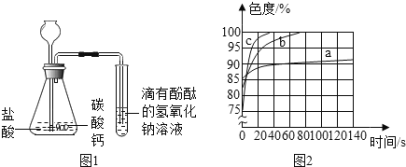
查看答案和解析>>
科目: 来源: 题型:
【题目】小维与家人聚餐时,对火锅燃料“固体酒精”产生了好奇,于是他与同学对其成分进行如下探究.
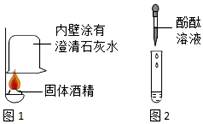
【查阅资料】(1)该固体酒精是用酒精、氯化钙和氢氧化钠按一定的质量比混合制成的.
(2)氯化钙、氯化钡溶液均呈中性.
【提出问题】(1)酒精中是否含有碳元素?
(2)固体酒精中氢氧化钠是否变质?
【作出猜想】猜想一:酒精中含有碳元素.
猜想二:固体酒精中氢氧化钠已变质.
【实验探究】(1)如图1所示进行实验,发现澄清石灰水___________,可得出酒精中含有碳元素的结论.
(2)取少量固体酒精于烧杯中,加足量的水充分溶解后静置,发现杯底有白色沉淀.取沉淀于试管中加入稀盐酸,固体溶解并有气泡产生,则生成气体的化学方程式_________________.
【实验结论】(1)酒精中含有碳元素.
(2)固体酒精中氢氧化钠已经变质.
【拓展延伸】为进一步确定固体酒精中是否还含有氢氧化钠,小维与同学继续探究.
(1)他另取少量固体酒精,加水溶解后,取上层清液,滴加酚酞溶液,酚酞溶液__________,于是得出固体酒精中还含有氢氧化钠.
(2)小维的同学认为他的实验不能证明固体酒精中一定有氢氧化钠剩余,理由是______.
(3)他们另取上层清液,加入足量的氯化钡溶液,充分反应后滴加氯化铁溶液,生成红褐色沉淀,他们一致认为固体酒精中氢氧化钠有剩余.
【反思交流】(1)实验中,加入足量氯化钡溶液的目的是_______________.
(2)想要熄灭火锅中的固体酒精,可用盖子盖上,其灭火原理是_________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】石膏(CaSO42H2O)是一种用途广泛的工业材料和建筑材料,工业上用含SO2的烟气制备石膏的简要流程图如下:
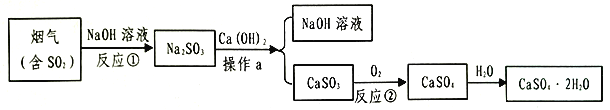
(1)在反应①时,常将NaOH喷成雾状的原因是___________________.
(2)操作a的名称是__________,在实验室里进行该操作,玻璃棒的作用是__________.
(3)CaSO3不易溶于水,它属于________(填“酸”、“碱”、“盐”或“氧化物”),其中硫元素的化合价为________,反应②的化学方程式是_________________________.
(4)生产流程中生成的______________可循环利用,节约成本.
查看答案和解析>>
科目: 来源: 题型:
【题目】根据如图实验装置回答问题。
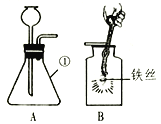
(1)仪器①的名称是_______。实验室用装置A制取氧气的化学方程式为______。该装置_____(选填“能”或“否”)用于实验室制取氢气。
(2)研究显示:O2的体积分数大于36%时就可以使带火星的木条复燃。因此,O2验满时采用使带火星的木条复燃的方法_______(填“可靠”或“不可靠”)。为了收集一瓶较纯净的O2,最好采用_______集气法。
(3)将收集到的氧气用来做铁丝燃烧的实验,如装置B,但该装置存在缺陷,你改进的措施是________.
查看答案和解析>>
科目: 来源: 题型:
【题目】2016年12月26日,合肥地铁一号线正式通车,实现了我省地下交通的新突破.根据如图回答下列问题:

(1)图中所示材料中,属于金属材料的是_____(填一种即可,下同);属于有机合成材料的是___;石墨电刷的使用主要利用其_________性.地铁车身的表面都喷上一层油漆,目的是为了防止铁与空气中的_______________发生反应而生锈.
(2)冶炼金属钛时,将钛铁矿石转化为TiCl4,TiCl4再与Na在一定条件下反应生成Ti和NaCl.请写出后一步反应的化学方程式:________________________________(不要求标出反应条件).
(3)轨道交通的发展减轻了公共交通及私家车带来的拥堵问题,从化学的角度来看,你认为发展轨道交通还有什么好处?_____________________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两种物质的溶解度曲线如图所示.下列说法不正确的是( )
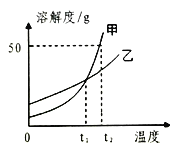
A. t2℃时,甲的溶解度大于乙的溶解度
B. t2℃时,将30g甲物质加入50g水中充分溶解后得到75g饱和溶液
C. t1℃时,甲、乙两种饱和溶液的溶质质量分数相等
D. t2℃时甲、乙的饱和溶液降温到t1℃时,析出晶体的质量甲一定大于乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com