
科目: 来源:不详 题型:单选题
| 温度℃ | 25 | 80 | 230 |
| 平衡常数 | 5×104 | 2 | 1.9×10-5 |
| A.上述生成Ni(CO)4(g)的反应为吸热反应 |
| B.25℃时反应Ni(CO)4(g)?Ni(s)+4CO(g)的平衡常数为0.5 |
| C.在80℃时,测得某时刻,Ni(CO)4、CO浓度均为0.5mol/L,则此时v(正)>v(逆) |
| D.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2mol/L |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 3 |
| 2 |
| 1 |
| 2 |
A.a-
| B.
| C.a
| D.aˉ2 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 1 |
| 2 |
| 1 |
| 2 |
| A.K1=2K2 | B.K1=K22 | C.K1=
| D.K1=
|
查看答案和解析>>
科目: 来源:不详 题型:单选题
A.反应①的平衡常数K1=
| ||
B.反应③的平衡常数K=
| ||
| C.对于反应③,恒容时,温度升高,H2 的浓度减小,则该反应的焓变为正值 | ||
| D.对于反应③,恒温恒容下,增大压强,H2 的浓度一定减小 |
查看答案和解析>>
科目: 来源:不详 题型:多选题
| T1 |
| T2 |
| A.灯管工作时,扩散到灯丝附近高温区的WI2(g)会分解出W,W重新沉积到灯丝上 | ||
| B.灯丝附近温度越高,WI2(g)的转化率越低 | ||
C.该反应的平衡常数表达式:K=
| ||
| D.利用该反应原理可以提纯钨 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
A.平衡常数为K=
| ||
| B.反应2NO2(g)?N2O4(g)△H<0,升高温度,该反应平衡常数增大 | ||
| C.对于给定可逆反应,温度一定时,其正、逆反应的平衡常数相等 | ||
| D.改变条件,反应物的转化率增大,平衡常数也一定增大 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
| A.电离平衡常数受溶液浓度的影响 | ||
| B.电离平衡常数可以表示弱电解质的相对强弱 | ||
| C.电离常数大的酸溶液中c(H+)一定比电离常数小的酸中大 | ||
D.H2CO3的电离常数表达式:K=
|
查看答案和解析>>
科目: 来源:朝阳区一模 题型:单选题
| 起始浓度 | c(H2)/mol/L | c(I2)/mol/L | c(HI)/mol/L |
| 甲 | 0.01 | 0.01 | 0 |
| 乙 | 0.02 | 0.02 | 0 |
| A.平衡时,乙中H2的转化率是甲中的2倍 |
| B.平衡时,甲中混合物的颜色比乙中深 |
| C.平衡时,甲、乙中热量的变化值相等 |
| D.该温度下,反应的平衡常数K=0.25 |
查看答案和解析>>
科目: 来源:不详 题型:问答题
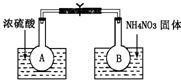
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 温度/℃ | 400 | 500 | 830 | 1000 |
| 平衡常数K | 10 | 9 | 1 | 0.6 |
| A.正反应是吸热反应 |
| B.830℃时,反应达到平衡,[CO]=[CO2] |
| C.恒温时缩小容器体积使压强增大,正反应速率增大 |
| D.400℃时,恒容反应器中投入CO、H2O、H2、CO2物质的量分别为5 mol、1 mol、2 mol、3mol,反应向逆方向进行 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com