
科目: 来源:不详 题型:填空题
| 压强(kPa) | 13.33 | 53.32 | 101.3 |
| K的沸点(℃) | 590 | 710 | 770 |
| Na的沸点(℃) | 700 | 830 | 890 |
| KCl的沸点(℃) | 1437 | ||
| NaCl的沸点(℃) | 1465 |
查看答案和解析>>
科目: 来源:不详 题型:单选题
| 1 |
| 2 |
| 1 |
| 2 |
A.
| B.2401 | C.7 | D.
|
查看答案和解析>>
科目: 来源:杭州二模 题型:填空题
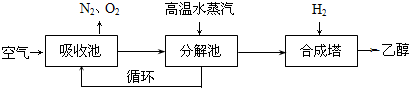
| 温度(K) CO2转化率(%) n(H2)/n(CO2) |
500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2 | 60 | 43 | 28 | 15 |
| 3 | 83 | 62 | 37 | 22 |
| n(H2) |
| n(CO2) |
查看答案和解析>>
科目: 来源:不详 题型:问答题
查看答案和解析>>
科目: 来源:不详 题型:填空题
| c(CO) |
| c(CO2) |
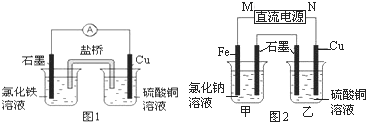
查看答案和解析>>
科目: 来源:不详 题型:问答题
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | Ka=1.8×10-5 | Ka1=4.3×10-7 | Ka2=5.6×10-11 | Ka=3.0×10-8 |
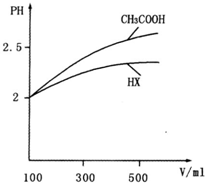
查看答案和解析>>
科目: 来源:不详 题型:问答题

查看答案和解析>>
科目: 来源:0111 期中题 题型:单选题
 PCl3 (g)+Cl2 (g) ,反应达到平衡时,混合气体中PCl5所占体积分数为M%。若同一温度的同一容器中,最初投入2 molPCl5,反应达平衡时,混合气体中PCl5所占体积分数为N%。则M和N的关系是
PCl3 (g)+Cl2 (g) ,反应达到平衡时,混合气体中PCl5所占体积分数为M%。若同一温度的同一容器中,最初投入2 molPCl5,反应达平衡时,混合气体中PCl5所占体积分数为N%。则M和N的关系是[ ]
查看答案和解析>>
科目: 来源:0111 期中题 题型:单选题
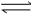 mZ(气)+nR(气),达平衡时,Z的体积分数为φ1,维持温度不变,若把3 molX和2molY放入另一体积相同的密闭容器,达平衡时,Z的体积分数为φ2,则φ1与φ2的关系为
mZ(气)+nR(气),达平衡时,Z的体积分数为φ1,维持温度不变,若把3 molX和2molY放入另一体积相同的密闭容器,达平衡时,Z的体积分数为φ2,则φ1与φ2的关系为[ ]
查看答案和解析>>
科目: 来源:0103 月考题 题型:单选题
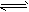 2SO3,平衡时SO3为wmol。相同温度下分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3物质的量等于wmol的是
2SO3,平衡时SO3为wmol。相同温度下分别按下列配比在相同体积的容器中反应,反应达到平衡时,SO3物质的量等于wmol的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com