
科目: 来源:0127 模拟题 题型:单选题
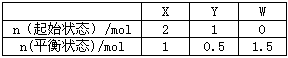
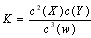
查看答案和解析>>
科目: 来源:0118 期中题 题型:填空题
 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a到b过程中改变的条件可能是:_____________________;b到c过程中改变的条件可能是
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a到b过程中改变的条件可能是:_____________________;b到c过程中改变的条件可能是
查看答案和解析>>
科目: 来源:天津高考真题 题型:单选题
 SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如所示。由图可得出的正确结论是
SO3(g)+NO(g)达到平衡,正反应速率随时间变化的示意图如所示。由图可得出的正确结论是 
查看答案和解析>>
科目: 来源:0114 月考题 题型:单选题
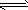 CO(g) + H2(g)的描述正确的是
CO(g) + H2(g)的描述正确的是查看答案和解析>>
科目: 来源:模拟题 题型:不定项选择题
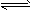 CH3OH(g) 过程中能量的变化如图示。下列判断正确的是
CH3OH(g) 过程中能量的变化如图示。下列判断正确的是 
查看答案和解析>>
科目: 来源:0104 模拟题 题型:填空题
 O2+Hb·CO 实验表明,c(Hb·CO)即使只有c(Hb·O2)的1/50,也可造成人的智力损伤。已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2mol·L-1,若使c(Hb·CO)小于c(Hb·O2)的1/50,则吸入肺部CO的浓度不能超过_________mol·L-1。
O2+Hb·CO 实验表明,c(Hb·CO)即使只有c(Hb·O2)的1/50,也可造成人的智力损伤。已知t℃时上述反应的平衡常数K=200,吸入肺部O2的浓度约为1.0×10-2mol·L-1,若使c(Hb·CO)小于c(Hb·O2)的1/50,则吸入肺部CO的浓度不能超过_________mol·L-1。 N2(g) + 2CO2(g) △H=-113kJ·mol-1
N2(g) + 2CO2(g) △H=-113kJ·mol-1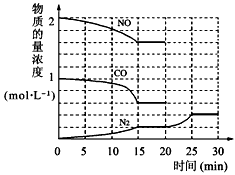
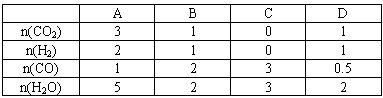
 H2(g)+CO2(g)的平衡常数随温度的变化如下表:
H2(g)+CO2(g)的平衡常数随温度的变化如下表: 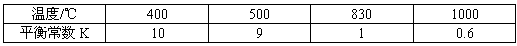
查看答案和解析>>
科目: 来源:山西省模拟题 题型:单选题
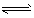 zC(g),达平衡后测得A气体的浓度为0.50 mol/L。恒温下将容器体积扩大1倍,反应重新达到平衡,测得A浓度为0.20mol/L。下列叙述中正确的是
zC(g),达平衡后测得A气体的浓度为0.50 mol/L。恒温下将容器体积扩大1倍,反应重新达到平衡,测得A浓度为0.20mol/L。下列叙述中正确的是 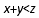
查看答案和解析>>
科目: 来源:模拟题 题型:单选题
 cC(g)+dD(g)达到平衡后,保持温度不变,将容器的体积变为原来的一半,当达到新平衡时,A的浓度变为原平衡的1.5倍,则下列结论正确的是
cC(g)+dD(g)达到平衡后,保持温度不变,将容器的体积变为原来的一半,当达到新平衡时,A的浓度变为原平衡的1.5倍,则下列结论正确的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com