
科目: 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:选择题
下列关于化学平衡常数的说法中,正确的是( )
A.在任何条件下,化学平衡常数都是一个定值
B.化学平衡常数K可以推断一个可逆反应进行的程度
C.化学平衡常数K只与温度、反应物浓度、体系的压强有关
D.当改变反应物的浓度时,化学平衡常数会发生改变
查看答案和解析>>
科目: 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:选择题
全钒电池以惰性材料作电极,在电解质溶液中发生的电池总反应为:VO2+(蓝色)+H2O+V3+(紫色) VO2+(黄色)+V2+(绿色)+2H+ 下列说法错误的( )
VO2+(黄色)+V2+(绿色)+2H+ 下列说法错误的( )
A.充电时,反应每生成2molH+时电子转移的物质的量为2mol
B.放电过程中,正极附近溶液的酸性减弱
C.放电时,正极反应为VO2++2H++e-=VO2++H2O
D.充电时,阳极附近溶液由蓝色逐渐变为黄色
查看答案和解析>>
科目: 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:填空题
密闭容器中加入4 mol A、1.2 mol C和一定量的B三种气体,一定条件下发生反应,各物质的浓度随时间变化如甲图所示[已知t0~t1阶段保持恒温、恒容,且c(B)未画出]。乙图为t2时刻后改变反应条件,反应速率随时间的变化情况,已知在t2、t3、t4、t5时刻各改变一种不同的条件,其中t3时刻为使用催化剂。
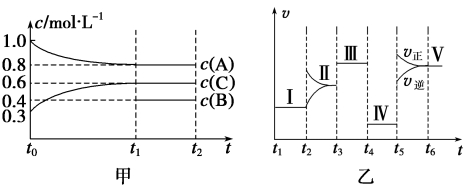
(1)若t1=15 s,则t0~t1阶段的反应速率为v(C)=___________。
(2)t4时刻改变的条件为____________,B的起始物质的量为______________。
(3)t5时刻改变的条件为_____________,该反应的逆反应为__________(填“吸热反应”或“放热反应”)。
(4)图乙中共有Ⅰ~Ⅴ五处平衡,其平衡常数最大的是_____________。
查看答案和解析>>
科目: 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:填空题
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺流程如下:
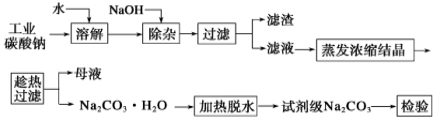
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:

回答下列问题:
(1)滤渣的主要成分为_____________________________。
(2)“趁热过滤”的原因是_________________________。
(3)若在实验室进行“趁热过滤”,可采取的措施是________(写出一种)。
(4)已知:Na2CO3·10H2O (s)===Na2CO3(s)+10H2O(g) ΔH1= +532.36 kJ·mol-1
Na2CO3·10H2O(s)===Na2CO3·H2O(s)+9H2O(g) ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式____________。
查看答案和解析>>
科目: 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:推断题
甲、乙、丙为常见单质。A、B、C、D、E、F、G、H均为中学化学中常见的化合物,其中B、G的焰色反应均为黄色,C能使品红溶液褪色。在一定条件下,各物质相互转化关系如图所示。
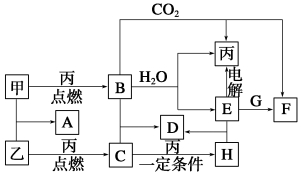
请回答下列问题:
(1)用化学式表示:丙为__________,H为__________。
(2)A的电子式为________________________________。
(3)电解E的水溶液时,E起到的作用是_______________________
(4)写出B+C―→D的化学方程式______________________________
写出E+G―→F的离子方程式___________________________________
查看答案和解析>>
科目: 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:填空题
(1)一定温度下,在恒容密闭容器中N2O5可发生下列反应:
2N2O5(g) 4NO2(g)+O2(g) ΔH>0
4NO2(g)+O2(g) ΔH>0
①反应达到平衡后,若再通入一定量氮气,则N2O5的转化率将________(填“增大”、“减小”或“不变”)。
②下表为反应在T1温度下的部分实验数据:
t/s | 0 | 500 | 1 000 |
c(N2O5)/mol·L-1 | 5.00 | 3.52 | 2.48 |
则500 s内N2O5的分解速率为__________。
③在T2温度下,反应1 000 s时测得NO2的浓度为4.98 mol·L-1,则T2________T1。
(2)如图所示装置可用于制备N2O5,则N2O5在电解池的________区生成,其电极反应式为______________
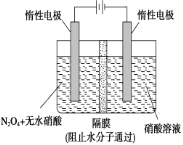
查看答案和解析>>
科目: 来源:2016-2017学年河北省高二上学期9月调研化学试卷(解析版) 题型:填空题
含铬(Cr)工业废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为沉淀。转化过程中,废水pH与Cr2O72-转化为Cr3+的关系如图1所示,实验室模拟工业电解法处理含铬废水的装置如图2所示。
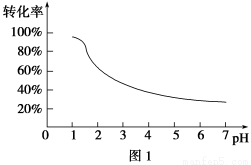
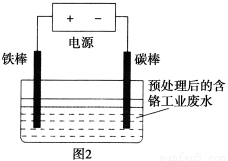
请根据以上知识回答下列问题:
(1)含铬废水预处理的方法是______________。
(2)写出下列反应的离子方程式:
①电解过程中的阴极反应式_________________;
②Cr2O72-转化为Cr3+的离子方程式________________。
查看答案和解析>>
科目: 来源:2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷(解析版) 题型:选择题
下列关于CH4、H2、C三种能源物质的研究方向可行的是( )
A.构成水的氢和氧都是可以燃烧的物质,因此可研究在水不分解的情况下使氢成为二次能源
B.寻找优质催化剂,使CO2与H2O反应生成CH4和O2,并放出热量
C.寻找优质催化剂,利用太阳能使大气中的CO2和海底开采的CH4合成合成气(CO、H2)
D.将固态碳合成C60,以C60作燃料
查看答案和解析>>
科目: 来源:2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数数值,下列叙述中正确的是( )
A.1.8 g的NH4+ 离子中含有的电子数为0.1NA
B.1mol Na2O2 固体中含离子总数为4NA
C.标准状况下,2.24L CCl4所含的共价键数为O.4NA
D.常温常压下,92g NO2和N2O4的混合气体含有的原子数为6NA
查看答案和解析>>
科目: 来源:2016-2017学年河南省许昌市五校高二上学期第一次联考化学试卷(解析版) 题型:选择题
有A、B、C、D、E五种短周期元素,其中A、B、C、D同周期, C、E同主族; A+ 与E2-具有相同的电子层结构;离子半径:C2->D-;B的单质晶体熔点、硬度大,是一种重要的半导体材料。下列说法中,正确的是( )
A. 由于D、C、E元素的氢化物相对分子质量依次减小,所以其沸点依次降低
B. 元素D和E的某些单质不可以作为水处理中的消毒剂
C. 元素B的单质只能与氢氧化钠溶液反应而不能与任何酸反应
D. A、E两种元素能形成A2E和A2E2型化合物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com