
科目: 来源: 题型:
一定温度下,向如图所示带有可移动活塞的密闭容器中充入2 L SO2 和1 L O2 的混合![]() 气体,发生如
气体,发生如![]() 下反应2 SO2 (g) + O2 (g)
下反应2 SO2 (g) + O2 (g) ![]()
![]() 2 SO3 (g) 。
2 SO3 (g) 。
(1) 若活塞可自由移动,平衡后,活塞停止在“2.1”处该反应中SO2 的转化率为 。
(2) 若开始时,充入容器的起始物质分别是
①2 L SO2 和1 L O2 ;
②2 L SO3 (g) 和 1 L N2 ;
 ③1 L SO2 、1 L O2 和 1 L SO3 (g),
③1 L SO2 、1 L O2 和 1 L SO3 (g),
使活塞固定在“3”处,达到平衡后,容器中SO3 (g)占反应混合物的体积分数的大小关系是:
(用序号①②③和“<”、“=”、“>”表示)。
(3) 向(1)平衡后的容器中充入0.2 mol 的SO3,活塞移动后再次达到平衡时,测得此过程中从外界共吸收了1.96 kJ 的热量。写出SO2 发生氧化反应的热化学方程式: ![]() _______________ 。
_______________ 。
查看答案和解析>>
科目: 来源: 题型:
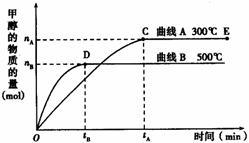 如右图所示,一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g) + 2H2(g)
如右图所示,一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO):CO(g) + 2H2(g) ![]() CH3OH(g)
CH3OH(g)
上述可逆反应正反应为___________反应(填“放热”或“吸热”)。
在500℃,从反应开始到平衡,氢气的平均反应速率v(H2) =___________________________(用nB、tB表示)。
对处于E点的体系,改变外界条件使平衡向正反应方向移动时,下列有关该体系的说法正确的是______________________(填字母)。
A.H2的转化率一定增大 B.v正一定增大,v逆一定减小
C.CH3OH的质量分数一定增加 D.v逆一定小于v正
查看答案和解析>>
科目: 来源: 题型:
CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
CO2(g)+3H2(g);该反应的正反应为吸热反应,请根据题目要求回答下列问题:
(1)在其它条件不变的情况下降低温度,则逆反应速率 (填“增大”或“减小”或“不变”,下同);在其它条件不变的情况下加压,则正反应速率 。
(2)一定条件下,向体积为2L的密闭容器中充入1molCH3OH(g)和3molH2O(g),20s后,测得混合气体的压强是反应前的1.2倍,则用甲醇表示该反应的速率为 。
(3)判断该可逆反应达到平衡状态的依据是(填序号) 。
A 、 v正(CH3OH)=v正(CO2)
B 、混合气体的密度不变
C、 混合气体的平均相对分子质量不变
D 、CH3OH、H2O、CO2、H2的浓度都不再发生变化
查看答案和解析>>
科目: 来源: 题型:
已知25℃、101kpa时,一些物质的燃烧热为:
| 化学式 | CO(g) | H2(g) | CH3OH(l) | CH4(g) |
| △H/(kJ/mol) | -283.0 | -285.8 | -726.5 | -890.3 |
请回答下列问题。
(1)写出该条件下CH3OH(l)完全燃烧的热化学方程式: 。
(2)根据盖斯定律完成下列反应的热化学方程式:CO(g)+ 2H2(g)= CH3OH(l);△H= 。
(3)现有H2和CH4的混合气体112 L(标准状况),使其完全燃烧生成CO2(g)和H2O(l),共放出热量3242.5 kJ,则原混合气体中H2和CH4的物质的量之比是:
A.1∶1 B.1∶3 C.1∶4 D.2∶3
查看答案和解析>>
科目: 来源: 题型:
氨气是氮循环中的重要物质,在人类的生产和生活中有着广泛的应用。
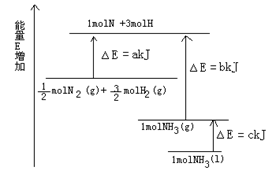 (1)右图是N2与H2反应过程中能量变化的示意图,则该反应生成液态氨的热化学方程式是______________________ 。
(1)右图是N2与H2反应过程中能量变化的示意图,则该反应生成液态氨的热化学方程式是______________________ 。
(2).若由N2和H2合成1molNH3时可放出46.2kJ/mol的热量。从手册上查出N≡N键的键能是948.9kJ/mol,H-H键的键能是436. 0kJ/mol,则N-H键的键能是________ kJ/mol。
查看答案和解析>>
科目: 来源: 题型:
实验室利用如右图装置进行中和热的测定。回答下列问题:
⑴该图中有两处实验用品未画出,它们是________________、____________________;
⑵在操作正确的前提下提高中和热测定的准确性的关键是:_____________________________________ _
⑶如果用0.5mol/L的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将________ (填“偏大”、“偏小”、“不变”)原因是______________________________________
查看答案和解析>>
科目: 来源: 题型:
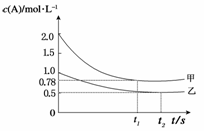 网向甲乙两个容积均为1L的恒容容器中,分别充入2mol A、4molB和1molA、2molB。相同条件下,发生下列反应:A(g)+2B(g)
网向甲乙两个容积均为1L的恒容容器中,分别充入2mol A、4molB和1molA、2molB。相同条件下,发生下列反应:A(g)+2B(g) ![]() xC(g) ΔH<0。测得两容器c(A)随时间t的变化如图所示,下列说法正确的是( )
xC(g) ΔH<0。测得两容器c(A)随时间t的变化如图所示,下列说法正确的是( )
A.x可能等于3
B.向平衡后的乙容器中充入氦气可使A的转
化率降低
C.将乙容器单独升温,c(A)可达到0.78 mol·L-1
D.若向甲容器中再充入2molA、4molB,平衡时甲容
器中c(A)等于1.56 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
 反应N2O4(g)
反应N2O4(g)![]() 2NO2(g);△H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2NO2(g);△H= +57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )![]()
A.A、C两点的反应速率:A>C![]()
B.A、C两点气体的颜色:A深,C浅![]()
C.由状态B到状态A,可以用加热的方法![]()
D.A、C两点气体的平均相对分子质量:A>C![]()
查看答案和解析>>
科目: 来源: 题型:
一定温度下,某密闭容器里发生如下反应:CO(g) + H2O(g)![]() CO2(g) + H2(g)(正反应为吸热反应),当反应达到平衡时,测量容器中各物质的物质的量均为n mol,欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可采用的是( )。
CO2(g) + H2(g)(正反应为吸热反应),当反应达到平衡时,测量容器中各物质的物质的量均为n mol,欲使H2的物质的量浓度增大1倍,在其他条件不变时,下列措施中可采用的是( )。![]()
①升高温度 ②增大压强 ③再通入n mol CO2和n mol H2 ![]() ④恒容再加入2n mol CO和2n mol H2O(g)
④恒容再加入2n mol CO和2n mol H2O(g)![]()
A.①② B.②④ C.③④ D.①②③![]()
查看答案和解析>>
科目: 来源: 题型:
已知常温下,N2(气)和H2(气)生成2mol NH3(气)放出92.4 kJ热量。现有甲、乙两个容积相同且恒容的密闭容器,在常温下:①向密闭容器甲中通入1 molN2和3 mol H2,达到平衡时放出热量Q1kJ。②向密闭容器乙中通入0.5 mol N2和1.5 mol H2,达到平衡时放出热量Q2kJ。则下列关系式正确的是( )![]()
A.Q1=2Q2=92.4 B.Ql>2Q2 C.Q1<2Q2 D.Q1=2Q2≠92.4![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com