
科目: 来源:山东省模拟题 题型:单选题
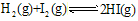 ,其它条件不变时,增大体系压强,平衡向正反应方向移动,体系颜色加深
,其它条件不变时,增大体系压强,平衡向正反应方向移动,体系颜色加深  可以大量共存
可以大量共存 查看答案和解析>>
科目: 来源:山东省模拟题 题型:填空题
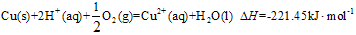

 。一定条件下,SO2的平衡转化率和温度的关系如图所示。该反应的ΔH _______0(填“>”或“<”)。反应进行到状态D时,v正________ v逆(填“>”、“<”或“=”)。?
。一定条件下,SO2的平衡转化率和温度的关系如图所示。该反应的ΔH _______0(填“>”或“<”)。反应进行到状态D时,v正________ v逆(填“>”、“<”或“=”)。? 
 2SO3(g)的平衡常数K=_________。
2SO3(g)的平衡常数K=_________。查看答案和解析>>
科目: 来源:陕西省模拟题 题型:填空题
 2Fe(s)+3CO2(g) △H=_______kJ/mol。
2Fe(s)+3CO2(g) △H=_______kJ/mol。  2/3 Fe(s)+CO2(g)在1000℃的平衡常数等于4.0。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡。
2/3 Fe(s)+CO2(g)在1000℃的平衡常数等于4.0。在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,反应经过10min后达到平衡。  。请根据图示回答下列问题:
。请根据图示回答下列问题: 

查看答案和解析>>
科目: 来源:江西省模拟题 题型:填空题
 H2(g)+CO2(g) △H=-41.2kJ/mol ,制备CO2与H2 的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用。
H2(g)+CO2(g) △H=-41.2kJ/mol ,制备CO2与H2 的混合气体,并进一步研究CO2与H2以不同的体积比混合时在合适条件下的反应产物应用。
 CO2(g)+ 2H2O(l) ΔH1=-890.3 kJ/mol
CO2(g)+ 2H2O(l) ΔH1=-890.3 kJ/mol  H2O(l) ΔH2=-285.8 kJ/mol
H2O(l) ΔH2=-285.8 kJ/mol 查看答案和解析>>
科目: 来源:江西省期中题 题型:填空题
 N2O4。反应中测得相关数据如下表所示:
N2O4。反应中测得相关数据如下表所示: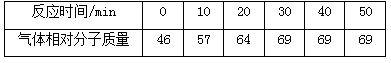
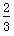 mol NO2,若要保持平衡不发生移动, 则应加入N2O4________mol。
mol NO2,若要保持平衡不发生移动, 则应加入N2O4________mol。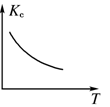
查看答案和解析>>
科目: 来源:新疆自治区月考题 题型:填空题

 2CH3OH
2CH3OH  CH3OH(g) ΔH=-90.8 kJ/mol
CH3OH(g) ΔH=-90.8 kJ/mol CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ/mol
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ/mol  CO2(g)+H2(g) ΔH=-41.3 kJ/mol
CO2(g)+H2(g) ΔH=-41.3 kJ/mol CH3OCH3(g)+CO2(g)的ΔH=________。一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是________(填字母代号)。
CH3OCH3(g)+CO2(g)的ΔH=________。一定条件下的密闭容器中,该总反应达到平衡,要提高CO的转化率,可以采取的措施是________(填字母代号)。查看答案和解析>>
科目: 来源:新疆自治区月考题 题型:单选题
 2B(g)和2A(g)
2B(g)和2A(g)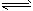 B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是
B(g)的转化率,在温度不变的情况下,均增加A的物质的量,下列判断正确的是查看答案和解析>>
科目: 来源:新疆自治区月考题 题型:单选题
 2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是 
查看答案和解析>>
科目: 来源:新疆自治区月考题 题型:单选题

查看答案和解析>>
科目: 来源:新疆自治区月考题 题型:单选题
 2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是
2N2(g)+3H2O(g) ΔH<0。在恒容的密闭容器中,下列有关说法正确的是查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com