
科目: 来源: 题型:
在硫酸的工业制法中,下列生产操作与生产操作的主要原因的说明都正确的是 ( )
A.SO2氧化为SO3时采用常压,因为高压会降低SO2转化率
B.从沸腾炉出来的炉气需要净化,因为炉气中SO2会与杂质反应
C.用98.3%的浓硫酸吸收,目的是防止形成酸雾,以便使SO3吸收完全
D.SO2氧化为SO3时需要使用催化剂,这样可以提高SO2的转化率
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是( )
A.任何化学反应伴随有能量变化
B.反应物总能量低于生成物的总能量时,该反应不能发生
C.反应物总能量高于生成物总能量的反应为放热反应
D.化石燃料在地球上的蕴藏量是有限的,而且又都是非再生能源
查看答案和解析>>
科目: 来源: 题型:阅读理解
铁是人体不可缺少的微量元素,摄入含铁的化合物可补充铁。“速力菲”是市场上一种常见的补铁药物,下表格是它的说明书。
| 【规格】 每片含琥珀酸亚铁0.1g 【适应症】 用于缺铁性贫血症,预防及治疗用。 【用量用法】 成人预防量0.1g/日,成人治疗量0.2g~0.4g/日, 小儿用量预防量30~60mg/日,治疗量0.1g~0.3g/日。 【藏】 避光、密封、在干燥处保存 |
(1)该药品中Fe2+ 会缓慢氧化,国家规定该药物中Fe2+ 的氧化率超过10%即不能再服用。
①为了检验某药店出售的“速力菲”是否氧化,实验室可选用最常用最灵敏的检验试剂为 ___________ ( 填试剂的名称 )
②实验室采用H2SO4酸化的KMnO4溶液,对“速力菲”中的Fe2+ 进行滴定(假设药品中,其它成分不与KMnO4反应)。请配平下列离子方程式
_____MnO4- + _____Fe2+ + ______H+ = _____Mn2+ + ______Fe3+ + ______H2O
③称量上述含铁元素质量分数为20.00% 的“速力菲”10.00 g,将其全部溶于稀硫酸中,配制成1000.00 mL溶液,取出20.00 mL,用0.01 mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00 mL。该药品可以服用吗?______________(填“可以”或“不可以”),请通过计算简述理由(写出主要计算过程)_______ 。
(2)已知琥珀酸亚铁相对分子质量为172,琥珀酸为有机酸。含23.6 g琥珀酸的溶液与4mol/L 100mL的氢氧化钠溶液恰好完全中和。质子核磁共振分析显示,琥珀酸分子中只含有两种位置不同的氢原子。写出琥珀酸溶液与氢氧化钠溶液完全中和的离子方程式(有机物须写结构简式) ,琥珀酸亚铁的化学式为 。
查看答案和解析>>
科目: 来源: 题型:
碱存在下,卤代烃与醇反应生成醚(R-O-R‘):
R-X+R‘OH![]() R-O-R‘+HX
R-O-R‘+HX
化合物A经下列四步反应可得到常用溶剂四氢呋喃,反应框图如下:
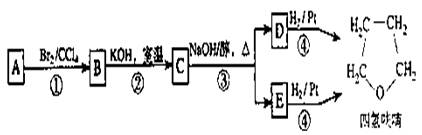
请回答下列问题:
(1)1 molA和1 molH2在一定条件下恰好反应,生成饱和一元醇Y,Y中碳元素的质量分数约为65%, 则Y的分子式为______ 的结构简式为____________。
(2)第①②步反应类型分别为 ①
②
(3)化合物B具有的化学性质(填写字母代号)是__________________________
a.可发生氧化反应
b.强酸或强碱条件下均可发生消去反应
c.可发生酯化反应
d.催化条件下可发生加聚反应
(4)写出D和E的结构简式:D_________________E_____ 。
(5)写出化合物C与![]() 水溶液共热的化学反应方程式:
水溶液共热的化学反应方程式:
(6)写出四氢呋喃链状醚类的所有同分异构体的结构简式:
查看答案和解析>>
科目: 来源: 题型:
如下图所示的各物质的相互转变中,反应①、②是重要的工业反应,A的相对分子质量为120。X被人体吸入会与血红蛋白结合而使人中毒,Y会造成温室效应,D会形成酸雨,E是常见的金属,F分子的结构与Y分子的结构相似,且F的相对分子质量为60。
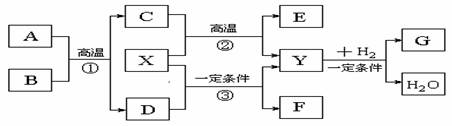
回答下列问题:
(1)反应①的化学方程式为: 。
(2)反应②的化学方程式为: 。
(3)写出F的结构式: 。
(4)Y与H2在一定条件下可生成多种物质,既可获得经济效益,也可减轻对环境的污染。
①若G是一种燃料,其相对分子质量与B的相对分子质量相等,则G的分子式为: 。
②若G是Y与H2按1∶3的比例反应而得,则G可能是 。(填编号)
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
查看答案和解析>>
科目: 来源: 题型:
现有A、B、C、D、E五种强电解质,它们在水中可电离产生下列离子(各种离子不重复)。
| 阳离子 | H+、Na+、A13+、Ag+、Ba2+ |
| 阴离子 | OH-、C1-、CO32-、NO3-、SO42- |
已知:①A、B两溶液呈碱性;C、D、E溶液呈酸性。
②A溶液与E溶液反应既有气体又有沉淀产生;A溶液与C溶液反应只有气体产生(沉淀包括微溶物,下同)。
③D溶液与另外四种溶液反应都能产生沉淀; C只能与D反应产生沉淀。
试回答下列问题:
(1)写出化学式:A___________ B___________ D_________
(2)E溶液呈酸性的原因是:(用离子方程式表示)_______________________________
(3)将C溶液逐滴加入等体积、等物质量的浓度的A溶液中,反应后溶液中各种离子浓度由大到小的顺序为: 。
(4)在100mL0.1mol?L-1 E溶液中,逐滴加入35mL 2mol?L-1NaOH溶液,最终得到沉淀物质的量为 mol
查看答案和解析>>
科目: 来源: 题型:
X、Y是周期表前二十号元素 ,已知X、Y之间原子序数相差3 ,X、Y能形成化合物M下列说法正确的是( )
A.若X、Y处于同一周期,则化合物M不可能是正四面体型分子晶体
B.若X的单质常温下是气体,则Y的单质常温下也是气体
C.若X、Y两元素周期数差1,则属于离子化合物的M只有四种
D.若M属于离子晶体,则其中可能含有非极性键
查看答案和解析>>
科目: 来源: 题型:
我国支持“人文奥运”的一个重要体现是坚决反对运动员服用兴奋剂。某种兴奋剂的结构简式如图所示,有关该物质的说法正确的是( )
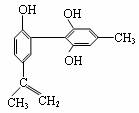
A.该分子中的所有碳原子一定在同一个平面上
B.滴入酸性KMnO4溶液,观察紫色褪去,能证明结构中存在碳碳双键
C.1mol该物质分别与浓溴水和H2反应是最多消耗Br2和H2的物质的量分别为4mol、7mol
D.遇FeCl3溶液呈紫色,因为该物质与苯酚属于同系物
查看答案和解析>>
科目: 来源: 题型:
现有碳酸钠、碳酸氢钠、氢氧化钠、氯化铁和苯酚五种物质的溶液,它们之间有如图所示转化关系,图中每条线两端的物质可以发生反应,下列判断不合理的是( )

A.X一定是碳酸钠溶液
B.Y一定是氯化铁溶液
C.Z可能为碳酸氢钠溶液
D.M、N必定各为苯酚、氢氧化钠溶液中的某一种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com