
科目: 来源: 题型:
化学在生产和日常生活中有着重要的应用。下列说法不正确的
A.明矾水解形成的Al(OH)3胶体能吸附水中悬浮物,可用于水的净
B. 在海轮外壳上镶入锌块,可减缓船体的腐蚀速
C. ![]() 的熔点很高,可用于制作耐高温材料
的熔点很高,可用于制作耐高温材料
D. 点解![]() 饱和溶液,可制得金属镁
饱和溶液,可制得金属镁
查看答案和解析>>
科目: 来源: 题型:
用NA表示阿伏加德罗常数的值。下列叙述正确的是
A. 25℃时,PH=13的1.0L Ba(OH)2溶液中含有的![]() 数目为0.2NA
数目为0.2NA
B. 标准状况下,2.24L Cl2与过量稀NaOH溶液反应,转移的电子总数为0.2NA
C. 室温下,21.0g乙烯和丁烯的混合气体中含有的碳原子数目为1.5NA
D. 标准状况下,22.4L 甲醇中含有的氧原子数为1.0NA
查看答案和解析>>
科目: 来源: 题型:
编号 | HX | YOH | 溶液的体积关系 |
(1) | 强酸 | 强碱 | V(HX)=V(YOH) |
(2) | 强酸 | 强碱 | V(HX)<V(YOH) |
(3) | 强酸 | 弱碱 | V(HX)=V(YOH) |
(4) | 弱酸 | 强碱 | V(HX)=V(YOH) |
A. (1)(3) B. (2)(3)
C. (1)(4) D. (2)(4)
查看答案和解析>>
科目: 来源: 题型:
下列所列各组物质中,物质之间通过一步反应就能实现如图所示转化的是
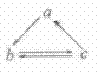
| a | b | c |
A | Al | AlCl3 | Al(OH)3 |
B | HNO3 | NO | NO2 |
C | Si | SiO2 | H2SiO3 |
D | CH2=CH2 | CH3CH2OH | CH3CHO |
查看答案和解析>>
科目: 来源: 题型:
《中华人民共和国食品安全法》于2009年月1日起实施。下列做法不利于平安全的是
A.用聚氯乙烯塑料袋包装食品w.w.w.k.s.5.u.c.o.m
B. 在食品盐中添加适量的碘酸钾
C.在食品加工中科学使用食品添加剂
D.研发高效低毒的农药,降低蔬菜的农药残留量
查看答案和解析>>
科目: 来源: 题型:
(14分)氢氧燃料电池是符合绿色化学理念的新型发电装置。下图为电池示意图,该电池电极表面镀一层细小的铂粉,铂吸附气体的能力强,性质稳定,请回答:
![]()
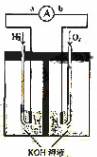
(1)氢氧燃料电池的能量转化主要形式是 ,在导线中电子流动方向为 (用a、b 表示)。
![]() (2)负极反应式为 。
(2)负极反应式为 。
![]() (3)电极表面镀铂粉的原因为 。
(3)电极表面镀铂粉的原因为 。
![]() (4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.k.s.5.u.c.o.m
(4)该电池工作时,H2和O2连续由外部供给,电池可连续不断提供电能。因此,大量安全储氢是关键技术之一。金属锂是一种重要的储氢材料,吸氢和放氢原理如下:w.w.w.k.s.5.u.c.o.m
![]() Ⅰ.2Li+H2
Ⅰ.2Li+H2![]()
![]() 2LIH
2LIH
![]() Ⅱ.LiH+H2O==LiOH+H2↑
Ⅱ.LiH+H2O==LiOH+H2↑
![]() ①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
①反应Ⅰ中的还原剂是 ,反应Ⅱ中的氧化剂是 。
②已知LiH固体密度为0.82g/cm3。用锂吸收224L(标准状况)H2,生成的LiH体积与被吸收的H2体积比为 。
③由②生成的LiH与H2O作用,放出的H2用作电池燃料,若能量转化率为80%,则导线中通过电子的物质的量为 mol。
查看答案和解析>>
科目: 来源: 题型:
(18分)海水是巨大的资源宝库,在海水淡化及综合利用方面,天津市位居全国前列。从海水中提取食盐和溴的过程如下:

(1)请列举海水淡化的两种方法: 、 。
(2)将NaCl溶液进行电解,在电解槽中可直接得到的产品有H2、 、 、或H2、 。
(3)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br,其目的为 。
(4)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 ,由此反应可知,除环境保护外,在工业生产中应解决的主要问题是 。
(5)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃。微溶于水,有毒性和强腐蚀性。他们参观生产过程后,了如下装置简图: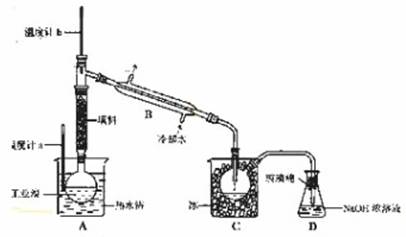
请你参与分析讨论:
①图中仪器B的名称: 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。
④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
查看答案和解析>>
科目: 来源: 题型:阅读理解
(18分)请仔细阅读以下转化关系:
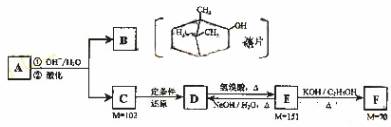
A.是从蛇床子果实中提取的一种中草药有效成分,是由碳、氢、氧元素组成的酯类化合物;
B.称作冰片,可用于医药和制香精,樟脑等;
C.的核磁共振氢谱显示其分子中含有4种氢原子;
D. 中只含一个氧原子,与 Na反应放出H2 ;
F.为烃。
请回答:(1) B的分子式为_______________________。
(2)B不能发生的反应是(填序号)______________。
a.氧化反应 b.聚合反应 c.消去反应 d取代反应 e.与Br2加成反应.
(3)![]() 写出D→E、E→F的反应类型:
写出D→E、E→F的反应类型:
D→E__________________、E→F_______________________。
(4)![]() F的分子式为____________________。
F的分子式为____________________。
化合物H是F的同系物,相对分子质量为56,写出H所有可能的结构;
_______________________________________________________________________。
(5)![]() 写出A、C的结构简式并用系统命名法给F命名:
写出A、C的结构简式并用系统命名法给F命名:
A:___________________、C: 、F的名称:__________________。
(6)写出E→D的化学力程式_____________________________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
(14分)下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
族
| IA |
| 0 | |||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
|
2 |
|
|
| ② | ③ | ④ |
|
|
3 | ⑤ |
| ⑥ | ⑦ |
|
| ⑧ |
|
(1)④、⑤、⑥的原子半径由大到小的顺序为_________________________。
(2)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是_________________________。
(3)①、④、⑤、⑧中的某些元素可形成既含离子键又含极性共价键的化合物,写出其中一种化合物的电子式:____________________。
(4)由表中两种元素的原子按1:1组成的常见液态化合物的稀液易被催化分解,可使用的催化剂为(填序号_________________。
a.MnO2 b.FeCl3 c.Na2SO3 d.KMnO4
(5)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
X溶液与Y溶液反应的离子方程式为_____________________,
N→⑥的单质的化学方程式为________________。
常温下,为使0.1 mol/L M 溶液中由M电离的阴、阳离子浓度相等,应向溶液中加入一定量的Y溶液至_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com