
科目: 来源: 题型:
向浓度相同的Al2(SO4)3、MgSO4、(NH4)2SO4溶液中,加入等体积等浓度的BaCl2溶液时,恰好使上述三种溶液中SO42-全部沉淀,则Al2(SO4)3、MgSO4、(NH4)2SO4三种盐溶液的体积之比为
A.1:2:3 B.3:2:1 C.1:3![]() :3 D.3:1:1
:3 D.3:1:1
查看答案和解析>>
科目: 来源: 题型:
已知a、e、I为三种由短周期元素构成的粒子,它们都有10个电子,其结构特点如下:
| 粒子代码 | a | e | I |
| 原子核数 | 单核 | 两核 | 四核 |
| 粒子的电荷数 | 一个单位正电荷 | 一个单位负电荷 | 0 |
物质A由a、e 构成, B、C、D、K都是单质,各有关物质之间的相互反应转化关系如下图所示,反应①—⑤ 都是用于工业生产的反应,⑥、⑦反应中个别产物在图中略去。
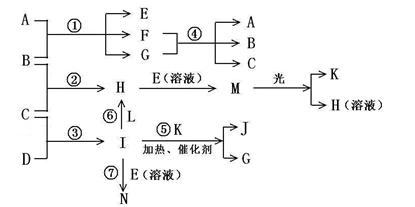
请填写下列空白:
(1)写出下列物质的化学式:B__________,J__________。
(2)写出下列反应的离子反应方程式:
H + E(溶液)→M____________________________________________________,
F + G →A + B + C________________________________________;
(3)E(溶液)能与I以1∶2的物质的量之比反应生成N、F和G,N中各原子均已达到惰性气体的稳定结构,写出N的结构式__________;
(4)L是由3种元素构成的分子,能与I以1∶2的物质的量之比反应生成尿素CO(NH2) 2 和物质H,写出L的电子式__________;
(5)反应③用于工业生产它应在_______________进行(填设备名称);反应④用于工业生产时为了防止B和C混合反应产生危险,所使用的一种特殊材料的名称为__________,在该工业生产中它具有的特殊的性质是________________________。
(6)常温下,实验室模拟工业反应④的过程如下图所示,标况下,当电极上产生112mL(已折算为标准状况下的体积)B气体时,烧杯中溶液的pH=__________。(假设气体完全逸出,溶液体积不变)
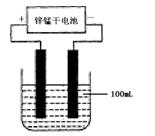
查看答案和解析>>
科目: 来源: 题型:
下列除去杂质的方法正确的是
A.除去N2中的少量O2:通过灼热的CuO粉末,收集气体
B.除去Fe2O3中的Al2O3:加入NaOH溶液,过滤
C.除去CO2中的少量HCl:通入饱和NaHCO3溶液,收集气体
D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤
查看答案和解析>>
科目: 来源: 题型:
下图中电极a、b分别为Ag电极和Pt电极,电极c、d都是石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体。回答:

(1)直流电源中,M为 极。
(2)写出c极上发生的电极反应式 。
(3)Pt电极上生成的物质是 ,其质量为 g。
(4)AgNO3溶液的浓度(填增大、减小或不变。) , H2SO4溶液的浓度 。(同上)
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为 g。
查看答案和解析>>
科目: 来源: 题型:
有A、、B、C、D四种元素,其中A元素和B元素的原子都有1个未成对电子,![]() 比
比![]() 少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1。请回答下列问题:
少一个电子层,B原子得一个电子后3p轨道全满;C原子的p轨道中有3个未成对电子,其气态氢化物在水中的溶解度在同族元素所形成的氢化物中最大;D的最高化合价和最低化合价的代数和为4,其最高价氧化物中含D的质量分数为40%,且其核内质子数等于中子数。R是由A、D两元素形成的离子化合物,其中A与D离子数之比为2:1。请回答下列问题:
(1)A单质、B单质、化合物R的熔点大小顺序为下列的 (填序号)。
①A 单质>B单质>R ②R>A单质>B单质
③B 单质>R>A单质 ④A单质>R>B单质
(2)在CB3分子中C元素原子的原子轨道发生的是________杂化,其固体时的晶体类型为 。
(3)写出D原子的核外电子排布式 _,C的氢化物比D的氢化物在水中溶解度大得多的可能原因 。
(4)右图是D和Fe形成的晶体FeD2最小单元“晶胞”,FeD2晶体中阴、阳离子数之比为 ,FeD2物质中具有的化学键类型为 。
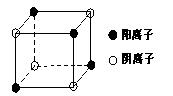
查看答案和解析>>
科目: 来源: 题型:
取10 mL 0.4 mol·L-1 FeCl3溶液置于烧杯中,向其中加入一定量的Fe、Cu混合物充分反应。下列叙述中一定不正确的是(设溶液体积不变,不考虑水解因素)
A.烧杯中有Cu无Fe,反应后溶液中c(Fe2+)≤0.6 mol·L-1
B.烧杯中有Fe无Cu,反应后溶液中c(Fe2+)=0.6 mol·L-1
C.烧杯中Fe、Cu均无,反应后溶液中c(Cl-)=1.2 mol·L-1
D.烧杯中Fe、Cu均有,反应后溶液中c(Fe2+)=0.6 mol·L-1
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z在周期表中的位置关系如图所示,已知X最外层电子数为2,则下列叙述中正确的是

A.Z一定是活泼的金属元素
B.Y的最高价氧化物的水化物是一种强酸
C.1molX的单质跟足量水反应时,发生转移的电子为2mol
D.Y的氢化物稳定性大于Z的氢化物稳定性
查看答案和解析>>
科目: 来源: 题型:
2.8g某单质A能从盐酸中置换出0.1g H2,同时生成ACl2;另一元素B,它的最高价氧化物的化学式为BO3 ,在B的氢化物中,B的质量分数为94.1%,且B中的质子数与中子数相等。
(1)计算A、B两种元素的相对原子质量。
(2)B是什么元素?指出它在元素周期表中的位置。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com