
科目: 来源: 题型:
【题目】下图表示某些物质间转化关系。其中A、D是由相同元素组成的固体,且A为紫黑色,C为黑色粉末,B、E为常见气体;X与F是由相同元素组成的无色液体,且X具有消毒杀菌作用;Y是一种红色金属。请回答下列问题:

(1)A的化学式是_______;绿色固体是________ ;
(2)C物质在反应③中的作用__________;
(3)写出反应②、③的化学方程式:② ________________;③______________;
(4)若将合成气中两气体按分子数之比为1:1进行化合(原子利用率为100%),可合成多种有机化工产品,写出其中一种可能产品的化学式_________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】以下是初中化学的一些基本实验:
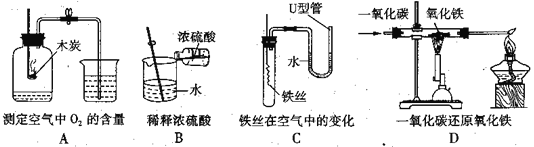
(1)上述实验中不能达到实验目的是__________________(填字母)。
(2)A中可燃物应取过量的原因是__________;B中玻璃棒的作用是_________;一段时间后,C中的实验现象为___________;D中硬质玻璃管内发生反应的化学方程式为___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】甲、乙两小组同学分别用下图所示装置(夹持仪器已略去)做兴趣实验。
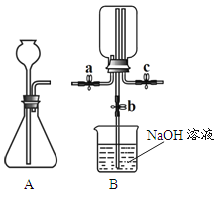
(1)甲组实验:
① 在A装置的锥形瓶中加入大理石,向长颈漏斗中注入稀盐酸,A中反应的化学方程式为_____。
② 连接A、B装置,打开a、c,关闭b,向B中集气瓶内充入气体,检验集气瓶中气体已收集满的方法是_____。
③ 关闭a、c,打开b,用冷毛巾捂住B中集气瓶,一段时间后,观察到B装置中的现象是_____, B中反应的化学方程式为_____。
(2)乙组实验:
【资料】氯化氢气体和氨气均极易溶于水,且两者反应生成白色固体氯化铵(NH4Cl)。
在c右端的导管口套一个气球,在A的锥形瓶中放入浓盐酸,向长颈漏斗中注入浓硫酸,有HCl气体产生,待A中的空气被排净后,连接A、B装置,打开a、c,关闭b,气球微微鼓起。产生HCl气体的原因是_____。
② 关闭a,将A中的药品替换为NaOH固体和浓氨水,待A中的空气被排净后,连接A、B装置,打开a,一段时间后关闭a,B中集气瓶内有白烟产生。冷却至室温后气球恢复原状。关闭c打开b,B中导管内的液面无任何变化。产生上述现象的原因是_____。
查看答案和解析>>
科目: 来源: 题型:
【题目】下图A、B、C为三种物质的溶解度曲线,据图回答:
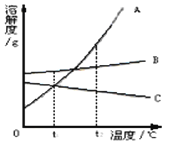
(1) t2℃时, A、B、C三种物质的溶解度由大到小顺序是 _____________
(2) 将t2℃时的等质量三种物质的饱和溶液分别降到0℃时,析出溶质最多的是________。
(3)当 A中含有少量B时为了得到纯净的A,可采用 ________的方法
(4)若将t2℃三种物质的饱和溶液分别降到t1℃时,则三种溶液中溶质的质量分数由大到小的顺序是___________。
查看答案和解析>>
科目: 来源: 题型:
【题目】做完“二氧化碳的制取和性质”实验后,废液缸中盛有大量的盐酸与氯化钙的混合溶液(不考虑其他杂质)。某同学处理废液时做了如下实验:取废液缸中上层清液于烧杯中,逐滴滴入Na2CO3溶液至过量。记录滴入Na2CO3溶液质量(x)与有关量的变化关系如图所示。下列判断正确的是
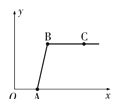
A.图中纵坐标(y)表示生成CO2的质量
B.反应进行到C点时,溶液中的溶质只有NaCl
C.C点溶液的pH>7
D.AB段发生反应的化学方程式是Na2CO3+2HCl=2NaCl+H2O+CO2↑
查看答案和解析>>
科目: 来源: 题型:
【题目】如图是浓盐酸试剂瓶上标签的部分内容,回答下列问题。

(1)该浓盐酸中溶质与溶剂质量比为_______;
(2)使用一段时间后,浓盐酸的溶质质量分数小于36%,可能原因是 _____________;
(3)盐酸等许多酸都能使紫色石蕊试液变红,是因为酸溶液中都含有______(用化学符号表示)。
查看答案和解析>>
科目: 来源: 题型:
【题目】向100克稀盐酸中加入锌粉(仅含不溶于酸的杂质),所加锌粉的质量与产生气体的质量的关系如下图所示。
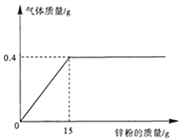
求:(1)充分反应后产生气体的质量为______________;
(2)原稀盐酸中溶质的质量分数为__________;
(3)锌粉中含锌的质量分数是____________?(写出计算过程,计算结果精确到0.1%)
查看答案和解析>>
科目: 来源: 题型:
【题目】某研究小组对自动充气气球(示意图如图1)进行下列探究.
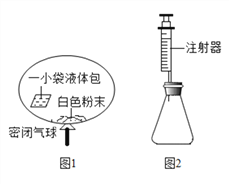
【查阅资料】该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气.
(1)为了检验气体是二氧化碳,可选用____(填试剂名称),反应方程式为_______________。
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液的pH=3,则该溶液呈_____性。
探究二:白色粉末成分的探究
【猜想与假设】
甲同学认为是碳酸钙; 乙同学认为是碳酸钠; 丙同学认为是碳酸氢钠。
【设计并进行实验】
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明________同学的猜想不正确。
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图2),记录如表:
实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
名称 | 质量/g | ||
① | 碳酸氢钠 | 5 | V1 |
② | 碳酸钠 | 5 | V2 |
③ | 白色粉末 | x | V1 |
实验①的化学方程式为__________;表中x=_____;V1 ____V2(填“>”、“<”或“=”)。
【分析并得出结论】:
(5)白色粉末是_________。
查看答案和解析>>
科目: 来源: 题型:
【题目】镁是一种用途很广的金属,目前世界上60%的镁是从海水(主要含NaCl和MgCl2等)中提取的。主要步骤如下:
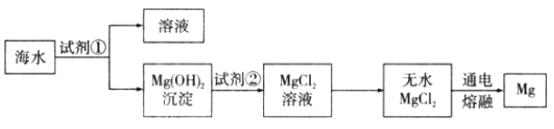
(1) 请写出Mg(OH)2沉淀与试剂②发生反应的化学方程式:____________,基本反应类型为 _________________;
(2)从海水中提取MgCl2时,经历了“MgCl2 ![]() Mg(OH)2
Mg(OH)2![]() MgCl2 ”的转化过程,这样做的目的是_____________ 。
MgCl2 ”的转化过程,这样做的目的是_____________ 。
查看答案和解析>>
科目: 来源: 题型:
【题目】某化学兴趣小组的同学做粗盐提纯实验,如图是同学们做粗盐提纯实验的示意图。
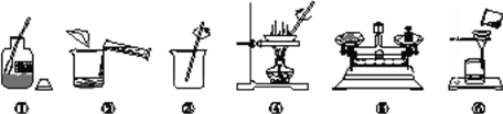
请回答下列问题。
(1)操作③中玻璃棒搅拌的作用是____________。
(2)操作⑥中的错误是___________。
(3)粗盐提纯实验中操作顺序为①⑤②_______(填操作序号),以及称量精盐并计算产率。
(4)操作④中,当观察到蒸发皿内____________时,停止加热,让余热蒸干剩余液体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com