
科目: 来源: 题型:
在120℃、101kPa下,amL由氢气、乙烯组成的混合气体在bmL氧气中充分燃烧后,恢复到原温度和压强。已知b > 3a,且燃烧后气体体积缩小了![]() mL,则乙烯的体积为 ( )
mL,则乙烯的体积为 ( )
A.![]() mL B.
mL B.![]() mL C.
mL C.![]() mL D.
mL D.![]() mL
mL
查看答案和解析>>
科目: 来源: 题型:
甲、乙两物体的溶解度曲线如图所示。 下列叙述中,正确的是 ( )
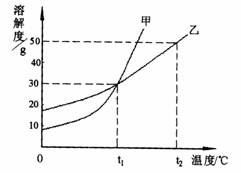
A.t1℃时,在100g水中放入60g甲,其溶质的质量分数为37.5%
B.t1℃时,甲和乙的饱和溶液的物质的量浓度一定相等
C.t2℃时,甲和乙的饱和溶液中溶质的质量数一定相等
D.t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
查看答案和解析>>
科目: 来源: 题型:
下列实验操作正确的是( )
A.向过量稀硫酸中加入除去油污的废铁屑,是制备硫酸亚铁的可行方案
B.向碳酸钠粉末中加入乙二酸溶液,生成大量气泡,说明乙二酸的酸性比碳酸强
C.向铝屑与硫酸反应后的溶液中加入氧氧化钠溶液,是制备氢氧化铝的最佳方案
D.向硫酸亚铁铵溶液中,依次加入氯水和硫氰化钾溶液,溶液变化,说明溶液中含有Fe2+
查看答案和解析>>
科目: 来源: 题型:
下列叙述不正确的是 ( )
A.电解饱和食盐水时,用铁作阳极,Cl-发生氧化反应
B.电解法精炼铜时,纯铜作阴极,Cu2+发生还原反应
C.电镀铜时,金属铜作阳极,电镀液可用硫酸铜溶液
D.铜锌原电池中,锌作负极,电子从锌极流向铜极
查看答案和解析>>
科目: 来源: 题型:
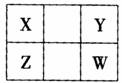 已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,Y、W不是O族元素。下列说法正确的是 ( )
已知X、Y、Z、W四种短周期元素在周期表中的相对位置如图所示,Y、W不是O族元素。下列说法正确的是 ( )
A.Z元素的原子半径可能比Y元素的小
B.Z元素的最高化合价可能比Y元素的高
C.W的气态氢化物的稳定性一定比Y的强
D.Z的最高价氧化物的水化物的酸性一定比W的强
查看答案和解析>>
科目: 来源: 题型:
下列说法正确的是 ( )
A.CO2、H2O都是非极性分子 B.乙酸、蔗糖都是弱电解质
C.C6H6O、C7H8O一定互为同系物 D.石英、食盐、金属钠、干冰的熔点依次降低
查看答案和解析>>
科目: 来源: 题型:
下列说法不正确的是( )
A.利用化学变化可以用活性炭除去冰箱中的异味
B.利用化学变化反应可以制得用作半导体材料的高纯硅
C.利用化学方法可以提高煤炭利用率,减少污染物的排放
D.利用高科技设备可以使人们清楚地观察到原子的图像和动态的化学变化
查看答案和解析>>
科目: 来源: 题型:
表中为一些短周期元素及相应氢化物沸点的数据:
元 素 性 质 | 元 素 编 号 | |||||
① | ② | ③ | ④ | ⑤ | ⑥ | |
氢化物的沸点(℃) | -60.7 | -33.4 | 100 | -87.7 | 19.54 | -84.9 |
最 高 化 合 价 | +6 | +5 | +5 | +7 | ||
最 低 化 合 价 | -2 | -3 | -2 | -3 | -1 | -1 |
A、B、Y均为上表中的元素。X是一种历史悠久,应用广泛的金属元素。
① X与Y可形成化合物XY、XY2, 二者可用接触法制强酸甲;
② A与B可形成化合物AB、AB2,二者均可用于制备强酸乙。
请回答:
(1)元素 ③ 氢化物的分子式是 __________。
(2)下列有关强酸甲、乙说法正确的是 ________。
a. 二者的浓溶液在常温时均可用铁制或铝制的容器贮运
b. 二者的浓溶液在敞口容器中放置,质量都会变化
c. 工业生产强酸甲、乙时,都要用水吸收相应的氧化物
d. 二者的稀溶液均是强氧化剂
(3)工业生产强酸甲时可用浓氨水处理尾气,并获得某种铵盐。
化学方程式为__________________________________。
(4)写出工业生产强酸乙时获得AB的化学方程式: 。
(5)工业生产强酸乙时可用纯碱溶液处理尾气,该反应如下:
AB + AB2 + Na2CO3 = 2 ![]() + CO2
+ CO2
① 在方框内填某盐的化学式
② 每产生44.8 L(标准状况)CO2,被吸收尾气的质量是 ______g。
(6) 表中属于第三周期的元素是_______________(用表中元素编号填写)。
查看答案和解析>>
科目: 来源: 题型:
短周期元素X、Y、Z、W原子序数依次增大,常温时化合物XW是气体,遇氨气产生大量白烟。化合物Z2Y2是淡黄色固体。
⑴ 写出离子化合物ZW的化学式 。
⑵ 写出Z2Y2与H2O反应的化学方程式 。
⑶ 如图装置所示,进行下列操作:
 第一步. 将开关K1接通后,水槽中 附近先变红
第一步. 将开关K1接通后,水槽中 附近先变红
(填阴极或阳极)。碳棒上的电极反应式为
。
第二步. 将开关K1断开,向水槽中滴入XW的溶液至红色恰
好褪去,再接通开关K2,发现电流表指针偏转。
写出碳棒上的电极反应式
。
第三步: 一段时间后,将开关K2断开,向水槽中滴入酸性K3[Fe(CN)6]溶液,可以看到有蓝色沉淀Fe3[Fe(CN)6]2生成,标出化学式 Fe3[Fe(CN)6]2 中铁元素的化合价(在横线处化学式上标出)。
⑷ Z2Y2可与氯化亚铁溶液反应产生红褐色沉淀和能使带火星木条复燃的气体,若沉淀和气体的物质的量之比为2:1,反应的化学方程式是
![]() 。
。
查看答案和解析>>
科目: 来源: 题型:
中学实验室可用同一种装置制备不同的气体,若只用如图装置制备气体

(1)请在下表空格中填上所需药品
| 所制气体 | 药品 | |
| 分液漏斗内 | 烧瓶中 | |
| O2 | MnO2 | |
| H2 | 稀H2SO4 | |
| NH3 | CaO | |
| NO | 稀HNO3 | Cu |
| CO2 | 稀H2SO4 | 石灰石 |
| C2H4 | 浓H2SO4 | C2H5OH |
| C2H2 | CaC2 | |
(2)写出表中药品制备O2的化学方程式
。
(3)写出表中药品制备C2H2的化学方程式
。
(4)请画出干燥NH3的装置图,并注明干燥剂和气体流向
。
(5)表中给全药品的项目中,不能用于制备相应气体的有(可不填满)
①气体 ,理由 。
②气体 ,理由 。
③气体 ,理由 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com