
科目: 来源:2012-2013学年湖北省黄冈市高三4月调研考试理综化学试卷(解析版) 题型:填空题
生产甲醇的原料CO、H2可由下列反应制取:CH4(g)+H2O(g)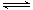 CO(g)+3H2(g),试回答下列问题。
CO(g)+3H2(g),试回答下列问题。
(1)已知:① CH4(g)+3/2 O2(g)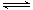 CO(g)+2H2O(g)△Hl;
CO(g)+2H2O(g)△Hl;
② H2(g)+1/2 O2(g)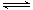 H2O(g) △H2,
H2O(g) △H2,
则CH4(g)+ H2O(g)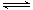 CO(g)+3H2(g)的△H=____ (用含△H1,△H2的式子表示)
CO(g)+3H2(g)的△H=____ (用含△H1,△H2的式子表示)
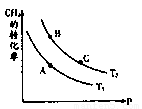
(2)一定条件下反应CH4(g)+H2O(g) CO(g)+3H2(g)中CH4的平衡转化率与温度、压强的关系如图,且T2>T1,
则上述反应的△H____ 0(填“<”、“>”、“=”,下同),A、B处对应平衡常数(KA、KB)的大小关系为KA____
KB
CO(g)+3H2(g)中CH4的平衡转化率与温度、压强的关系如图,且T2>T1,
则上述反应的△H____ 0(填“<”、“>”、“=”,下同),A、B处对应平衡常数(KA、KB)的大小关系为KA____
KB
(3)维持温度T2,将0.04 mol CH4和0.04mol H2O(g)通入容积为1L的定容密闭容器中发生反应,平衡时达到B点,测得CH4的转化率为50%,该反应在此温度下的平衡常数KB=____ ,下列现象能说明该反应已经达到平衡状态的是_ ___
a.容器内CH4、H2O、CO、H2的物质的量之比为1:1:1:3
b.容器的密度恒定
c.容器的压强恒定
d.3υ正(CO)=υ逆((H2)
(4)在上述B点平衡基础上,向容器中再通入amol CH4和a mol H2O气体,使之在C点重新达平衡,此时测得CO有0.03mol,则a=____ 。
查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三4月调研考试理综化学试卷(解析版) 题型:实验题
电石(主要成分为CaC2,杂质为CaO和CaS)是工业制乙炔的常见原料,某研究性学习小组拟用以下两种方案测定CaC2的质量分数,试完成下列各题。
方法一:称取1.40 g样品于圆底烧瓶中,用分液漏斗加入适量的水,使样品反应完全,将产生的无色
气体经B洗气后,通过量气装置测得乙炔气体体积为标准状况下448 mL(不考虑乙炔在水中的溶解,
下同)。
(1)电石水解生成乙炔气体的化学方程式为:
(2)用两个装入适当试剂的广口瓶、两个双孔橡胶塞及导管若干,完成上述实验的装置,请在图中将其补充完整,并注明广口瓶中装入试剂的名称。

(3)对获得准确的气体体积无益的操作有 (填序号)
①检查装置的气密性;
②恢复到室温后再上下调整量筒位置,使C、D两液面相平;
③在A装置胶塞上再连接一个导管,通入N2将A中C2H2全部进入到B、C中;
④读数时视线与量筒内凹液面最低点相平
(4)由以上数据可计算出样品中CaC2的质量分数为____ 。
方法二:称取l.40g样品于下图所示石英管中(夹持及加热装置省略),从a处不断缓缓通入空气,高
温灼烧石英管中的样品至反应完全,测得丙溶液的质量比反应前增重了1.80g,反应方程式为:2CaC2+
5O2=2CaO+ 4CO2。

(5)反应完成后,石英管内样品易与管壁产生腐蚀,试用化学方程式解释其原因
(6)甲锥形瓶中酸性高锰酸钾溶液的作用为
(7)由此方法测得的样品中CaC2的质量分数比方法一中的____ (填“大”、“小”或“相
等”),从实验装置的角度看,原因为 。
查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三4月调研考试理综化学试卷(解析版) 题型:填空题
下图是一种正在投入生产的大型蓄电系统。左右两侧为电解质储罐,中央为电池,利用2Na2S2+NaBr3 Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。
Na2S4+3NaBr反应原理进行工作,电解质通过泵不断在储罐和电池间循环;电池中的左右两侧为电极,中间为离子选择性膜,在电池放电和充电时该膜可允许钠离子通过。
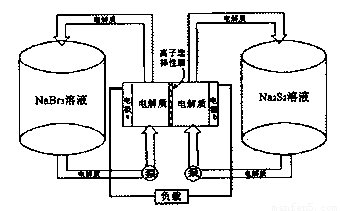
(1)当蓄电池工作放电时,电池中Na+的移动方向是:____ (填“电极a→b”或“电极b→a”),电极a的电极名称为 ,发生的电极反应为 。
(2)当蓄电池处于充电状态时,电极a应接外电源 极(填“正”或“负”),电极b的电极名称为 ,发生的电极反应为 。
(3)若左侧储罐的中溶液体积为VL(导管、泵及电池内部溶液忽略不计),一段时间观察,溶液中Na+的平均浓度由c1mol·L-1降至c2mol·L-1,则此装置该段时间正处于 (填“放电”或“充电”)状态,此过程中电极b上转移电子的物质的量共有__ mol。
查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三4月调研考试理综化学试卷(解析版) 题型:填空题
已知A、B、C、D均是元素周期表中前36号中的元素,其原于序数依次递增,其他相关结构或性质信息如下表。
元素 结构或性质信息
A 原子核外有一个未成对电子,其氢化物与水分子间能形成氢键
B 原子核外M层电子数是N层电子数的4倍
C 是使用最为广泛的合金的主要成分
D 原子各内层电子均已饱和,最外层电子数为1
请根据信息回答有关问题:
(1)C元素在周期表中的位置为____ ,D元素原子的外围电子排布式为
(2)用氢键表示式写出A的氢化物水溶液中存在的所有氢键____ 。
(3)A与氧可形成原子个数比为2:1的三原子分子,其中氧的化合价为____ ,氧原子杂化类型与下列分子的中心原子杂化类型相同的是____
a:CO2 b:SO2 c:NH3 d;CH4
(4)A、B可形成离子化合物,其晶胞结构如下图甲所示,则晶胞中B离子的个数为____ ,与B离子最近且等距的A离子的个数为 。
(5)1183 K以下C晶体的晶胞如图乙中图1,而1183 K以上则转变为图2,在两种晶胞中最邻近的C原子间距离相同,则图1、图2所示两种晶中原子的空间利用率之比为___ _(可用根号表示)。

查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三4月调研考试理综化学试卷(解析版) 题型:填空题
已知:当羟基与双键碳原子相连接时,易发生如下转化: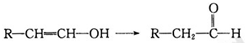 化学式为C11H10O4的有机物A有如下的转化关系
化学式为C11H10O4的有机物A有如下的转化关系
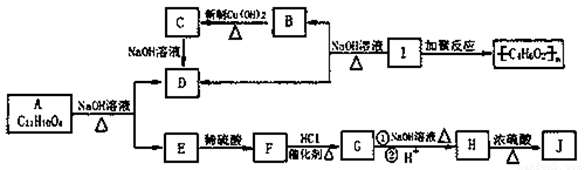
其中F为苯的二元对位取代物,分子中含有羟基、羧基及碳碳双键,存在顺反异构现象,J分子中有三十六元环状结构,其中一个六元环含有两个酯基。试回答:
(1)写出有机物结构简式:I:____ ,J:
(2)指出F→G的反应类型:
(3)写出A→E+D 的化学反应方程式:
(4)写出G与NaOH溶液共热的化学反应方程式:
(5)F的同分异构体F1也为苯的二元对位取代物,且与F具有相同的官能团,但其不存在顺反异构现象,则F1的结构简式为 。
查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
下列说法正确的是
A.SO2 可用于杀菌消毒
B.棉,麻,羊毛及合成纤维完全燃烧都只生成CO2和H2O
C.粒子直径在10-9-10-7 cm的分散系为胶体
D.植物油的主要成分是高级脂肪酸
查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列叙述正确的是
A.等物质的量的N2和CO所含分子数均为NA
B.标准状况下,11.2 L氟化氢所含的分子数为0. 5NA
C. 常温下,5.6g铁钉与足量浓硝酸反应,转移的电子数为0.5NA
D.常温常压下,14.9g KCl与NaClO的混合物中含氯元素的质量为7.1g
查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
氢镍电池是可充电电池,总反应式是H2+2NiO(OH)  2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:
2Ni(OH)2。根据此反应式,下列 有关说法中正确的是:
A.该电池所用的电解质溶液为酸性溶液
B电池充电时,氢元素被还原
C.电池放电时,镍元素被氧化
D.该电池的负极反应为H2-2e-=2H+
查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
醋酸溶液中存在电离平衡CH3COOH H++CH3COO-,下列叙述不正确的是
H++CH3COO-,下列叙述不正确的是
A.醋酸溶液中离子浓度的关系满足:c(H+)=c(CH3COO-)+c(OH-)
B.物质的量浓度相等CH3COOH和CH3COONa混合溶液:
c(CH3COO-)-c(CH3COOH)=2 c(H+)-2 c(OH-)
C.CH3COOH溶液加水稀释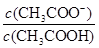 不变
不变
D.CH3COOH溶液加水稀释,溶液中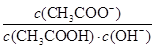 不变
不变
查看答案和解析>>
科目: 来源:2012-2013学年湖北省黄冈市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
已知:R-OH+R-OH R-O-R(醚)+H2O,分子式为C2H6O和C3H8O醇的混合物在一定条件下脱水形成的醚最多有
R-O-R(醚)+H2O,分子式为C2H6O和C3H8O醇的混合物在一定条件下脱水形成的醚最多有
A.4种 B. 5种 C.6种 D. 7种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com