
科目: 来源: 题型:
A.滴定管使用前要先用待装液润洗2—3次,而容量瓶不能先用待装液润洗
B.在电泳实验中,Fe(OH)3胶体粒子在电场作用下向阴极移动
C.过滤、渗析作为分离除杂的方法,分离原理是不同的
D.为了防止钢瓶被腐蚀,在储运液氯前钢瓶必须彻底干燥
查看答案和解析>>
科目: 来源: 题型:
A.X是石墨,Y是铜棒 B.X、Y均是铜棒
C.X极发生还原反应 D.Y是阳极
查看答案和解析>>
科目: 来源: 题型:
A
B.标准状况下,
C.1 mol Cl2与足量NaOH溶液反应转移的电子数为NA
D.
查看答案和解析>>
科目: 来源: 题型:
问:(1)当x=0.8时,溶液中产生的沉淀是什么?其物质的量为多少?
(2)当沉淀只有Fe(OH)3时,计算x的取值范围。
(3)请在图中画出沉淀总量n/mol随x(0—1)变化的曲线。
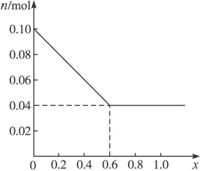
查看答案和解析>>
科目: 来源: 题型:
①首先将该空气样品通过盛有I2O5固体的加热管,反应生成CO2和I2(不考虑其他气体的反应);
②用30.0 mL 5.00×10-5 mol·L-1过量的硫代硫酸钠溶液完全吸收反应所产生的碘,发生的反应为:I2+2![]() ====2I-+
====2I-+![]() ;
;
③将②反应后溶液取出![]() ,放入锥形瓶中,加入几滴指示剂,用1.00×10-5 mol·L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:
,放入锥形瓶中,加入几滴指示剂,用1.00×10-5 mol·L-1的标准碘溶液进行滴定,滴定至终点,实验记录如下:
滴定次数 | 1.00×10-5 mol·L-1标准碘溶液体积/mL | |
滴定前刻度 | 滴定后刻度 | |
1 | 0.00 | 10.01 |
2 | 1.21 | 11.20 |
(1)写出①中反应的化学方程式;
(2)计算该空气样品中CO的浓度,并说明符合几级标准。
查看答案和解析>>
科目: 来源: 题型:
实验序号 | 固体混合物(A) | 加入蒸馏水 | 加入试剂(B) | 过滤、洗涤、干燥,得固体(C) | 蒸发滤液得到晶体(D) | 需称量的物质 |
Ⅰ | BaCl2、NaCl | 溶解 | 过量CO2 | — | D | A、D |
Ⅱ | CaCl2、NaCl | 溶解 | 过量饱和Na2CO3溶液 | CaCO3 | NaCl | A、C |
Ⅲ | Na2SO4、MgSO4 | 溶解 |
|
|
|
|
试回答下列问题:
(1)实验Ⅰ中D的成分是____________,称量后____________(填“能”或“不能”)通过计算得到A中各组分的质量比。
(2)实验Ⅱ填写的内容中明显错误的是____________,其原因是_____________________。
(3)对实验Ⅲ进行设计,并将相应内容填入Ⅲ中对应的空格内,最终能得出A中各组分的质量比为:(用含字母的表达式表示)_____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
方案1:向废液中加入过量的铁粉,充分反应后,过滤。在所得滤渣中加入足量的盐酸,充分反应后,再过滤即得到铜。方案1中涉及的四种阳离子的氧化性由强到弱的顺序为:______________________;过滤操作时,需要用到的玻璃仪器是:____________________。
方案2:在废液中加入适量盐酸调节溶液的pH=1,用铜和石墨作电极进行电解。当观察到阴极上有少量气泡产生时,即停止电解,这时要回收的Cu已全部析出。方案2中铜作___________极,所发生的电极反应为(若有多个电极反应,请按照反应发生的先后顺序全部写出):_____________________;另一电极所发生的电极反应为:____________________。
方案2在电极上直接回收到铜,操作上比方案1简便,但方案2也有不足之处,主要表现为:____________________________________________。
查看答案和解析>>
科目: 来源: 题型:
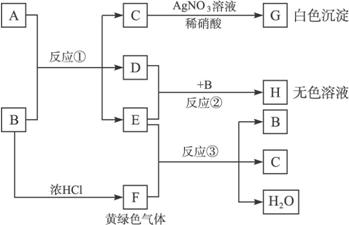
请回答:
(1)写出A、B中溶质的化学式:A___________,B___________。
(2)依次写出反应①和②的离子方程式(H中含有某+5价元素含氧酸根离子)___________、_______________。
(3)写出反应③的化学方程式__________________________________________________。
查看答案和解析>>
科目: 来源: 题型:
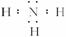
(1)③号元素位于周期表第___________周期___________族,其单质的一种同素异形体能导电,该同素异形体的名称叫___________。
(2)④号元素形成的气态氢化物的电子式为___________,属于___________分子(填“极性”或“非极性”)。
(3)⑥⑦两种元素形成的最高价氧化物对应的水化物之间相互反应的离子方程式为_______
_____________________________________________________________________。
(4)⑨号元素的原子结构示意图为___________,⑨与⑤两种元素形成的一种化合物是污染大气的主要有害物质之一,它对环境的危害主要是__________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com