
科目: 来源: 题型:阅读理解
(12分)选择性催化还原(SCR)是在有催化剂的条件下将NOx 转变为N2和H2O,这是目前国外硝酸厂进行尾气治理所普遍采用的一种方法。
.某校甲、乙两个化学兴趣小组拟验证NO能被氨气还原并测算其转化率。
(一)甲组拟制取活性亚铬酸铜催化剂
亚铬酸铜(Adkin催化剂)是极好的NO催化还原的催化剂,是铜和铬的复合氧化物,成分不固定,如:CuO?Cr2O3等,统称为亚铬酸铜。该组同学取一定量硝酸铜溶液(并加少量硝酸钡作稳定剂)、重铬酸铵溶液与氨水作用得土黄色沉淀, 将沉淀物[经测定为:碱式铬酸铜铵(CuNH4(OH)CrO4 )]过滤、洗涤,80℃烘干12h, 最后焙烧。
(1)过滤用到的玻璃仪器有: (选填序号,下同);焙烧用到的仪器有: 。
A.蒸发皿 B.石棉网 C.泥三角 D.烧杯 E.坩埚钳 F.酒精灯
G.玻璃棒 H.漏斗 I.坩埚(部分仪器已略去)
(2)CuNH4(OH)CrO4在295℃分解生成复合的氧化物(催化剂)、氮气及水,该反应的化学方程式: 。
(二)乙组拟用甲组制得催化剂按下列流程进行实验。
![]()

试回答下列问题:
(3)若制取氨气在A装置,则发生反应的化学方程式为: ;若用B装置制取氨气,则分液漏斗和锥形瓶中盛放的药品分别是: 。
![]()

(4)用图C装置制取NO时,用可抽动的铜丝其优点是: ;
(5)装置⑦的作用可能是: 。
(6)若进入装置⑤的NO共2688 mL(已折算为标准状况,下同),氨气过量,最后收集到标准状况下2016 mL N2,则NO的转化率为: 。
查看答案和解析>>
科目: 来源: 题型:
(8分)反应①②为重要的工业反应:⑤为火箭燃烧室中主要反应,E为黄绿色气体,P为红棕色气体I常温下为无色液体,为酸式盐,J由三种元素组成,相对分子质量为100,O相对分子质量为32。部分反应水已略去。
w.w.w.k.s.5.u.c.o.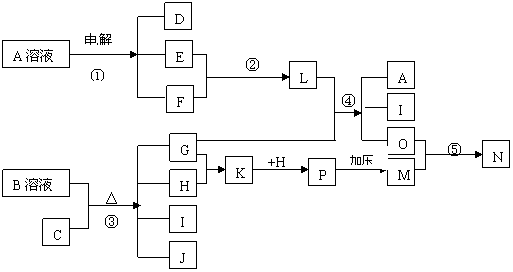
(1)写出物质O的结构式 物质C的电子式
(2)写出反应①的离子方程式
(3)写出反应③的化学方程式
(4)写出反应④的化学方程式
查看答案和解析>>
科目: 来源: 题型:
(07年广东卷)下列各溶液中,微粒的物质的量浓度关系正确的是()
A 1.0mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3)
B 1.0mol/LNH4Cl溶液:c(NH4+)=c(Cl-)
C 向醋酸钠溶液中加入适量醋酸,得到的酸性混合溶液:c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+)=c(NO3-)
查看答案和解析>>
科目: 来源: 题型:
(12分)利用甲烷与氯气发生取代反应制取副产品盐酸的设想在工业上已成为现实。某化学兴趣小组通过在实验室中模拟上述过程,其设计的模拟装置如下: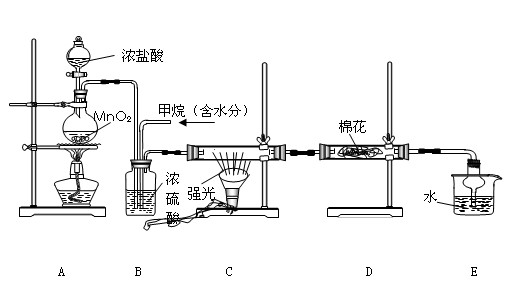
(1)写出A装置中发生反应的离子方程式
(2)B装置有三种功能:①控制气流速度;②均匀混合气体;③
(3)设V(Cl2)/V(CH4)=x,若理论上欲获得最多的氯化氢,则x值应≥
(4)一段时间后发现D装置中的棉花由白色变为蓝色,则棉花上可能预先滴![]() 有 溶液。
有 溶液。
(5)在C装置中,经过一段时间的强光照射,发现硬质玻璃管内壁有黑色小颗粒产生,写出反应的化学方程式 。
(6) E装置中除盐酸外,还含有有机物,从E中分离出盐酸的最佳方法为 (填字母)。
![]() A.水洗分液法 B.蒸馏法 C.萃取分液法 D.结晶法
A.水洗分液法 B.蒸馏法 C.萃取分液法 D.结晶法
(7) 该装置还有缺陷,原因是没有进行尾气处理,其尾气主要成分为 (填字母)。
![]() A、CH4 B、CH3Cl C、CH2Cl2 D、CHCl3
A、CH4 B、CH3Cl C、CH2Cl2 D、CHCl3
查看答案和解析>>
科目: 来源: 题型:
(08年上海卷)生态农业涉及农家肥料的综合利用,某种肥料经发酵得到一种含有甲烷、二氧化碳、氮气的混合气体。2.016L(标准状况)该气体通过盛有红色CuO粉末的硬质玻璃管,发生的反应为:CH4+4CuO![]() CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
CO2+2H2O+4Cu。当甲烷完全反应后,硬质玻璃管的质量减轻4.8g。将反应后产生的气体通过过量的澄清石灰水,充分吸收,生成沉淀8.5g。
(1)原混合气体中甲烷的物质的量是____________。
(2)原混合气体中氮气的体积分数为多少?(写出计算过程)
查看答案和解析>>
科目: 来源: 题型:
可逆反应![]() △H=-QKJ/mol(Q>0)。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2。下列叙述不正确的是
△H=-QKJ/mol(Q>0)。有甲、乙两个容积相同且不变的密闭容器,向甲容器中加入1molN2和3molH2,在一定条件下达到平衡时放出热量为Q1KJ;在相同条件下,向乙容器中加入2molNH3达到平衡后吸收热量为Q2KJ,已知Q1=4Q2。下列叙述不正确的是
A.达A到平衡时,甲容器中反应物的转化率与乙容器相等
B.达到平衡时,甲中NH3的体积分数与乙相等
C.达到平衡后,再向乙中加入0.2moLN2、0.6mol3H2、1.6molNH3,平衡向生成NH3的方向移动
D.乙中的热化学反应方程式为![]()
![]() ;△H=+QKJ/mol(Q>Q2>0)
;△H=+QKJ/mol(Q>Q2>0)
查看答案和解析>>
科目: 来源: 题型:
(07年广东卷)将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如下图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是()
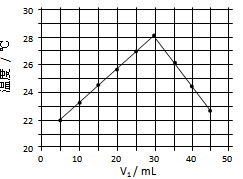
A . 做该实验时环境温度为22℃
B. 该实验表明化学能可能转化为热能
C . NaOH溶液的浓度约为1.0mol/L
D . 该实验表明有水生成的反应都是放热反应
查看答案和解析>>
科目: 来源: 题型:
取A、B两份物质的量浓度相等的NaOH溶液,体积均为50mL,分别向其中通入一定量的CO2后,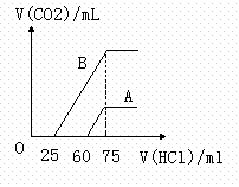 再分别稀释到100 mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的CO2体积(标准状况)与所加盐酸的体积关系如图所示,下列说法正确的是
再分别稀释到100 mL,在稀释后的溶液中分别滴加0.1mol/L的盐酸,产生的CO2体积(标准状况)与所加盐酸的体积关系如图所示,下列说法正确的是
A.原NaOH溶液的物质的量浓度0.15mol/L
![]()
B.A曲线表明原溶液通入CO2后,所得溶质为NaOH和Na2CO3,此时用酚酞作指示剂,溶液颜色变化时消耗盐酸的体积为75mL
C.B曲线表明原溶液通入CO2后,所得溶质为Na2CO3和NaHCO3且物质的量之比为1:1
![]() D.B曲线表明原溶液通入CO2后,所得溶质与盐酸反应产生的最大体积为33.6 mL(标准状况)
D.B曲线表明原溶液通入CO2后,所得溶质与盐酸反应产生的最大体积为33.6 mL(标准状况)
查看答案和解析>>
科目: 来源: 题型:
下列各溶液中,微粒的物质的量浓度关系正确的是:
![]() A.10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:
A.10mL 0.5mol/L CH3COONa溶液与6mL 1mol/L盐酸混合:
c(Cl-)>c(Na+) >c(CH3COO-)>c(H+) >c(OH-)
![]() B.0.1mol/L pH为4的NaHB溶液中:
B.0.1mol/L pH为4的NaHB溶液中:
c(HB-)>c(H2B)>c(B2-)
![]() C.硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:
C.硫酸氢铵溶液中滴加氢氧化钠至溶液恰好呈中性:
c(Na+)> c(SO42-)> c(NH4+)> c(OH-)= c(H+)
![]() D.PH相等的(NH4)2SO4溶液,(NH4)2Fe(SO4)2溶液和NH4Cl溶液:
D.PH相等的(NH4)2SO4溶液,(NH4)2Fe(SO4)2溶液和NH4Cl溶液:
![]() c[(NH4)2SO4]<c[(NH4)2Fe(SO4)2]<c(NH4Cl)
c[(NH4)2SO4]<c[(NH4)2Fe(SO4)2]<c(NH4Cl)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com