
科目: 来源: 题型:
(10分)江苏东海有蛭石。蛭石为一种层状结构的含镁的水铝硅酸盐,是黑云母等天然矿物风化蚀变的产物,因为其受热膨胀时呈挠曲状,形态酷似水蛭,故此得名蛭石。膨化后的蛭石呈颗粒状,有隔热、耐冻、抗菌、防火、吸声等优异性能,但不耐酸。
(1)某硅酸盐矿石的组成可以看作SiO2中有1/3的Si被Al置换,再由K平衡其电荷形成的。该矿石得组成以氧化物的形式表示为 。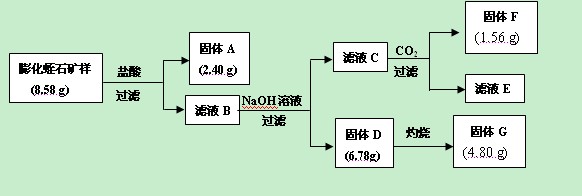
(2)某校研究性学习小组取得了某种牌号的膨化蛭石样品,其成分可以用氧化物(MgO、Fe2O3、Al2O3、SiO2、H2O)的形式表示。为研究蛭石的组成,拟进行实验探究,实验流程及相关数据如下:
①固体A的化学式是
②固体F的物质的量是
③通过计算,给出用氧化物的形式表示某种膨化蛭石组成的化学式
查看答案和解析>>
科目: 来源: 题型:
(10分)请仔细观察两种电池的构造示意图,
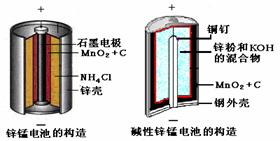
回答下列问题:
(1)碱性锌锰电池的总反应式:
Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,
则负极的电极反应式:
(2)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是
(3)某工厂回收废旧锌锰电池,其工艺流程如下:
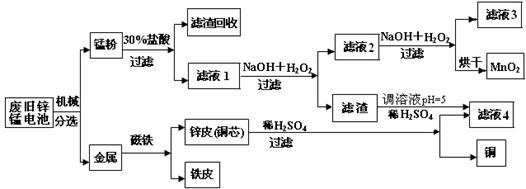
已知:生成氢氧化物的pH如下表:
物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2 |
开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
完全沉淀pH | 3.7 | 9.6 | 8.0 | 9.8 |
①经测定,“锰粉”中除含少量铁盐和亚铁盐外,主要成分应是MnO2、Zn(OH)2 。
②第一次加入H2O2后,调节pH=8.0。目的是 。
③试列举滤液4的应用实例 。
查看答案和解析>>
科目: 来源: 题型:
(8分)A、B、C、D都是中学化学常见的物质,其中A、B、C均含有同一种元素。在一定条件下相互转化的关系如下图所示(部分反应中的H2O已略去)。请按要求回答下列问题:
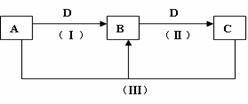 |
(1)若D为金属单质,且D是用量最大、用途最广的金属,若加热蒸干B的溶液没有得到B的盐,则B的化学式可能为 。
(2)A常用作制冷剂,B和D为空气的主要成分,则反应(Ⅲ)的化学方程式为 。
(3)D为氯碱工业的重要产品,反应(Ⅲ)的离子方程式可以是 。
(4)D为酸或酸性气体,则A、B、C、D可以是 (请按顺序写出合理任意一组物质的化学式即可)。
查看答案和解析>>
科目: 来源: 题型:
(10分)北京时间2008年2月21日上午11时26分,美国用导弹击毁了失控的卫星。美方称,卫星坠落地面时,燃料罐中装有的约453 kg联氨(N2H4),可能发生泄漏,造成伤害。
(1)联氨是一种无色可燃的液体,溶于水显碱性,其原理与氨相似,但其碱性不如氨强,写出其溶于水呈碱性的离子方程式: 。
(2)联氨(N2H4)是航天飞船常用的高能燃料。联氨可用氨和次氯酸钠按一定物质的量之比混合反应生成联氨、氯化钠和水;该反应的氧化产物是 。也可以采用尿素[CO(NH2)2]为原料制取,方法是在高锰酸钾催化剂存在下,尿素和次氯酸钠、氢氧化钠溶液反应生成联氨、另外两种盐和水,写出其反应的化学方程式 。
(3)火箭推进器中分别装有联氨和过氧化氢,当它们混合时即产生气体,并放出大量热。已知:12.8 g液态联氨与足量过氧化氢反应生成氮气和水蒸气,放出256.65 kJ的热量;
H2O(l)=H2O (g) DH=+44 kJ?mol-1
2H2O2(l)=2H2O(l)+ O2(g) DH=-196.4 kJ?mol-1
则写出表示联氨燃烧热的热化学方程式为 。
查看答案和解析>>
科目: 来源: 题型:
(10分)废旧塑料回收和利用是减轻“白色污染”、实现资源再利用的有效途径之一。某兴趣小组进行如下探究:
【实验课题】废旧聚丙烯塑料热分解主要产物的探究
【查阅资料】①石蜡热分解的产物为常温下的气态烃和液态烃
②CuO能将烃氧化成CO2和H2O
③苯甲酸能溶于苯
【实验设计】

【实验记录】
①B装置试管中有液态物质生成;②C中溴水的颜色变浅;③E装置中黑色氧化铜变红;
④F装置中无水硫酸铜变蓝。
【问题讨论】请你参与实验设计的评价和实验结果的分析:
(1)经分析得知B装置试管中的液态产物是甲苯和苯的混合物。若要除去其中的甲苯,实验操作方法是 ;
(2)C装置的作用是 ;
(3)如果不设置D装置,对实验结论产生的影响是 ;
(4)甲同学认为从C中出来的气体是氢气,乙同学认为还可能有其它成分。你认为其他成分可能是 。为完善实验设计,请在上图方框内画出装置图并注明其中盛放的试剂名称。
查看答案和解析>>
科目: 来源: 题型:
阿伏加德罗常数约为6.02×1023 mol-1,下列叙述正确的是
![]() A. 25℃时,
A. 25℃时,
![]() B.4.6 g Na在空气中完全反应生成Na2O、Na2O2,转移约0.2×6.02×1023个电子
B.4.6 g Na在空气中完全反应生成Na2O、Na2O2,转移约0.2×6.02×1023个电子
![]() C.1 mol羟基(-OH)所含的电子数约为10×6.02×1023
C.1 mol羟基(-OH)所含的电子数约为10×6.02×1023
![]() D.标准状况下,测得一定量的铜与硝酸反应后生成
D.标准状况下,测得一定量的铜与硝酸反应后生成
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com