
科目: 来源: 题型:
(10分)760℃和101.3kPa下,令氢气和氦气(体积比为1 :1)慢慢通过盛有熔融AgBr的舟皿,而使部分AgBr还原为Ag。然后让反应后的气体通过盛有40.00 mL 0.1000 mol?L-1NaOH的洗气瓶(溴单质被NaOH溶液吸收时,所生成的盐是两种强酸盐),并收集干燥后的尾气。某次实验后,洗气瓶内的溶液可以被l0.00 mL 0.1000 mol?L-1的HCl溶液中和,并在27.0℃ 101.3kPa下收集得干燥尾气492.4mL(已知760℃时纯HBr气体有16.67%分解为单质)。
(1)写出该实验过程中所发生的全部反应的方程式,并配平。
(2)计算舟皿中银单质的物质的量。
(3)计算尾气中氢气的物质的量。
查看答案和解析>>
科目: 来源: 题型:阅读理解
(本题共6分)
(1)化学是生命的语言,生命是建筑在原子、分子与复杂的化学反应之上的。根据大部 分已被接受的模型,宇宙开始于150亿年前的一次大爆炸,至今宇宙还在持续扩张。就整体 而言,当宇宙冷却时,宇宙的历史可以看作是从元素到复杂的粒子弋系列的收缩。当然,正如我们所知,生命在室温的地球是一种奇特的现象。
大部分的轻元素,如氢及氦,在大爆炸后扩张的几分钟内即形成。在宇宙中,当星球形 成时温度将由下降而开始回升。在化学领域中,星球是很重要的,因为生命所需的重元素是 由星球内部温度超过一千万度制造出来的。合理地排列下列的字符串,使其能符合宇宙中超 过99%都为氢或氦的事实。
a一( )一一( )一( )一( )-( )一-( )一( )
a.夸克→质子,中子
b.1014细胞→人类
c.H,C,N,O→H2,CH4,NH3,H20(在宇宙中)
d.质子,氦原子核+电子→中性H,He原子
e.蛋白质,核苷酸,细胞膜→第一个细胞
f.质子,中子→氦原子核
g.H2,He,CH4,NH3,H2O,灰尘→太阳系
h.H,He原子→再解离,第一个星球与银河生成
i.质子,氦原子(轻元素)→重元素,如C,N,O,只S,Fe,U;超新星爆炸
j.H2,CH4,NH3,H20等→地球上的氨基酸,糖类,氨基酸碱基,磷酸酯
(2)人体是由细胞所组成的,而细胞由原子组成。人体大约三分之二的质量是水,这表示细胞大约三分之二的质量是水。估算一个重60kg的人体约由多少个原子组成。(提示:可考虑一个水分子中三个原子的平均相对原子质量,再由你自己考虑其它分子如蛋白质、脂肪或碳水化合物的平均相对原子质量)
查看答案和解析>>
科目: 来源: 题型:
(8分)已知右图中所有物质均为化合物,A、 C的水溶液呈碱性,且C是一种强碱,F、G的水溶液呈酸性。B为红褐色沉淀,化合物G在常温下呈气态,其水溶液是一种常见的强酸,A、C、D、E焰色反应呈黄色。A、D的水溶液都有杀菌消毒作用。 A、B、C反应时,物质的量之比为3:2:4。其它物质相互间的转化关系如图所示(各反应在常温下即可发生;多数反应的生成物没有写完整)。请写出:
(1)A的化学式_____________,C的电子式:_________________;
(2)A、B、C三者发生反应的离子方程式:__________________________
(3)已知D和G反应时还有使带火星的木条复燃的气体产生,则D和G反应的化学方程式为:_ _。
查看答案和解析>>
科目: 来源: 题型:
(10分)铜是一种重要的金属元素,铜元素与银元素同处第ⅠB族,+l价的铜和+l价的银都可形成二配位的络离子,如Ag(NH3)2+、AgCl2-、Cu(CN)2-等,含铜最丰富的自然资 源是黄铜矿(CuFeS2)。
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转 变为铜,完成下列2个化学方程式:
①CuFeS2+O2一Cu2S+Fe3O4+SO2
②Cu2S+O2一
(2)但是,这种方法的缺点是副产物SO2会导致大气的污染,同时要消耗大量的热能。
现有一种湿法冶炼技术,其步骤是:
①用FeCl3、CuCl2的混合液处理富铜矿砂,使CuFeS2中的Cu转变为难溶的氯化物A,硫元素转变为硫单质沉淀
②将沉淀分离出来,用氯化钠溶液处理所得的沉淀物,使A溶解变成化合物B,从而和硫单质分离;
⑨控制条件使B在溶液中通过歧化反应生成铜,母液中的一种成分可以在处理铜矿砂时循环使用,指出A、B各是什么物质,写出①、③步中的化学方程式。
查看答案和解析>>
科目: 来源: 题型:
(8分)金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”美称;具有低密度、高强度,耐腐蚀、耐高温,记忆能力等优良性能。金属钛的制备主要包括下面几个步骤:
①用硫酸溶解钛铁精矿(FeTiO3),溶解后水浸、冷却、结晶得到副产品绿矾;
②所得滤液水解充分后得到沉淀A和稀硫酸,稀硫酸循环利用;
③高温煅烧沉淀A得到化合物B,B是重要的白色颜料;
④化合物B在高温条件下氯化时得到化合物C和一氧化碳气体,其中C在常温下呈液态,且极易水解,可以用作军事烟雾剂;
⑤高温下用金属镁还原C得到金属钛。
(1)金属钛在加热时可以与浓NaOH溶液作用,写出钛与热的浓碱作用时的离子方程式:_____________________;写出主族金属元素中与此相似的一个离子反应方程式:_____________________________________。
(2)写出第④步的化学反应方程式____________________________。
(3)用化学方程式表示C为什么可以用作军事烟雾剂:_________________________。
查看答案和解析>>
科目: 来源: 题型:
 (9分).已知下列物质的物理常数如下:苯甲酸:白色固体,密度1.2659,熔点122℃,沸点249℃。甲醇:无色液体,密度0.7915, 熔点-97.8℃,沸点64.65℃。苯甲酸甲酯:无色液体,密度1.0888,熔点-12.3℃,沸点199.6℃。乙酸:熔点16.6℃,沸点117.9℃。乙醇:熔点一117.3℃,沸点78.5℃。乙酸乙酯:熔点-83.6℃,沸点77.1℃
(9分).已知下列物质的物理常数如下:苯甲酸:白色固体,密度1.2659,熔点122℃,沸点249℃。甲醇:无色液体,密度0.7915, 熔点-97.8℃,沸点64.65℃。苯甲酸甲酯:无色液体,密度1.0888,熔点-12.3℃,沸点199.6℃。乙酸:熔点16.6℃,沸点117.9℃。乙醇:熔点一117.3℃,沸点78.5℃。乙酸乙酯:熔点-83.6℃,沸点77.1℃
![]() (1).下图为课本上制取乙酸乙酯的实验装置图,请回答下列问题:①实验室制备乙酸乙酯的化学方程式为___________________________;
(1).下图为课本上制取乙酸乙酯的实验装置图,请回答下列问题:①实验室制备乙酸乙酯的化学方程式为___________________________;
![]()
 ②用上述装置制取乙酸乙酯时,为提高原料乙酸的利用率所采取的措施有_____________;
②用上述装置制取乙酸乙酯时,为提高原料乙酸的利用率所采取的措施有_____________;
![]() (2).实验室用苯甲酸和甲醇反应制取苯甲酸甲酯时用了右图装置(画图时省略了铁夹、导管等仪器):①实验室制取苯甲酸甲酯为什么不同样使用制取乙酸乙酯的装置?
(2).实验室用苯甲酸和甲醇反应制取苯甲酸甲酯时用了右图装置(画图时省略了铁夹、导管等仪器):①实验室制取苯甲酸甲酯为什么不同样使用制取乙酸乙酯的装置?![]() ____________________________________________;
____________________________________________;
![]() ②制得的产品含有多种杂质,如何提纯产品(只需写出所用试剂和操作名称)?
②制得的产品含有多种杂质,如何提纯产品(只需写出所用试剂和操作名称)?![]() ______________________________________________________________
______________________________________________________________
查看答案和解析>>
科目: 来源: 题型:
(4分)铜不能与稀硫酸直接反应,本实验中将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶可制得硫酸铜晶体(装置如图1、2所示)。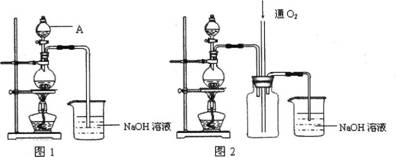
(1)把浓硝酸分多次加入到铜粉与稀硫酸的混合物中的目的是_________________________。
(2)图2是图1的改进装置, 其优点除可以防止倒吸外还有:_______________________。
查看答案和解析>>
科目: 来源: 题型:阅读理解
(14分)由乙酰水杨酸(ASS)制成的阿司匹林是德国一家制药公司于1899年合成出的止痛剂(Pain Reliefers)。长时间以来一直被广泛的使用,现在每年的需求量仍是很高。ASS可由下列反应序列合成制得:
![]()

(1)写出A与B的结构简式及B与乙酸酐反应的化学方程式
(2)B物质与乙酸酐反应时,还会生成一些副产品,其中有一种是高分子,其结构简式为__________。为了除去此物质,可在产物中加入_______溶液,再经过滤、酸化等步骤可得较纯净的ASS。
(3)为了测定自制乙酰水杨酸的纯度,一般可采用以下步骤:准确称取自制的乙酰水杨酸三份,每份约0.25g,分别置于250mL锥形瓶中,加入25 mL 95%乙醇(已调至对酚酞指示剂显中性),摇动使其溶解,再向其中加入适量酚酞指示剂,用准确浓度的NaOH溶液滴定至出现微红色,30秒钟不变色为终点,分别记录所消耗NaOH溶液的体积,根据所消耗NaOH溶液的体积,分别计算乙酰水杨酸的质量分数。在上述测定过程中,为防止乙酰水杨酸在滴定过程中水解,应如何正确操作?并说明理由。
(4)为了测定阿司匹林片剂中乙酰水杨酸的含量,通常采用返滴定法。步骤为:称取10片药物(设总质量为w总/g),研细混匀后,准确称取一定量(G/g)药粉于锥形瓶中,加入V1/mL(过量)的NaOH标准溶液[浓度c(NaOH)/mol?L-1],于水浴上加热使乙酰基水解完全后,再用HCl标准溶液[浓度c(HCl)/mol?L-1]回滴,以酚酞为指示剂,耗去HCl溶液V2/mL。请列出求算每片药中含有乙酰水杨酸的质量(g/片)的计算式。
![]() 已知乙酰水杨酸可溶于NaOH溶液中,并生成水杨酸盐和乙酸盐。其溶解反应式可表示为:
已知乙酰水杨酸可溶于NaOH溶液中,并生成水杨酸盐和乙酸盐。其溶解反应式可表示为:
![]()

![]() 乙酰水杨酸的摩尔质量为180.2g?mol-1,水杨酸的pKal=3.0,pKa2=13.1,乙酸的pKa=4.75
乙酰水杨酸的摩尔质量为180.2g?mol-1,水杨酸的pKal=3.0,pKa2=13.1,乙酸的pKa=4.75
查看答案和解析>>
科目: 来源: 题型:
(9分)高效、低毒农药杀灭菊酯的合成路线如下:
![]()
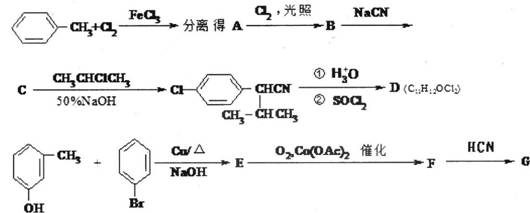
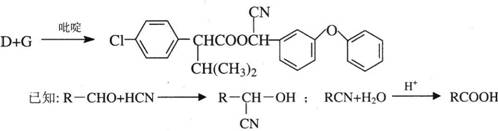
(1)写出A、B、C、D、E、F、G的结构简式。
A__________ B__________ C__________ D__________ E__________ G__________
(2)写出E→F的化学方程式____________________
查看答案和解析>>
科目: 来源: 题型:
酸A是某抗氧化剂成分之一,A与FeCl3溶液反应显紫色,A能使Br2-CCl4溶液褪色。
![]()
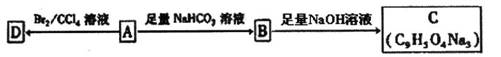
![]() 现已知A中苯环上含有三个取代基,则A的可能结构有
现已知A中苯环上含有三个取代基,则A的可能结构有
A.6种 B.9种 C. 12种 D.15种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com